Toimeained: imatiniib
Glivec 50 mg kõvakapslid
Gliveci pakendi infolehed on saadaval järgmistes pakendisuurustes:- Glivec 50 mg kõvakapslid
- Glivec 100 mg kõvakapslid
Näidustused Miks Gliveci kasutatakse? Milleks see mõeldud on?
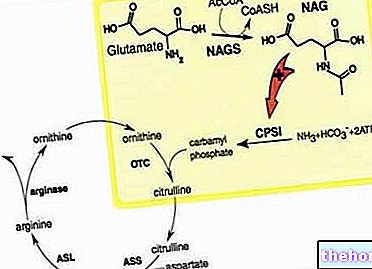
Glivec on ravim, mis sisaldab toimeainena imatiniibi. Allpool loetletud haiguste korral pärsib see ravim ebanormaalsete rakkude kasvu. Nende hulka kuuluvad teatud tüüpi vähid.
Glivec on näidustatud täiskasvanutel ja lastel järgmiste haiguste raviks:
- Krooniline müeloidne leukeemia (KML). Leukeemia on valgete vereliblede vähk. Valged verelibled aitavad tavaliselt kehal infektsioonidega võidelda. Krooniline müeloidne leukeemia on leukeemia vorm, mille puhul teatud ebanormaalsed valged verelibled (nn müeloidrakud) hakkavad kontrolli alt väljuma.
- Philadelphia kromosoomi positiivne äge lümfoblastne leukeemia (Ph + ALL). Leukeemia on valgete vereliblede vähk. Valged verelibled aitavad tavaliselt kehal infektsioonidega võidelda. Äge lümfoblastne leukeemia on leukeemia vorm, mille puhul teatud ebanormaalsed valged verelibled (nn lümfoblastid) hakkavad kontrolli alt väljuma. Glivec pärsib nende rakkude kasvu.
Glivec on näidustatud ka täiskasvanud patsientidel järgmiste haiguste raviks:
- Müelodüsplastilised / müeloproliferatiivsed haigused (MDS / MPD). Need on verehaiguste rühm, mille puhul mõned vererakud hakkavad kontrollimatult kasvama. Glivec pärsib nende rakkude kasvu nende haiguste teatud alatüüpides.
- Hüpereosinofiilne sündroom (HES) ja / või krooniline eosinofiilne leukeemia (CEL). Need on verehaigused, mille puhul vererakud (nn eosinofiilid) hakkavad kontrollimatult kasvama. Glivec pärsib nende rakkude kasvu nende haiguste teatud alatüübis.
- Seedetrakti pahaloomulised strooma kasvajad (GIST). GIST on mao ja soolte neoplasm, mis tuleneb nende elundite kudesid toetavate rakkude kontrollimatu kasvust.
- Protuberaanne Dermatofibrosarcoma (DFSP). DFSP on nahaaluskoe kasvaja, milles mõned rakud hakkavad kontrolli alt väljuma. Glivec pärsib nende rakkude kasvu.
Selle infolehe ülejäänud osas kasutatakse nende haiguste arutamisel lühendeid.
Kui teil on küsimusi selle kohta, kuidas Glivec toimib või miks teile Gliveci välja kirjutati, pidage nõu oma arstiga.
Vastunäidustused Gliveci ei tohi kasutada
Gliveci määravad teile ainult arstid, kellel on kogemusi verevähi ja tahkete kasvajate ravimitega.
Järgige hoolikalt kõiki arsti juhiseid, isegi kui need erinevad selles infolehes sisalduvast üldisest teabest.
Ärge võtke Gliveci:
- kui olete imatiniibi või selle ravimi mis tahes koostisosade (loetletud lõigus 6) suhtes allergiline.
Kui see kehtib teie kohta, konsulteerige oma arstiga ilma Gliveci võtmata.
Kui arvate, et võite olla allergiline, kuid pole selles kindel, küsige nõu oma arstilt
Ettevaatusabinõud kasutamisel Mida on vaja teada enne Gliveci võtmist
Enne Gliveci võtmist pidage nõu oma arstiga:
- kui teil on või on kunagi olnud maksa-, neeru- või südameprobleeme.
- kui te võtate levotüroksiini kilpnäärme eemaldamise tõttu.
Kui mõni neist kehtib teie kohta, pidage enne Gliveci võtmist nõu oma arstiga.
Rääkige Glivec -ravi ajal kohe oma arstile, kui te võtate väga kiiresti kaalus juurde. Glivec võib põhjustada teie kehas veepeetust (raske vedelikupeetus).
Gliveci võtmise ajal peab arst regulaarselt kontrollima, kas ravim on efektiivne. Lisaks tehakse teile vereanalüüse ja teid kaalutakse regulaarselt.
Lapsed ja noorukid
Glivec on ka ravi KML -iga lastele. Puudub "kogemus alla 2 -aastaste KML -iga laste kohta. Ph + ALL -ga lastel on vähe kogemusi ja MDS / MPD, DFSP, GIST ja HES / CEL -ga laste kogemus on väga piiratud."
Mõnedel Gliveci võtvatel lastel ja noorukitel võib kasv olla tavalisest aeglasem. Arst kontrollib kasvu regulaarselt.
Koostoimed Millised ravimid või toiduained võivad Gliveci toimet muuta
Teatage oma arstile või apteekrile, kui te kasutate, olete hiljuti kasutanud või kavatsete kasutada mis tahes muid ravimeid, kaasa arvatud ilma retseptita ostetud ravimeid (nt atsetaminofeen) ja taimseid ravimeid (nt naistepuna). Mõned ravimid võivad mõjutada Gliveci toime koosmanustamisel. Need võivad suurendada või vähendada Gliveci toimet, põhjustades rohkem kõrvaltoimeid või vähendades Gliveci efektiivsust. Glivec võib sama teha ka teiste ravimitega.
Öelge oma arstile, kui kasutate verehüübeid ennetavaid ravimeid.
Hoiatused Oluline on teada, et:
Rasedus. imetamine ja viljakus
- Kui te olete rase, imetate või arvate end olevat rase või kavatsete rasestuda, pidage enne selle ravimi kasutamist nõu oma arstiga.
- Gliveci ei soovitata raseduse ajal kasutada, kui see ei ole hädavajalik, kuna see võib imikut kahjustada. Arst arutab teiega Gliveci raseduse ajal kasutamise võimalikke riske.
- Naistel, kes võivad rasestuda, soovitatakse ravi ajal kasutada tõhusaid rasestumisvastaseid vahendeid.
- Glivec -ravi ajal ei tohi last rinnaga toita.
- Patsientidel, kes on Glivec -ravi ajal oma viljakuse pärast mures, soovitatakse konsulteerida oma arstiga.
Autojuhtimine ja masinatega töötamine
Selle ravimi võtmise ajal võite tunda pearinglust või unisust või nägemishäired. Kui see juhtub, ärge juhtige autot ega kasutage tööriistu ega masinaid enne, kui tunnete end hästi.
Annus, manustamisviis ja manustamisaeg Kuidas Gliveci kasutada: Annustamine
Arst on teile määranud Gliveci, kuna teil on raske haigus. Glivec aitab teil selle seisundiga võidelda.
Võtke seda ravimit siiski alati täpselt nii, nagu arst või apteeker on teile rääkinud.
Oluline on seda teha seni, kuni arst või apteeker seda soovitab. Kui te ei ole milleski kindel, küsige oma arstilt või apteekrilt. Ärge lõpetage Gliveci riputamist, kui arst pole seda käskinud. Kui te ei saa oma ravimit ettenähtud viisil võtta. pöörduge oma arsti poole või tunnete, et te ei vaja seda enam, võtke kohe ühendust oma arstiga.
Kui palju Gliveci võtta
Kasutamine täiskasvanutel
Arst ütleb teile täpselt, mitu Glivec'i kapslit võtta.
- Kui teil ravitakse KML -i:
Sõltuvalt teie seisundist on tavaline algannus 400 mg või 600 mg:
- 400 mg tuleb võtta 8 kapslina üks kord ööpäevas
- 600 mg tuleb võtta 12 kapslina üks kord ööpäevas.
- Kui teil ravitakse GIST -i:
Algannus on 400 mg, mis võetakse 8 kapslina kord päevas.
CML -i ja GIST -i korral võib arst määrata teile suurema või väiksema annuse, sõltuvalt sellest, kuidas te ravile reageerite. Kui ööpäevane annus on 800 mg (16 kapslit), peate võtma 8 kapslit hommikul ja 8 kapslit õhtul. - Kui teid ravitakse Ph + ALL vastu: Algannus on 600 mg, mis tuleb võtta 12 kapslina üks kord ööpäevas. - Kui teil ravitakse MSD / MPD -d: Algannus on 400 mg, mis tuleb võtta 8 kapslina üks kord ööpäevas. - Kui teid ravitakse HES / CLE -ga: Algannus on 100 mg, mis tuleb võtta 2 kapslina üks kord päevas. Teie arst võib otsustada suurendada annust 400 mg -ni, mida võetakse 8 kapslina üks kord päevas, sõltuvalt teie ravivastusest. - Kui teil ravitakse DFSP -d: Annus on 800 mg ööpäevas (16 kapslit), mis tuleb võtta 8 kapslina hommikul ja 8 kapslina õhtul. Kasutamine lastel ja noorukitel Arst ütleb teile, kui palju Gliveci kapsleid lapsele anda. Gliveci manustatav kogus sõltub lapse seisundist, tema kaalust ja pikkusest. Päevane koguannus ei tohi KML -iga lastel ületada 800 mg ja Ph + ALL -ga lastel 600 mg. Ravi võib anda lapsele ühekordse ööpäevase annusena või teise võimalusena jagada päevane annus kaheks manustamiskorraks (pool hommikul ja pool õhtul). Millal ja kuidas Gliveci võtta Kui kaua Gliveci võtta Jätkake Gliveci võtmist iga päev nii kaua, kui arst on teile öelnud. Kui te võtate Gliveci rohkem kui ette nähtud Kui olete kogemata võtnud liiga palju kapsleid, võtke kohe ühendust oma arstiga. Teil võib tekkida vajadus arstiabi järele. Võtke ravimikarp kaasa. Kui te unustate Gliveci võtta Kui teil on lisaküsimusi selle ravimi kasutamise kohta, pidage nõu oma arsti, apteekri või meditsiiniõega. Nagu kõik ravimid, võib ka see ravim põhjustada kõrvaltoimeid, kuigi kõigil neid ei teki. Need on tavaliselt kerged kuni mõõdukad. Mõned kõrvaltoimed võivad olla tõsised. Rääkige kohe oma arstile, kui teil tekib mõni järgmistest: Väga sage (võib esineda rohkem kui 1 inimesel 10 -st) või sage (võib esineda kuni 1 inimesel 10 -st): Aeg -ajalt (võib esineda kuni 1 inimesel 100 -st) või harv (võib esineda kuni 1 inimesel 1000 -st): Teadmata (esinemissagedust ei saa hinnata olemasolevate andmete alusel): Kui teil tekib mõni ülalkirjeldatud toime, rääkige sellest otsekohe oma arstile. Muud kõrvaltoimed võivad hõlmata järgmist: Väga sage (võib esineda rohkem kui 1 inimesel 10 -st): Kui mõni neist mõjutab teid tõsiselt, rääkige sellest oma arstile. Sage (võib esineda kuni 1 inimesel 10 -st): Kui mõni neist mõjutab teid tõsiselt, rääkige sellest oma arstile. Teadmata (esinemissagedust ei saa hinnata olemasolevate andmete alusel): Kõrvaltoimetest teatamine Kui teil tekib ükskõik milline kõrvaltoime, pidage nõu oma arsti, apteekri või meditsiiniõega. Kõrvaltoime võib olla ka selline, mida selles infolehes ei ole nimetatud. Kõrvaltoimetest võite ka ise teavitada otse riikliku teavitussüsteemi kaudu, mis on loetletud lisas V. Kõrvaltoimed, mida saate aidata lisateavet selle ravimi ohutuse kohta. Mida Glivec sisaldab Gliveci välimuse ja pakendi sisu kirjeldus Glivec 50 mg kapslid on helekollast kuni kollakasoranži värvi ja märgistusega "NVR SH". Need sisaldavad valget kuni kollast pulbrit. Neid tarnitakse 30 kapsliga pakendites. Allika pakendi infoleht: AIFA (Itaalia ravimiamet). Sisu avaldati jaanuaris 2016. Esitatud teave ei pruugi olla ajakohane. GLIVEC 50 MG KÕVAD KAPSLID Iga kapsel sisaldab 50 mg imatiniibi (mesülaadina). Abiainete täielik loetelu vt lõik 6.1. Kõva kapsel Valge kuni kollane pulber helekollasest kuni kollakasoranžini läbipaistmatusse kapslisse, millele on trükitud "NVR SH". Glivec on näidustatud raviks • täiskasvanud ja pediaatrilised patsiendid, kellel on äsja diagnoositud Philadelphia kromosoomi (bcr-abl) positiivne (Ph +) krooniline müeloidne leukeemia (KML) ja kellele luuüdi siirdamist ei peeta esmavaliku raviks. • täiskasvanud ja pediaatrilised patsiendid, kellel on krooniline faas Ph + CML pärast interferoon-alfa-ravi ebaõnnestumist või kiirendatud faasi või plahvatuskriisi. • täiskasvanud ja lapsed, kellel on äsja diagnoositud Philadelphia kromosoompositiivne äge lümfoblastne leukeemia (Ph + ALL), millele on lisatud keemiaravi. • täiskasvanud patsiendid, kellel on retsidiivne või refraktaarse Ph + ALL monoteraapiana. • täiskasvanud patsiendid, kellel on müelodüsplastilised / müeloproliferatiivsed haigused (MDS / MPD), mis on seotud trombotsüütidest pärineva kasvufaktori retseptori (PDGFR) geeni ümberkorraldustega. • kaugelearenenud hüpereosinofiilse sündroomiga (HES) ja / või kroonilise eosinofiilse leukeemiaga (CEL) täiskasvanud patsiendid, kellel on FIP1L1-PDGFRa ümberkorraldused. Gliveci mõju luuüdi siirdamise tulemustele ei ole kindlaks tehtud. Glivec on näidustatud • eemaldatavate ja / või metastaatiliste pahaloomuliste seedetrakti strooma kasvajate (GIST) täiskasvanud patsientide ravi, Kit -positiivne (CD 117). • adjuvantravi täiskasvanud patsientidel, kellel on märkimisväärne retsidiivide oht pärast Kit -positiivsete GIST -ide resektsiooni (CD 117). Patsiendid, kellel on madal või väga väike retsidiivide oht, ei tohi adjuvantravi saada. • täiskasvanud patsientide, kellel on eemaldamatu dermatofibrosarkoom protuberans (DFSP), ja retsidiivse ja / või metastaatilise DFSP -ga täiskasvanud patsientide ravi, kes ei sobi operatsiooniks. Gliveci efektiivsus täiskasvanutel ja lastel põhineb üldisel hematoloogilisel ja tsütogeneetilisel ravivastusel ning progresseerumiseta elulemusel KML-is, hematoloogilise ja tsütogeneetilise ravivastuse väärtustel Ph + ALL, MDS / MPD, hematoloogilise ravivastuse väärtustel HES / CLE ja objektiivse raviväärtuse kohta täiskasvanud patsientidel, kellel on GIST ja DFSP, mida ei ole võimalik eemaldada ja / või metastaatiline ning kellel on GIST-i adjuvantravi. piiratud (vt lõik 5.1). Puuduvad kontrollitud kliinilised uuringud, mis näitaksid nende seisundite kliinilist kasu või suurenenud elulemust, välja arvatud need, mis viidi läbi äsja diagnoositud kroonilise faasi KML -is. Ravi võib alustada vastavalt vajadusele hematoloogiliste kasvajate ja pahaloomuliste sarkoomidega patsientide ravis kogenud arst. Seedetrakti ärrituse ohu vähendamiseks tuleb ettenähtud annus manustada suu kaudu, söögi ajal ja suure klaasi veega. 800 mg ööpäevas tuleb manustada 400 mg kaks korda päevas, hommikul ja õhtul. Patsientidele (lastele), kes ei saa kapsleid alla neelata, võib sisu lahjendada klaasi gaseerimata veega või õunamahlaga. Kuna loomkatsed on näidanud reproduktiivtoksilisuse märke ja potentsiaalne oht inimese lootele ei ole teada, peavad kapsleid avavad fertiilses eas naised selle sisu käsitsema ettevaatlikult ning vältima silma sattumist või sissehingamist (vt lõik 4.6). pesta kohe pärast avatud kapslite käsitsemist. Annustamine CML täiskasvanud patsientidel Kroonilise faasi KML -iga täiskasvanud patsientidel on Gliveci soovitatav annus 400 mg ööpäevas. KML on krooniline, kui on täidetud kõik järgmised kriteeriumid: veri ja luuüdi plahvatab perifeerses veres basofiilid trombotsüüdid> 100 x 109 / l. Kiirendatud faasis täiskasvanud patsientidele on Gliveci soovitatav annus 600 mg ööpäevas. Kiirendatud faasi määratleb mis tahes järgmine: blastid veres või luuüdis ≥15%, kuid Plahvatuskriisis täiskasvanud patsientidele on Gliveci soovitatav annus 600 mg ööpäevas. Blastkriisi määratletakse vere- või luuüdi blastide esinemisega ≥ 30% või muu ekstramedullaarse haigusega peale hepatosplenomegaalia. Ravi kestus: Kliinilistes uuringutes jätkus Glivec -ravi kuni haiguse progresseerumiseni. Ravi lõpetamise mõju pärast täieliku tsütogeneetilise ravivastuse saavutamist ei ole uuritud. Kroonilise faasi haigusega patsientidel võib annuseid suurendada 400 mg -lt 600 mg -le või 800 mg -le või kroonilise faasiga patsientidel 600 mg -lt maksimaalselt 800 mg -le (400 mg kaks korda ööpäevas). tõsiste kõrvaltoimete puudumine ja raske neutropeenia või trombotsütopeenia, mis ei ole seotud leukeemiaga järgmistel tingimustel: haiguse progresseerumine (igal ajal); rahuldava hematoloogilise ravivastuse puudumine pärast vähemalt 3 -kuulist ravi; tsütogeneetilise ravivastuse puudumine pärast 12 -kuulist ravi; või varem saadud hematoloogilise ja / või tsütogeneetilise vastuse kadumine. Patsiente tuleb hoolikalt jälgida annuse suurendamise suhtes, arvestades võimalike kõrvaltoimete esinemissageduse suurenemist suuremate annuste kasutamisel. Annustamine KML -i raviks lastel Pediaatriliste patsientide annused tuleb arvutada kehapinna alusel (mg / m2). Kroonilise ja kaugelearenenud KML -iga lastele on soovitatav ööpäevane annus 340 mg / m2 (mitte ületada koguannust 800 mg). Päevase koguannuse võib võtta ühe annusena või jagada kaheks annuseks, üks hommikul ja teine õhtul. Annustamissoovitused põhinevad praegu piiratud arvul lastel (vt lõigud 5.1 ja 5.2).Puuduvad andmed alla 2 -aastaste laste ravi kohta. Lastel on võimalik ööpäevast annust suurendada 340 mg / m2 -lt 570 mg / m2 -le (mitte ületada koguannust 800 mg), kui puuduvad tõsised kõrvaltoimed ja raske neutropeenia või trombotsütopeenia, mis ei ole seotud leukeemiaga. järgmistel asjaoludel: haiguse progresseerumine (igal ajal); rahuldava hematoloogilise ravivastuse saavutamata jätmine pärast vähemalt 3 -kuulist ravi, tsütogeneetilise ravivastuse puudumine pärast 12 -kuulist ravi; või varem saadud hematoloogiliste ja / või Patsiente tuleb pärast annuse suurendamist hoolikalt jälgida, arvestades suuremate annuste kõrvaltoimete esinemissageduse suurenemist. Annustamine Ph + ALL korral täiskasvanud patsientidel Ph + ALL -ga täiskasvanud patsientidele on Gliveci soovitatav annus 600 mg päevas. Hematoloogid Selle haiguse ravi eksperdid peavad jälgima ravi kõigil ravi etappidel. Ravi ajakava: Olemasolevate andmete põhjal on Glivec osutunud efektiivseks ja ohutuks, kui seda manustatakse 600 mg ööpäevas kombinatsioonis keemiaraviga induktsiooni-, konsolideerumis- ja säilitusfaasis (vt lõik 5.1), mida kasutatakse täiskasvanud patsientide ravis. äsja diagnoositud Ph + ALL Glivec -ravi kestus võib varieeruda sõltuvalt valitud raviskeemist, kuid üldiselt on Gliveci pikema kokkupuute korral saavutatud paremaid tulemusi. Taastunud või refraktaarse Ph + ALL -ga täiskasvanud patsientidele on Gliveci monoteraapia annuses 600 mg ööpäevas ohutu, efektiivne ja seda võib manustada kuni haiguse progresseerumiseni. Annustamine Ph + ALL korral lastel Pediaatriliste patsientide annused tuleb arvutada kehapinna alusel (mg / m2). Ph + ALL -ga lastele on soovitatav päevane annus 340 mg / m2 (mitte ületada 600 mg koguannust). Annustamine MDS / MPD korral MDS / MPD -ga täiskasvanud patsientidele on Gliveci soovitatav annus 400 mg ööpäevas. Ravi kestus: Ainsas seni läbi viidud kliinilises uuringus jätkati ravi Gliveciga kuni haiguse progresseerumiseni (vt lõik 5.1). Analüüsi ajal oli ravi keskmine kestus 47 kuud (24 päeva - 60 kuud). Annustamine HES / CLE korral HES / CEL -ga täiskasvanud patsientidele on Gliveci soovitatav annus 100 mg ööpäevas. Ravimi kõrvaltoimete puudumisel võib kaaluda annuse suurendamist 100 mg -lt 400 mg -le, kui hindamised näitavad ebapiisavat ravivastust. Ravi tuleb jätkata seni, kuni patsient sellest kasu saab. Annustamine GIST -ile Täiskasvanud patsientidel, kellel on eemaldatav ja / või metastaatiline pahaloomuline GIST, on Gliveci soovitatav annus 400 mg ööpäevas. Andmete suurendamise mõju kohta 400 mg -lt 600 mg -le või 800 mg -le patsientidel, kes lähevad madalamale annusele, on vähe andmeid (vt lõik 5.1). Ravi kestus: GIST -ga patsientidel läbi viidud kliinilistes uuringutes jätkati Glivec -ravi kuni haiguse progresseerumiseni. Analüüsi ajal oli ravi kestus keskmiselt 7 kuud (7 päeva kuni 13 kuud). Ravi lõpetamise mõju pärast ravivastuse saavutamist ei ole uuritud. GIST -ga täiskasvanud patsientidel on pärast resektsiooni Gliveci soovitatav annus adjuvantraviks 400 mg ööpäevas. Adjuvantravi optimaalne kestus ei ole veel kindlaks määratud. Ravi kestus seda näidustust toetavas kliinilises uuringus oli 36 kuud (vt lõik 5.1). Annustamine DFSP jaoks DFSP -ga täiskasvanud patsientidele on Gliveci soovitatav annus 800 mg päevas. Annuse kohandamine kõrvaltoimete korral Mittehematoloogilised kõrvaltoimed Kui Gliveci kasutamisel ilmneb mittehematoloogiline kõrvaltoime, tuleb ravi katkestada kuni sündmuse lahenemiseni. Seejärel võib ravi vastavalt vajadusele jätkata, sõltuvalt sündmuse esialgsest tõsidusest. Kui bilirubiinisisaldus tõuseb üle 3 -kordse IULN -i institutsionaalse ülempiiri või maksa transaminaaside tase ületab 5 -kordselt IULN -i piiri, tuleb Glivec -ravi katkestada seni, kuni bilirubiin on taastunud alla 1,5 -kordse väärtuse IULN -i piir ja transaminaaside tase alla 2,5 -kordse piiri. Glivec -ravi võib jätkata vähendatud päevase annusega. Täiskasvanutel tuleb annust vähendada 400 mg -lt 300 mg -le või 600 mg -lt 400 mg -le või 800 mg -lt 600 mg -le ja lastel 340 mg -lt 260 mg / m2 -le päevas. Hematoloogilised kõrvaltoimed Raske neutropeenia ja trombotsütopeenia korral on soovitatav annust vähendada või ravi katkestada, nagu on näidatud allolevas tabelis. Annuse kohandamine neutropeenia ja trombotsütopeenia korral: Patsientide teatud kategooriad Kasutamine lastel: puuduvad kogemused alla 2 -aastaste KML -iga laste ja alla 1 -aastaste Ph + ALL -ga laste kohta (vt lõik 5.1). Kogemus MDS / MPD, DFSP, GIST ja HES / LEC -ga lastel on väga piiratud. Imatiniibi ohutust ja efektiivsust alla 18 -aastastel lastel, kellel on MDS / MPD, DFSP, GIST ja HES / CEL, ei ole kliinilistes uuringutes tõestatud. Praegu kättesaadavad avaldatud andmed on kokku võetud lõigus 5.1, kuid neile ei saa anda soovitusi annustamise kohta . Maksapuudulikkus: imatiniib metaboliseerub peamiselt maksas. Kerge, mõõduka või raske maksafunktsiooni häirega patsientidele tuleb anda minimaalne soovitatav annus 400 mg ööpäevas. Kui seda ei taluta, võib annust vähendada (vt lõigud 4.4, 4.8 ja 5.2). Maksapuudulikkuse klassifikatsioon: ULN = asutuse normi ülempiir AST = aspartaataminotransferaas Neerupuudulikkus: Neerufunktsiooni häirega või dialüüsi saavatele patsientidele tuleb algannuseks anda minimaalne soovitatav annus 400 mg ööpäevas. Siiski on nendel patsientidel soovitatav olla ettevaatlik. Kui seda ei taluta, võib annust vähendada. Tolerantsuse korral võib annust efektiivsuse puudumise tõttu suurendada (vt lõigud 4.4 ja 5.2). Vanemad inimesed: imatiniibi farmakokineetikat eakatel ei ole spetsiaalselt uuritud. Täiskasvanud patsientidel ei täheldatud kliinilistes uuringutes, milles osales üle 20% 65-aastastest ja vanematest patsientidest, olulisi vanusega seotud farmakokineetilisi erinevusi. Vanematel inimestel ei ole spetsiifilisi annuse soovitusi vaja. Ülitundlikkus toimeaine või lõigus 6.1 loetletud mis tahes abiainete suhtes. Gliveci manustamisel koos teiste ravimitega on võimalik ravimite koostoime. Gliveci manustamisel koos proteaasi inhibiitorite, seenevastaste asoolide, mõnede makroliididega (vt lõik 4.5), kitsa terapeutilise aknaga CYP3A4 substraatidega (nt tsüklosporiin, pimosiid, takroliimus, siroliimus, ergotamiin, diergotamiin, fentanüül, alfentaniil, terfenadiin, bortesomiib) tuleb olla ettevaatlik , dotsetakseel, kinidiin) või varfariin ja teised kumariini derivaadid (vt lõik 4.5). Imatiniibi ja CYP3A4 indutseerivate ravimite (nt deksametasoon, fenütoiin, karbamasepiin, rifampitsiin, fenobarbitaal võiHypericum perforatum(tuntud ka kui naistepuna) võib oluliselt vähendada Gliveci ekspositsiooni, suurendades potentsiaalselt ravi ebaõnnestumise riski. Seetõttu tuleks vältida tugevate CYP3A4 indutseerijate ja imatiniibi samaaegset kasutamist (vt lõik 4.5). Hüpotüreoidism Glivec -ravi ajal levotüroksiini asendusravi saanud patsientidel, kellel on kilpnäärme kahjustus, on teatatud hüpotüreoidismi kliinilistest juhtudest (vt lõik 4.5). Sellistel patsientidel tuleb hoolikalt jälgida kilpnääret stimuleeriva hormooni (TSH) taset. Hepatotoksilisus Gliveci metabolism toimub peamiselt maksas ja ainult 13% eritub neerude kaudu. Maksafunktsiooni häirega (kerge, mõõdukas või raske) patsientidel tuleb hoolikalt jälgida perifeerse vere analüüse ja maksaensüüme (vt lõigud 4.2, 4.8 ja 5.2). ). On leitud, et GIST -ga patsientidel võivad olla maksametastaasid, mis võivad põhjustada maksakahjustusi. Imatiniibi kasutamisel on täheldatud maksakahjustusi, sealhulgas maksapuudulikkust ja maksanekroosi. Kui imatiniibi kombineeritakse suurte annustega keemiaraviga, on teatatud raskete maksareaktsioonide sagenemisest. Maksafunktsiooni tuleb hoolikalt jälgida olukordades, kus imatiniibi kombineeritakse keemiaraviga, mis on samuti teadaolevalt seotud maksapuudulikkusega (vt lõigud 4.5 ja 4.8). Vedelikupeetus Gliveciga ravitud ligikaudu 2,5% -l KML -i patsientidest on teatatud raske vedelikupeetuse juhtudest (pleuraefusioon, turse, kopsuturse, astsiit, pindmine turse). Seetõttu on tungivalt soovitatav patsiente regulaarselt kaaluda. Ootamatult kiiret kehakaalu tõusu tuleks hoolikalt uurida ning vajaduse korral rakendada asjakohast toetavat ravi ja ravimeetmeid. Kliinilistes uuringutes on nende nähtude esinemissagedus eakatel inimestel ja neil, kellel on varem esinenud südamehaigusi, seetõttu tuleb südamepuudulikkusega patsientidel olla ettevaatlik. Südamehaigusega patsiendid Südamehaigusi, südamepuudulikkuse riskitegureid või neerupuudulikkusega patsiente tuleb hoolikalt jälgida ning kõiki südame- või neerupuudulikkusega seotud nähtude või sümptomitega patsiente tuleb hinnata ja ravida. Hüpereosinofiilse sündroomiga (HES) patsientidel, kellel on müokardis varjatud infiltratsioon HES -rakkudesse, on varsti pärast imatiniibravi alustamist seostatud üksikuid kardiogeense šoki / vasaku vatsakese düsfunktsiooni juhtumeid HES -rakkude degranulatsiooniga. On teatatud, et seisund on pöörduv steroidide süsteemse manustamise, hemodünaamiliste toetusmeetmete ja imatiniibi ajutise katkestamise korral. Kuna imatiniibi kasutamisel on aeg -ajalt teatatud südamega seotud kõrvalnähtudest, tuleb enne ravi alustamist hoolikalt kaaluda imatiniibravi kasu ja riski suhet HES / CEL patsientide populatsioonis. Müelodüsplastilised / müeloproliferatiivsed haigused koos PDGFR geeni ümberkorraldustega võivad olla seotud kõrgenenud eosinofiilide tasemega. Seetõttu tuleb HES / CEL -ga patsientidel ja MDS / MPD -ga patsientidel, kes on seotud eosinofiilide taseme tõusuga, enne imatiniibi manustamist kaaluda kardioloogi hindamist, ehhokardiogrammi tegemist ja seerumi troponiini määramist. Üks neist kahest on väljas normist, tuleb ravi alguses kaaluda kardioloogi perioodilist kontrolli ja süsteemsete steroidide (1-2 mg / kg) profülaktilist kasutamist ühe kuni kahe nädala jooksul samaaegselt ravi alustamisega. Seedetrakti verejooks Uuringus, kus osalesid patsiendid, kellel oli eemaldatav ja / või metastaatiline GIST, teatati nii seedetrakti kui ka kasvajasisestest verejooksudest (vt lõik 4.8). Olemasolevate andmete põhjal ei ole tuvastatud eelsoodumust põhjustavaid tegureid (nt kasvaja suurus, kasvaja asukoht, hüübimishäired), mis seaksid GIST -ga patsiendid mõlema verejooksu tüübi puhul suurema riskiga. Kuna suurenenud vaskulaarsus ja verejooksu kalduvus on osa GIST -ide olemusest ja kliinilisest käigust, tuleks kõigi patsientide puhul rakendada ühiseid meditsiinilisi tavasid ja protseduure verejooksu jälgimiseks ja raviks. Kasvaja lüüsi sündroom Kasvaja lüüsi sündroomi (TLS) võimaliku esinemise tõttu soovitatakse enne Glivec -ravi alustamist korrigeerida kliiniliselt olulist dehüdratsiooni ja kõrge kusihappe sisalduse ravi (vt lõik 4.8). Laboratoorne analüüs Glivec -ravi ajal tehke regulaarselt täielik vereanalüüs. KML -i patsientide ravi Gliveciga on seostatud neutropeenia või trombotsütopeeniaga. Siiski on nende tsütopeeniate esinemine tõenäoliselt seotud ravitava haiguse staadiumiga ja esines sagedamini CML -i kiirendatud faasi või blastsete kriisiga patsientidel kui kroonilise faasi KML -iga patsientidel. Ravi Gliveciga võib lõpetada või annust vähendada, nagu on soovitatud lõigus 4.2. Glivec -ravi saavatel patsientidel tuleb regulaarselt jälgida maksafunktsiooni (transaminaas, bilirubiin, leeliseline fosfataas). Neerufunktsiooni kahjustusega patsientidel näib imatiniibi plasmakontsentratsioon olevat kõrgem kui normaalse neerufunktsiooniga patsientidel, mis võib olla tingitud imatiniibiga seonduva valgu alfahappe glükoproteiini (AGP) plasmakontsentratsiooni tõusust. Neerukahjustusega patsientidele tuleb anda väikseim algannus. Raske neerukahjustusega patsiente tuleb ravida ettevaatusega. Kui ravimit ei talu, võib annust vähendada (vt lõigud 4.2 ja 5.2). Lapsed Imatiniibiga ravitud lastel ja noorukitel on teatatud kasvupeetuse juhtudest. Imatiniibi pikaajalise ravi pikaajaline mõju laste kasvule ei ole teada. Seetõttu soovitatakse imatiniibi saavatel lastel hoolikalt jälgida nende kasvu (vt lõik 4.8). Toimeained, mis võivad suurendada imatiniibi plasmakontsentratsiooni: Ained, mis pärsivad tsütokroom P450 isoensüümi CYP3A4 aktiivsust (nt proteaasi inhibiitorid nagu indinaviir, lopinaviir / ritonaviir, ritonaviir, sakvinaviir, telapreviir, nelfinaviir, bocepreviir; asoolsed seenevastased ained, sh ketokonasool, itolidrakonasool, mõned makrikonakroloon, mõned (klaritromütsiin ja telitromütsiin) võivad vähendada metabolismi ja suurendada imatiniibi kontsentratsiooni. Imatiniibi ekspositsioon suurenes märkimisväärselt (imatiniibi keskmine Cmax ja AUC suurenes vastavalt 26% ja 40%), kui seda manustati koos ketokonasooli (CYP3A4 inhibiitor) ühekordse annusega. Gliveci manustamisel koos CYP3A4 inhibiitorite rühma tuleb olla ettevaatlik. Toimeained, mis võivad vähendada imatiniibi plasmakontsentratsiooni: Ained, mis stimuleerivad CYP3A4 aktiivsust (nt deksametasoon, fenütoiin, karbamasepiin, rifampitsiin, fenobarbitaal, fosfenütoiin, primidoon võiHypericum perforatum(tuntud ka kui naistepuna) võib oluliselt vähendada Gliveci ekspositsiooni, suurendades potentsiaalselt ravi ebaõnnestumise riski. Eeltöötlus 600 mg rifampitsiini korduvate annustega, millele järgnes ühekordne Gliveci 400 mg annus, vähendas Cmax ja AUC (0-∞) vähemalt 54% ja 74% võrreldes nende väärtustega ilma rifampitsiinita. Sarnaseid tulemusi täheldati Gliveciga ravitud pahaloomuliste glioomidega patsientidel, kes võtsid ensüüme indutseerivaid epilepsiavastaseid ravimeid (EIAED), nagu karbamasepiin, okskarbasepiin Imatiniibi plasma AUC vähenes 73% võrreldes patsientidega, keda ei ravitud EIAED -ga. Rifampitsiini või tugevate CYP3A4 indutseerijate ja imatiniibi samaaegset kasutamist tuleb vältida. Toimeained, mille plasmakontsentratsiooni Glivec võib muuta Imatiniib suurendab simvastatiini (CYP3A4 substraat) keskmisi Cmax ja AUC väärtusi vastavalt 2- ja 3,5-kordselt, mis näitab "CYP3A4 inhibeerimist imatiniibi poolt. Seetõttu on Gliveci manustamisel koos CYP3A4 substraatidega, millel on terapeutiline aken, ettevaatlik ( nt tsüklosporiin, pimosiid, takroliimus, siroliimus, ergotamiin, diergotamiin, fentanüül, alfentaniil, terfenadiin, bortesomiib, dotsetakseel ja kinidiin). Glivec võib suurendada teiste CYP3A4 vahendusel metaboliseeritavate ravimite (nt bensidodiasool-triasool) plasmakontsentratsiooni, mõned HMG-CoA reduktaasi inhibiitorid, nt statiinid jne). Kuna imatiniibi kasutamisel on teadaolevalt suurenenud verejooksu oht (nt hemorraagia), peaksid antikoagulante vajavad patsiendid saama kumariini derivaatide, näiteks varfariini asemel tavalist või madala molekulmassiga hepariini. In vitro Glivec pärsib tsütokroom P450 isoensüümi CYP2D6 aktiivsust kontsentratsioonides, mis on sarnased CYP3A4 aktiivsust mõjutavate kontsentratsioonidega. Imatiniib 400 mg kaks korda ööpäevas pärssis metoprolooli CYP2D6 vahendatud metabolismi, suurendades AUC Cmaxe ligikaudu 23% (90 % CI [1,16-1,30]). Imatiniibi manustamisel koos CYP2D6 substraatidega ei tundu annuse kohandamine olevat vajalik, kuid kitsa terapeutilise aknaga CYP2D6 substraatide, näiteks metoprolooli puhul tuleb olla ettevaatlik. Metoprolooliga ravitavatel patsientidel tuleb kaaluda kliinilist jälgimist. In vitroGlivec pärsib paratsetamooli O-glükuronisatsiooni Ki väärtusega 58,5 mikromooli / l. Seda pärssimist ei täheldatud in vivo pärast 400 mg Gliveci ja 1000 mg paratsetamooli manustamist. Gliveci ja paratsetamooli suuremaid annuseid ei ole uuritud. Seetõttu tuleb Gliveci ja paratsetamooli suurte annuste samaaegsel kasutamisel olla ettevaatlik. Kilpnäärme kahjustusega patsientidel, kes saavad levotüroksiini, võib levotüroksiini plasmakontsentratsioon väheneda, kui seda manustatakse koos Gliveciga (vt lõik 4.4). Seetõttu on soovitatav olla ettevaatlik. Täheldatud koostoime mehhanism on siiski teadmata. Gliveci manustamisel koos kemoteraapiaga on kliiniline kogemus Ph + ALL -ga patsientidel (vt lõik 5.1), kuid ravimite koostoimeid imatiniibi ja keemiaravi vahel ei ole täielikult iseloomustatud. Imatiniibi kõrvaltoimed, nagu hepatotoksilisus, müelosupressioon või teised, võivad suureneda ning on teatatud, et samaaegne kasutamine L-asparaginaasiga võib olla seotud hepatotoksilisuse suurenemisega (vt lõik 4.8). Seetõttu nõuab Glivec'i kombineeritud kasutamine erilisi ettevaatusabinõusid. Fertiilses eas naised Fertiilses eas naisi tuleb teavitada vajadusest kasutada ravi ajal tõhusaid rasestumisvastaseid vahendeid. Rasedus Imatiniibi kasutamise kohta rasedatel on vähe andmeid. Loomkatsed on siiski näidanud reproduktiivtoksilisust (vt lõik 5.3) ja võimalikku ohtu lootele ei ole teada. Gliveci ei tohi raseduse ajal kasutada. Kui see pole absoluutselt vajalik teavitage patsienti võimalikust ohust lootele. Toitmisaeg Teave imatiniibi jaotumise kohta rinnapiima on piiratud. Kahe imetava naise hinnangud näitasid, et nii imatiniib kui ka selle aktiivne metaboliit võivad imenduda rinnapiima. Piima / plasma suhe, mida hinnati ühel patsiendil, oli imatiniibi puhul 0,5 ja metaboliidi puhul 0,9, mis viitab metaboliidi suuremale jaotumisele piimas. Võttes arvesse imatiniibi ja metaboliidi kombineeritud kontsentratsiooni ning imikute maksimaalset päevast piimatarbimist, näib kogu ekspositsioon olevat väike (ligikaudu 10% raviannusest). teadmata, imatiniibi võtvad naised ei tohi last rinnaga toita. Viljakus Mittekliinilistes uuringutes ei mõjutatud isaste ja emaste rottide viljakust (vt lõik 5.3). Gliveciga ravitud patsientidel ei ole uuringuid selle mõju kohta viljakusele ja spermatogeneesile läbi viidud. Patsiendid, kes on Glivec -ravi ajal oma viljakuse pärast mures, peaksid nõu pidama oma arstiga. Patsiente tuleb teavitada, et imatiniibravi ajal võivad tekkida sellised kõrvaltoimed nagu pearinglus, nägemise hägustumine või unisus. Seetõttu on soovitatav autojuhtimisel ja masinate käsitsemisel olla ettevaatlik. Kaugelearenenud vähiga patsientidel võib olla mitmeid ebaselgeid kliinilisi seisundeid, mis raskendavad kõrvaltoimete põhjuste hindamist, arvestades põhihaigusega seotud sümptomite mitmekesisust, selle progresseerumist ja paljude ravimite samaaegset manustamist. KML-i kliinilistes uuringutes täheldati ravimiga seotud kõrvaltoimete tõttu ravimi ärajätmist 2,4% -l äsja diagnoositud patsientidest, 4% -l kaugelearenenud kroonilise faasi patsientidest pärast interferoonravi ebaõnnestumist, 4% -l kaugelearenenud kroonilises faasis. Kiirenenud faasi patsientidel pärast interferoonravi ebaõnnestumist ja 5% -l blastakriisiga patsientidest pärast interferoonravi ebaõnnestumist. GIST-uuringutes katkestati ravimi manustamine 4% -l patsientidest ravimiga seotud kõrvaltoimete tõttu. Kõrvaltoimed olid kõigi näidustuste korral sarnased, välja arvatud kaks erandit. KML -i patsientidel täheldati rohkem müelosupressiooni kui GIST -patsientidel, mis on tõenäoliselt tingitud põhihaigusest. Uuringus, kus osalesid patsiendid, kellel ei olnud eemaldatavat ja / või metastaatilist GIST-i, esines 7 patsiendil (5%) CTC astme 3/4 GI verejooks (3 patsienti), kasvajasisene verejooks (3 patsienti) või mõlemad (1 patsient). GI verejooksu põhjuseks võis olla seedetrakti kasvajate asukoht (vt lõik 4.4). Seedetrakti verejooks ja kasvajaverejooks võivad olla tõsised ja mõnikord surmavad. Kõige sagedasemad (≥10%) ravimiga seotud kõrvaltoimed, millest teatati mõlema häire korral, olid kerge iiveldus, oksendamine, kõhulahtisus, kõhuvalu, väsimus, müalgia, lihaskrambid ja lööve. Kõigis uuringutes leiti tavaliselt pindmist turset, mida kirjeldati peamiselt kui periorbitaalset või alajäsemete turset. Kuid need tursed olid harva rasked ja neid saab ravida diureetikumide, muude toetavate meetmete või Gliveci annuse vähendamisega. Kui imatiniibi kombineeriti Ph + ALL-ga patsientidel suure annusega keemiaraviga, täheldati mööduvat maksatoksilisust, mis on seotud suurenenud transaminaaside ja hüperbilirubineemiaga. Arvestades piiratud ohutusalast teavet, on lastel seni teatatud kõrvaltoimed kooskõlas Ph + ALL täiskasvanud patsientide ohutusprofiiliga. Ph + ALL -ga laste ohutusalane teave on väga piiratud, kuid uusi ohutusprobleeme pole tuvastatud. Erinevaid kõrvaltoimeid, nagu pleuraefusioon, astsiit, kopsuturse ja kiire kaalutõus koos pindmise tursega või ilma, võib ühiselt kirjeldada kui "vedelikupeetust". Neid reaktsioone saab tavaliselt hallata, kui Gliveci ja diureetikumide ning muude sobivate toetavate ravimeetmete kasutamise ajutiselt ära jätta. Mõned neist reaktsioonidest võivad siiski olla tõsised või eluohtlikud ning mitmed plahvatuskriisiga patsiendid on surnud, kellel on pleuraefusiooni, kongestiivse südamepuudulikkuse ja neerupuudulikkuse keeruline kliiniline pilt. Lastega läbi viidud kliinilistest uuringutest ei ilmnenud mingeid erilisi ohutusaspekte. Kõrvaltoimed Kõrvaltoimed, millest on teatatud rohkem kui ühe üksikjuhuna, on loetletud allpool organsüsteemi klassi ja esinemissageduse järgi. Esinemissageduse kategooriad on määratletud järgmiselt: väga sage (≥1 / 10), sage (≥1 / 100, Igas esinemissageduse klassis on kõrvaltoimed loetletud esinemissageduse järjekorras, kõige sagedamini esimesena. Tabelis 1 esitatud kõrvaltoimed ja nende esinemissagedused põhinevad peamistel kesksetel uuringutel. Tabel 1 Kõrvaltoimed kliinilistes uuringutes 1 Pneumooniat teatati kõige sagedamini kaugelearenenud KML -iga ja GIST -ga patsientidel. 2 Peavalu esines sagedamini GIST -ga patsientidel. 3 Patsiendiaastate kaupa täheldati südamehaigusi, sealhulgas südame paispuudulikkust, kaugelearenenud KML-iga patsientidel sagedamini kui kroonilise KML-iga patsientidel. 4 Punetus oli sagedasem GIST-ga patsientidel ja verejooks (hematoom, hemorraagia) oli sagedasem GIST-i ja kaugelearenenud KML (AP-CML ja CMLBC) patsientidel. 5 Pleuraefusiooni esines sagedamini GIST-ga patsientidel ja kaugelearenenud CML-iga (CML-AP ja CML-BC) patsientidel kui kroonilise KML-iga patsientidel. 6 + 7 Kõhuvalu ja seedetrakti verejooksu täheldati kõige sagedamini GIST -ga patsientidel. 8 On teatatud mõnest surmaga lõppenud maksapuudulikkuse ja maksanekroosi juhtumist. 9 Lihas -skeleti valu ja sellega seotud sündmusi täheldati sagedamini KML -i patsientidel kui GIST -ga patsientidel. Gliveci turustamisjärgsest kogemusest on peamiselt teatatud järgmist tüüpi reaktsioonidest. Need hõlmavad spontaanseid teateid ja tõsiseid kõrvaltoimeid, mis on teatatud käimasolevatest uuringutest, laiendatud juurdepääsuprogrammidest, kliinilise farmakoloogia uuringutest ja kinnitamata näidustuste uuringutest. tundmatu suurusega, ei ole alati võimalik usaldusväärselt hinnata nende esinemissagedust ega tuvastada põhjuslikku seost imatiniibi ekspositsiooniga. Tabel 2 Turustamisjärgsete aruannete kõrvaltoimed 1 Surmavaid juhtumeid on teatatud kaugelearenenud haiguse, raskete infektsioonide, raske neutropeenia ja muude tõsiste kaasuvate seisunditega patsientidel. Laboratoorsete analüüside kõrvalekalded: Hematoloogia KML -i korral olid tsütopeeniad, eriti neutropeenia ja trombotsütopeenia, kõikides uuringutes tavalised, mis näitab suuremat esinemissagedust suurtes annustes ≥750 mg (I faasi uuring). Siiski leiti, et tsütopeenia esinemine sõltub selgelt ka staadiumist. haigus, neutropeenia sagedus (ANC) Äsja diagnoositud kroonilise faasi KML -i korral neutropeenia (ANC) Kuid harvadel juhtudel võivad need põhjustada ravi püsiva peatamise. KML -iga lastel olid kõige sagedamini täheldatud toksilisused 3. või 4. astme tsütopeeniad, sealhulgas neutropeenia, trombotsütopeenia ja aneemia. Need tekkisid tavaliselt ravi esimestel kuudel. Uuringus, kus osalesid patsiendid, kellel oli eemaldatav ja / või metastaatiline GIST, teatati 3. ja 4. astme aneemiast vastavalt 5,4% ja 0,7% patsientidest, mis vähemalt mõnedel neist patsientidest võivad olla seotud seedetrakti või kasvajasisese verejooksuga. 3. ja 4. astme neutropeeniat täheldati vastavalt 7,5% -l ja 2,7% -l patsientidest ning 3. astme trombotsütopeeniat 0,7% -l patsientidest. Ühelgi patsiendil ei tekkinud 4. astme trombotsütopeeniat. Leukotsüüdid (leukotsüüdid) ja neutrofiilide arv esinesid enamasti esimese kuue nädala jooksul. ravi, kusjuures väärtused jäävad pärast seda suhteliselt stabiilseks. Biokeemia KML patsientidel täheldati 3. või 4. astme transaminaaside (alaniinaminotransferaasi) ja 3. või 4. astme aspartaataminotransferaasi (AST) taseme tõusu 4,8%. On esinenud tsütolüütilise ja kolestaatilise hepatiidi ja maksapuudulikkuse juhtumeid; Mõnel juhul oli tulemus surmav, sealhulgas üks patsient, keda raviti paratsetamooli suurte annustega. Arvatavatest kõrvaltoimetest teatamine Pärast ravimi müügiloa väljastamist tekkinud arvatavatest kõrvaltoimetest teatamine on oluline, kuna see võimaldab pidevalt jälgida ravimi kasu ja riski suhet. Tervishoiutöötajatel palutakse teavitada kõigist võimalikest kõrvaltoimetest riikliku teavitussüsteemi kaudu. Soovitatud terapeutilisest annusest suuremate annuste kasutamise kogemus on piiratud. Gliveci üleannustamise üksikjuhtudest on teatatud spontaanselt ja kirjanduses. Üleannustamise korral tuleb patsienti jälgida ja talle sobivat sümptomaatilist ravi anda. Tavaliselt on nende juhtumeid on "parandatud" või "parandatud". Erinevate annuste intervallidega on teatatud järgmistest sündmustest: Täiskasvanud elanikkond 1200-1600 mg (ravi kestus 1 kuni 10 päeva): iiveldus, oksendamine, kõhulahtisus, lööve, erüteem, turse, turse, väsimus, lihasspasmid, trombotsütopeenia, pantsütopeenia, kõhuvalu, peavalu, söögiisu vähenemine. 1800-3200 mg (kuni 3200 mg päevas 6 päeva jooksul): nõrkus, müalgia, suurenenud kreatiinfosfokinaas, suurenenud bilirubiin, seedetrakti valu. 6400 mg (ühekordne annus): kirjanduses teatati juhtumist patsiendist, kellel esines iiveldus, oksendamine, kõhuvalu, palavik, näoturse, vähenenud neutrofiilide arv, suurenenud transaminaaside sisaldus. 8-10 g (ühekordne annus): on teatatud oksendamisest ja seedetrakti valust. Lapsed Ühel 3-aastasel lapsel, kellele manustati ühekordne 400 mg annus, oli oksendamine, kõhulahtisus ja anoreksia ning teisel 3-aastasel lapsel, kellele manustati ühekordne annus 980 mg, vähenes valgete vereliblede arv ja tekkis kõhulahtisus. Üleannustamise korral tuleb patsienti jälgida ja talle määrata sobiv toetav ravi. Farmakoterapeutiline rühm: valgu türosiinkinaasi inhibiitor, ATC -kood: L01XE01 Toimemehhanism Imatiniib on väike valk-türosiinkinaasi inhibiitormolekul, mis pärsib tugevalt Bcr-Abl türosiinkinaasi ja mitmete türosiinkinaasi retseptorite aktiivsust: komplekt, proto-onkogeeni c-Kit , diskoidiini domeeni retseptorid (DDR1 ja DDR2), kolooniat stimuleeriva faktori retseptor (CSF-1R) ning trombotsüütidest pärineva kasvufaktori (PDGFR-alfa ja PDGFR-beeta) alfa- ja beeta-retseptorid. Imatiniib võib samuti pärssida nende kinaasi retseptorite aktiveerimise vahendatud rakulisi sündmusi. Farmakodünaamilised toimed Imatiniib on valgu-türosiinkinaasi inhibiitor, mis pärsib tugevalt Bcr-Abl türosiinkinaasi taset in vitro, rakutasandil e in vivo. Ühend inhibeerib selektiivselt proliferatsiooni ja indutseerib apoptoosi Bcr-Abl-positiivsetes rakuliinides ja Philadelphia kromosoompositiivse KML-i ja ägeda lümfoblastilise leukeemia (ALL) patsientide värsketes leukeemiarakkudes. In vivo ühendil on kasvajavastane toime ainsa ainena loommudelites koos Bcr-Abl-positiivsete kasvajarakkudega. Imatiniib on ka türosiinkinaasi retseptori inhibiitor trombotsüütidest pärineva kasvufaktori (PDGF), PDGF-R ja tüvirakufaktori (SCF), c-Kit jaoks ning pärsib PDGF ja SCF vahendatud rakulisi sündmusi. In vitroimatiniib pärsib proliferatsiooni ja indutseerib apoptoosi seedetrakti strooma kasvaja (GIST) rakkudes, mis ekspresseerivad aktiivset mutatsiooni komplekt. MDS / MPD, HES / CLE ja DFSP patogeneesis on kaasatud PDGF retseptori või Abl valgu türosiinkinaasi konstitutiivne aktiveerimine erinevate partnervalkude sulandumise või PDGF konstitutiivse tootmise tagajärjel. Imatiniib pärsib signaaliülekannet ja rakkude proliferatsiooni. PDGFR dereguleerimise ja Abl kinaasi aktiivsuse järgi. Kroonilise müeloidse leukeemia kliinilised uuringud Gliveci efektiivsus põhineb hematoloogilise ja tsütogeneetilise ravivastuse ning haiguse progresseerumisvaba elulemuse üldväärtustel. Välja arvatud äsja diagnoositud kroonilise faasi KML, puuduvad kontrollitud kliinilised uuringud, mis näitaksid kliinilist kasu, mis tähendab haigusega seotud sümptomid või suurenenud elulemus. Philadelphia kromosoompositiivse (Ph +) KML-iga patsientidel, kellel on kaugelearenenud, kiirendatud või plahvatuskriisihaigus, on läbi viidud kolm suurt avatud, kontrollimata II faasi rahvusvahelist uuringut. muud Ph + leukeemiad või krooniline faasi KML, kuid mis ei saanud kasu eelmisest interferoon-alfa (IFN) ravist.Suur, randomiseeritud, avatud, III faasi rahvusvaheline uuring viidi läbi Ph + CML-iga patsientidega. Lisaks raviti pediaatrilisi patsiente kahes I ja ühes II faasi uuringus. Kõigis kliinilistes uuringutes olid 38–40% patsientidest ≥ 60-aastased ja 10–12% patsientidest ≥ 70-aastased. Krooniline faas, uus diagnoos: Selles III faasi uuringus täiskasvanud patsientidel võrreldi ravi ainult Gliveciga ja alfa-interferooni (IFN) ja tsütarabiini (Ara-C) kombinatsiooniga. Patsiendid, kes ei reageerinud (täielik hematoloogiline vastus (REC) 6 kuu pärast, valgete vereliblede arvu suurenemine, suur tsütogeneetiline vastus (MCR) 24 kuu pärast), kellel tekkis ravivastus (kadus REC ja MCR) või raske ravi talumatus, lubati üle minna alternatiivsele ravile. Gliveci rühmas raviti patsiente 400 mg ööpäevaste annustega. IFN rühmas manustati patsiente subkutaanselt IFN annustega 5 MIU / m2 / päevas kombinatsioonis Ara-C-ga annuses 20 mg / m2 / päevas 10 päeva kuus. Kokku randomiseeriti 1106 patsienti, 553 kummagi käe kohta. Kahe rühma algtaseme omadused olid sarnased. Keskmine vanus oli 51 aastat (vahemikus 18–70 aastat), 21,9% ≥60-aastastest patsientidest. 59% olid mehed ja 41% naised; 89,9% olid kaukaasia ja 4,7% mustanahalised. Seitse aastat pärast viimase patsiendi registreerimist oli esmavaliku ravi keskmine kestus vastavalt 82 ja 8 kuud Gliveci ja IFN rühmas. Teise rea Glivec-ravi keskmine kestus oli 64 kuud. Üldiselt oli Gliveci esmavaliku ravi saanud patsientidel keskmine manustatud ööpäevane annus 406 ± 76 mg. Uuringu peamine efektiivsuse tulemusnäitaja on progresseerumisvaba elulemus. Progressiooni määratleti järgmiselt: progresseerumine kiirendatud faasi või plahvatuskriisi, surm, täieliku hematoloogilise vastuse (REC) kadumine või suur tsütogeneetiline vastus (MCR) või patsientidel, kes ei saavuta REC -d, valgete vereliblede arvu suurenemine vaatamata asjakohasele terapeutilisele juhtimisele. Peamised sekundaarsed tulemusnäitajad on suur tsütogeneetiline vastus, hematoloogiline vastus, molekulaarne ravivastus (haiguse hindamise jääkmiinimum), aeg kiirendatud faasi ja plahvatuskriis ja ellujäämine Tulemused on toodud tabelis 3. Tabel 3. Vastus äsja diagnoositud KML uuringus (84 kuu andmed) * lk ** Molekulaarse ravivastuse määrad põhinevad saadaolevatel proovidel Hematoloogilise ravivastuse kriteeriumid (kõik vastused tuleb kinnitada vähemalt 4 nädala pärast): WBC Tsütogeneetilise ravivastuse kriteeriumid: täielik (0%Ph + metafaasid), osaline (1–35%), väike (36–65%) või minimaalne (66–95%). Peamine vastus (0–35%) ühendab nii täielikud kui ka osalised vastused. Peamised molekulaarse ravivastuse kriteeriumid: perifeerses veres Bcr-Abl transkripti vähenemine ≥ 3 log (vähenenud kvantitatiivse pöördtranskriptaasi RT-PCR abil) võrreldes standardse algtasemega. Täieliku hematoloogilise ravivastuse, peamise tsütogeneetilise vastuse ja täieliku tsütogeneetilise ravivastuse määrad esmavaliku ravis arvutati vastavalt Kaplan-Meieri meetodile, kusjuures ravivastused kärbiti viimase hindamise kuupäeval. Selle meetodi puhul kumulatiivne ravivastus esmavaliku Glivec-ravi korral olid näitajad paremad 12 kuult 84 kuule järgmiselt: CHR vastavalt 96,4% -lt 98,4% -ni ja CCyR vastavalt 69-lt, 5% -lt 87,2% -ni. Pärast 7-aastast jälgimist oli Gliveci rühmas 93 (16,8%) progresseerumist: 37 (6,7%) kiirendatud faasi progresseerumine / plahvatuskriis, 31 (5,6%) MCyR-i kaotus, 15 (2,7%) CHR-i kaotus või valgete vereliblede arvu suurenemine ja 10 juhtumit (1,8%) mitte-KML-iga seotud surma korral. IFN + Ara-C ravis esines 165 juhtumit (29,8%), millest 130 esines esmavaliku IFN-ravi ajal + Ara-C. Prognoosivabade patsientide hinnanguline määr kiirendatud faasi või plahvatuskriisi tekkimisel 84 kuu pärast oli Gliveci rühmas oluliselt suurem kui IFN rühmas (92,5% vs 85,1%, p Gliveci ja IFN + Ara-C rühmas oli vastavalt 71 (12,8%) ja 85 (15,4%) surmajuhtumit. Hinnanguline üldine elulemus 84 kuu jooksul on Gliveci randomiseerimisrühmas 86,4% ja IFN + Ara-C rühmas 83,3% (log-rank test p = 0,073). "Sündmuseni jõudmise aeg" lõpp-punkti mõjutab suuresti "IFN + Ara-C haru ja Gliveci haru ülemineku suur protsent. Glivec-ravi mõju ellujäämisele äsja diagnoositud kroonilise faasi KML-is hinnati täiendavalt "ülaltoodud Gliveci andmete ja teise III faasi uuringu esmaste andmete tagasiulatuv analüüs, kasutades IFN + Ara-C (n = 325) sama annustamisskeemiga. Gliveci tagasiulatuv analüüs näitas IFN + Ara -C üldise ellujäämise osas (lk Tsütogeneetilise ja molekulaarse ravivastuse määr avaldas Gliveci kasutavate patsientide pikaajalistele tulemustele ilmset mõju. Kui hinnanguliselt 96% (93%) patsientidest, kellel oli 12 kuu pärast CCyR (PCyR), oli 84 kuu jooksul progresseerumiseta kuni kiirendatud faasi / plahvatuskriis, siis ainult 81% patsientidest, kellel ei olnud 12 kuu möödudes MCyR-i, oli KML progresseerumisvaba kaugelearenenud etapp 84 kuuga (ülemaailmne lk Selles uuringus suurendati lubatud annust 400 mg -lt 600 mg -ni päevas, seejärel 600 mg -lt 800 mg -le päevas. Pärast 42-kuulist jälgimist tekkis 11 patsiendil tsütogeneetilise ravivastuse kaotus (üle 4 nädala). Nendest 11 patsiendist suurendas 4 patsienti annust kuni 800 mg ööpäevas, neist 2 taastus tsütogeneetiline reaktsioon (1 osaline ja 1 täielik, viimane saavutas ka molekulaarse vastuse), samas kui 7 patsiendil ei olnud annust suurendanud, ainult üks oli taastanud täieliku tsütogeneetilise vastuse. Mõnede kõrvaltoimete esinemissagedus oli suurem 40 patsiendil, kelle ööpäevast annust suurendati 800 mg -ni võrreldes patsientide populatsiooniga enne annuse suurendamist (n = 551). Kõige sagedasemad kõrvaltoimed olid seedetrakti verejooks, konjunktiviit ja transaminaasid või bilirubiin Teisi kõrvaltoimeid on kirjeldatud sama või väiksema sagedusega. Krooniline faas, interferoonravi ebaõnnestumine: 532 täiskasvanud patsienti raviti algannusega 400 mg. Patsiendid jagati kolme põhikategooriasse: hematoloogiline puudulikkus (29%), tsütogeneetiline puudulikkus (35%) või interferoonitalumatus (36%). Patsiendid olid varem saanud IFN -ravi keskmiselt 14 kuud annustes ≥ 25 x 106 RÜ nädalas ja kõik olid kroonilises kaugelearenenud faasis, keskmine aeg diagnoosimisest oli 32 kuud. Uuringu esmane efektiivsuse muutuja oli peamise tsütogeneetilise ravivastuse määr (täielik pluss osaline ravivastus, Ph + metafaasid luus 0 ... 35% luuüdi). Selles uuringus saavutas 65% patsientidest peamise tsütogeneetilise ravivastuse, mis oli täielik 53% patsientidest (kinnitatud 43% -l) (tabel 4). Täielik hematoloogiline vastus saavutati 95% patsientidest. Kiirendatud faasUuringusse kaasati 235 kiirendatud faasi haigusega täiskasvanud patsienti. Esimesed 77 patsienti alustasid ravi 400 mg -ga, hiljem kohandati protokolli, et võimaldada suuremaid annuseid, ja ülejäänud 158 patsienti alustasid ravi 600 mg -ga. Esmane efektiivsuse muutuja oli hematoloogilise ravivastuse määr, millest teatati täieliku hematoloogilise ravivastusena, leukeemia puudumine (st blastide eemaldamine luuüdist ja verest, kuid ilma perifeerse vere täieliku taastumiseta, nagu täieliku ravivastuse korral). Või kroonilise faasi KML -i juurde naasmine . Kinnitatud hematoloogiline vastus saavutati 71,5% patsientidest (tabel 4). Oluline on see, et asjakohane tsütogeneetiline vastus saavutati ka 27,7% -l patsientidest, mis oli täielik 20,4% -l patsientidest (kinnitatud 16% -l). Patsientidel, keda raviti annusega 600 mg, olid praegused progressioonivaba elulemuse mediaanid ja üldised elulemused vastavalt 22,9 ja 42,5 kuud. Müeloidne lööklaine: Registreeriti 260 müeloidse lööklainega patsienti. 95 (37%) olid varem saanud kiirendatud faasi haiguse või plahvatuskriisi raviks keemiaravi ("eeltöödeldud patsiendid"), samas kui 165 (63%) ei saanud ravi ("ravimata patsiendid"). Esimesed 37 patsienti alustasid ravi 400 mg -ga, hiljem kohandati protokolli, et võimaldada suuremaid annuseid, ja ülejäänud 223 patsienti alustasid ravi 600 mg -ga. Esmane efektiivsuse muutuja oli hematoloogilise ravivastuse määr, mis teatati täieliku hematoloogilise ravivastusena, leukeemia puudumine või kroonilise faasi KML -i taastumine, kasutades samu kriteeriume nagu kiirendatud faasi uuringus. Selles uuringus saavutas hematoloogilise ravivastuse 31% patsientidest (36% varem ravimata ja 22% varem ravitud patsientidest). Seetõttu oli ravivastuse määr 600 mg (33%) saanud patsientidel suurem kui 400 mg (16%, p = 0,0220). Varem ravimata ja ravitud patsientide keskmine elulemus oli vastavalt 7,7 ja 4,7 kuud. Lümfoidse lööklaine kriisI faasi uuringutes osales piiratud arv patsiente (n = 10). Hematoloogilise ravivastuse väärtus oli 70%, kestus 2-3 kuud. Tabel 4 Vastus täiskasvanute KML uuringutes Lapsed: Kokku 26 vanuses pediaatrilist patsienti Patsiente raviti Gliveci annustega 260 mg / m2 päevas (n = 5), 340 mg / m2 päevas (n = 9), 440 mg / m2 päevas (n = 7) ja 570 mg / m2 päevas. sureb (n = 5). Üheksa kroonilise faasi KML -iga patsiendi seas, kelle kohta olid olemas tsütogeneetilised andmed, saavutasid 4 (44%) ja 3 (33%) vastavalt täieliku ja osalise tsütogeneetilise ravivastuse, mille korral tsütogeneetilise ravivastuse (MCR) määr oli suurem kui 77%. Kokku osales 51 äsja diagnoositud, ravimata kroonilise faasi KML-iga lapspatsienti avatud, ühe käega, mitmekeskuselises II faasi uuringus. Patsiente raviti Gliveciga 340 mg / m2 / päevas, ilma katkestusteta annust piirava toksilisuse puudumisel. Äsja diagnoositud KML -iga lastel põhjustas Glivec -ravi kiire ravivastuse ja täieliku hematoloogilise ravivastuse (REC) 78% pärast 8 -nädalast ravi. Kõrge REC määr oli seotud täieliku tsütogeneetilise vastuse (CCyR) kujunemisega 65%, mis on võrreldav täiskasvanutel täheldatud tulemustega.Lisaks täheldati osalist tsütogeneetilist ravivastust (PCyR) 16% juhtudest, kui suur ravivastus (MCyR) oli 81%. Enamikul patsientidest, kes saavutasid täieliku tsütogeneetilise ravivastuse (CCyR), esines CCyR ajavahemikus 3. – kuu. 10, mille keskmine reageerimisaeg oli Kaplan-Meieri hinnangu põhjal 5,6 kuud. Euroopa Ravimiamet on loobunud kohustusest esitada Philadelphia kromosoompositiivse kroonilise müeloidse leukeemia (bcr-abl translokatsioon) kõigi laste alarühmade kohta Gliveciga tehtud uuringute tulemused (teave lastel kasutamise kohta vt lõik 4.2). Ph + ALL kliinilised uuringud Äsja diagnoositud Ph + ALL: Kontrollitud uuringus (ADE10) imatiniibi ja induktsioonkeemiaravi kohta 55 äsja diagnoositud 55 -aastastel ja vanematel patsientidel põhjustas imatiniib monoteraapiana oluliselt suurema täieliku hematoloogilise ravivastuse kui keemiaravi (96,3% vs 50%; p = Kui päästeravi imatiniibiga manustati patsientidele, kes ei reageerinud või ei reageerinud piisavalt kemoteraapiale, täheldati 9 patsienti (81,8%) 11-st, kes olid saavutanud täieliku hematoloogilise ravivastuse. See kliiniline toime oli seotud vererõhu suurema vähenemisega. abl-transkripti imatiniibiga ravitud patsientidel kui keemiaravi saanud patsientidel pärast 2-nädalast ravi (p = 0,02). Kõik patsiendid olid pärast induktsioonifaasi saanud imatiniibi ja konsolideerivat keemiaravi (vt tabel 5) ja bcr-abl 8 olid identsed mõlemas käes. Nagu uuringu ülesehituses ennustati, ei täheldatud erinevusi remissiooni kestuses, haigusvabas ellujäämises ega üldises elulemuses, kuigi täieliku molekulaarse ravivastusega ja minimaalse jääkhaigusega patsientidel oli tulemus parem nii mõlema kestuse osas. p = 0,01) ja haigusvaba elulemus (p = 0,02). Neljas kontrollimata kliinilises uuringus (AAU02, ADE04, AJP01 ja AUS01) 211 äsja diagnoositud Ph + ALL patsiendiga populatsioonis täheldatud tulemused on kooskõlas ülalkirjeldatud tulemustega. Imatiniib kombinatsioonis induktsioonkeemiaraviga (vt tabel 5) saavutas täieliku hematoloogilise ravivastuse määra 93% (147 -l 158 -st hinnatavast patsiendist) ja tsütogeneetilise ravivastuse määra üle 90% (19 -l 21 -st hinnatavast patsiendist). oli 48% (49-l 102-st hinnatavast patsiendist). Kahes uuringus (AJP01 ja AUS01) ületas haigusvaba elulemuse (DFS) ja üldise elulemuse (OS) järjepidevalt 1 aasta ja oli parem kui varasemad kontrollid (p DFS) Tabel 5 Keemiaravi skeemid, mida kasutatakse kombinatsioonis Gliveciga Pediaatrilised patsiendid: III faasi I2301, mitmekeskuselises, avatud, mitte-randomiseeritud, järjestikuses kohordiuuringus osales 93 lastel, noorukitel ja noortel täiskasvanutel Ph + ALL (vanuses 1 kuni 22 aastat) ja neid raviti Gliveciga ( 340 mg / m2 / päevas) kombinatsioonis intensiivse keemiaraviga pärast induktsioonravi. Glivec'i manustati perioodiliselt kohordides 1-5, pikendades Gliveci kestust ja alustades seda varem kohordist kohorti; kohord 1 sai Gliveci madalaima annuse intensiivsust ja kohort 5 sai suurima annuse intensiivsuse (pikim kestus Glivec -ravi päevade jooksul, mida manustati pidevalt iga päev keemiaravi esimestel kuuridel). Kohordis 5 (n = 50) patsientidel parandas Gliveci pidev igapäevane ekspositsioon ravikuuri alguses kombinatsioonis keemiaraviga 4-aastast sündmusteta elulemust (EFS) võrreldes varasemate kontrollidega (n = 120), kes olid saanud standardset keemiaravi ilma Glivec (vastavalt 69,6% versus 31,6%). Hinnanguline 4-aastane OS 5. rühmas oli 83,6% versus 44,8% ajaloolises kontrollis. 20 -st 50 -st patsiendist (40%) 5. kohordis tehti vereloome tüvirakkude siirdamine. Tabel 6 Keemiaravi skeemid, mida kasutati kombinatsioonis Gliveciga uuringus I2301 G-CSF = granulotsüütide kasvufaktor, VP-16 = etoposiid, MTX = metotreksaat, IV = intravenoosne, SC = subkutaanne, IT = intratekaalne, PO = suuline, IM = intramuskulaarne, ARA-C = tsütarabiin, CPM = tsüklofosfamiid, VCR = vinkristiin, DEX = deksametasoon, DAUN = daunorubitsiin, 6-MP = 6-merkaptopuriin, E.Coli L-ASP = L-asparaginaas, PEG-ASP = pegüleeritud asparaginaas, MESNA = naatrium-2-merkaptoetaanisulfonaat, iii = või rohkem, kui MTX tase on Uuring AIT07 oli II / III faasi mitmekeskuseline avatud randomiseeritud uuring, milles osales 128 patsienti (1 ... Ph + retsidiivne / tulekindel KÕIK: Kui imatiniibi kasutati monoteraapiana retsidiivse / refraktaarse Ph + ALL -ga patsientidel, oli hematoloogilise ravivastuse määr 30% (9% täielik) ja tsütogeneetilise ravivastuse määr 23% kõrgem 53 patsiendil. (Täpsemalt, 411 patsiendist raviti "laiendatud juurdepääsuprogrammi kontekstis, mis ei näinud ette andmete kogumist esmase ravivastuse kohta." Kogu 411 patsiendi populatsioonis, kellel oli retsidiivne / ravile allumatu Ph + ALL keskmine aeg progresseerumiseni oli 2,6 kuni 3,1 kuud ja 401 hinnataval patsiendil oli keskmine üldine elulemus vahemikus 4,9 kuni 9 kuud. Uuesti testides olid andmed sarnased ainult 55 -aastastele ja vanematele patsientidele. MDS / MPD kliinilised uuringud Gliveci kasutamise kogemus selles näidustuses on väga piiratud ning põhineb hematoloogilise ja tsütogeneetilise ravivastuse määradel. Puuduvad kontrollitud kliinilised uuringud, mis näitaksid kliinilist kasu või paremat elulemust. Avatud, mitmekeskuseline II faasi kliiniline uuring (uuring B2225) viidi läbi Gliveci hindamiseks erinevates patsientide populatsioonides, kellel on Abl, Kit või PDGFR valgu türosiinkinaasidega seotud riskid. Sellesse uuringusse kaasati 7 patsienti. MPD, keda oli ravitud Gliveciga 400 mg ööpäevas. Kolmel patsiendil oli täielik hematoloogiline vastus (CHR) ja ühel patsiendil oli hematoloogiline osaline ravivastus (PHR). Esialgse analüüsi ajal tuvastati kolmel neljast patsiendist PDGFR geeni ümberkorraldamisel oli neil tekkinud hematoloogiline vastus (2 CHR ja 1 PHR). Nende patsientide vanus oli vahemikus 20 kuni 72 aastat. Lisaks teatati 13 väljaandes veel 24 MDS / MPD -ga patsiendist. 21 patsienti raviti Gliveci 400 mg ööpäevasga, ülejäänud 3 patsienti aga väiksemate annustega. leiti üksteist PDGFR geeni ümberkorraldust, neist 9 olid saavutanud CHR ja 1 PHR. Nende patsientide vanus oli 2 kuni 79 aastat. Hiljutises väljaandes ilmnes ajakohastatud teabest 6 neist 11 patsiendist, et kõik patsiendid püsisid tsütogeneetilises remissioonis (vahemikus 32–38 kuud). Sama väljaanne teatas pikaajaliste jälgimisandmete kohta 12 patsiendilt (sealhulgas 5 patsiendilt uuringust B2225), kellel oli MDS / MPD koos PDGFR geeni ümberkorraldustega. Need patsiendid olid saanud Gliveci keskmiselt 47 kuud (vahemikus 24 päeva kuni 60 kuud). Nendest 6 patsiendist ületab jälgimine nüüd 4 aastat. Üksteist patsienti saavutasid kiiresti CHR-i, kümnel oli tsütogeneetiliste kõrvalekallete täielik taandumine ja RT-PCR-ga mõõdetud sulandunud transkriptide vähenemine või kadumine. Hematoloogilised ja tsütogeneetilised vastused püsisid vastavalt keskmiselt 49 kuud (vahemik 19–60) ja 47 kuud (vahemik 16–59). Üldine elulemus on diagnoosimisest 65 kuud (vahemik 25-234). Gliveci manustamine geneetilise translokatsioonita patsientidele üldiselt paranemist ei too. MDS / MPD -ga lastel ei ole kontrollitud uuringuid. Neljas väljaandes on teatatud viiest patsiendist, kellel on PDGFR geeni ümberkorraldamisega seotud MDS / MPD. Nende patsientide vanus oli 3 kuud kuni 4 aastat ja imatiniibi manustati annuses 50 mg ööpäevas või annustes 92,5 kuni 340 mg / m2 ööpäevas. Kõik patsiendid olid saavutanud täieliku hematoloogilise vastuse, tsütogeneetilise ravivastuse ja / või kliiniline vastus. HES / CLE kliinilised uuringud Avatud, mitmekeskuseline II faasi kliiniline uuring (uuring B2225) viidi läbi, et hinnata Gliveci erinevates patsientide populatsioonides, kellel on raske haigus, mis on seotud Abl, Kit või PDGFR valgu türosiinkinaasidega. Selles uuringus raviti 14 HES / CEL-ga patsienti Gliveci ööpäevased annused 100 mg kuni 1000 mg. Täiendavad 162 HES / CEL -ga patsienti, kellest teatati 35 juhtumite aruandes ja avaldatud juhtumite seerias, said Gliveci ööpäevastes annustes 75 mg kuni 800 mg. Neid tsütogeneetilisi kõrvalekaldeid hinnati 117 patsiendil 176 patsiendi kogu populatsioonist. 61 -st neist 117 -st patsiendist tuvastati fusioonkinaas FIP1L1 -PDGFRα. Veel 3 avaldatud dokumendis näitasid veel neli HES -iga patsienti FIP1L1 sulandkinaasi -PDGFRα positiivset tulemust. Kõik 65 patsienti, positiivsed FIP1L1-PDGFRα fusioonkinaas oli saavutanud CHR-i, mis oli säilinud kuid (vahemik 1+ kuni 44+ kuud lühendati aruande esitamise ajal). ja teatati hiljutises väljaandes, 21 neist 65 patsiendist olid saavutanud täieliku molekulaarse remissiooni, mille keskmine jälgimisperiood oli 28 kuud (vahemik 13–67 kuud). Nende patsientide vanus oli 25 kuni 72. Lisaks sellele teatasid uurijad sümptomite paranemise ja muude funktsionaalsete organite kõrvalekallete kliinilistest juhtudest. On teatatud südame, närvisüsteemi, naha / nahaaluskoe, hingamisteede / rindkere / mediastiinumi, lihasluukonna / sidekoe / veresoonte ja seedetrakti paranemisest. HES / CEL -iga lastel ei ole kontrollitud uuringuid. Kolmes publikatsioonis teatati kolmest patsiendist, kellel oli PDGFR geeni ümberkorraldamisega seotud HES ja CLE. Nende patsientide vanus oli 2 kuni 16 aastat ja imatiniibi manustati annuses 300 mg / m2 päevas või annuses 200 kuni 400 mg ööpäevas. Kõik patsiendid olid saavutanud hematoloogilise vastuse, täieliku tsütogeneetilise vastuse ja / või täielik molekulaarne reaktsioon. Kliinilised uuringud mittetoimiva ja / või metastaatilise GIST -iga Rahvusvaheline, randomiseeritud, kontrollimatu, II faasi avatud uuring viidi läbi patsientidel, kellel oli eemaldatav või metastaatiline pahaloomuline seedetrakti strooma kasvaja (GIST). Selles uuringus osales ja randomiseeriti 147 patsienti. Said suukaudselt 400 mg või 600 mg üks kord ööpäevas kuni 36 kuud. Need patsiendid olid vanuses 18 kuni 83 aastat ja neil oli patoloogiline diagnoos eemaldamatute ja / või metastaatiliste pahaloomuliste komplekt. Immunohistokeemilised testid viidi perioodiliselt läbi Kit-antikehaga (A-4502, polükloonitud küüliku antiseerum, 1: 100; DAKO Corporation, Carpinteria, CA) vastavalt analüüsile avidiini-biotiin-peroksidaasi kompleksi meetodiga pärast antigeeni taastumist.. Peamised tõendid efektiivsuse kohta põhinesid objektiivsetel raviväärtustel.Kasvajad pidid olema vähemalt ühes haiguse punktis mõõdetavad ja ravivastuse iseloomustamine põhines Edela -onkoloogia rühma (SWOG) kriteeriumidel. Tulemused on esitatud tabelis 7. Tabel 7 Parim kasvajavastus uuringus STIB2222 (GIST) Kahe ravigrupi ravivastuses ei olnud erinevusi. Märkimisväärne osa patsiente, kellel oli vaheanalüüsi ajal haigus stabiliseerunud, saavutas osalise ravivastuse pikema ravi korral (keskmine jälgimisperiood 31 kuud). Keskmine ravivastus oli 13 nädalat (95% CI 12–23). ravile ebaõnnestunud patsientide ravile kulunud aeg oli 122 nädalat (95% CI 106-147), samas kui kogu uuringupopulatsioonis oli see 84 nädalat (95% CI 71–109). Keskmist elulemust ei saavutatud. pärast 36-kuulist jälgimist on 68%. Kahes kliinilises uuringus (uuring B2222 ja rühmadevaheline uuring S0033) suurendati Gliveci ööpäevast annust kuni 800 mg -ni patsientidel, kelle annus oli 400 mg või 600 mg. Päevane annus suurendati 800 mg -ni kokku 103 patsiendil; 6 patsienti saavutasid pärast annuse suurendamist osalise ravivastuse ja 21 haiguse stabiliseerumise, mille üldine kliiniline kasu oli 26%. Olemasolevate ohutusandmete põhjal ei tundu Gliveci ohutusprofiil päevase annuse suurendamisel olevat mõjutatud. 800 mg -ni väheneb 400 mg või 600 mg ööpäevane annus. GIST -i adjuvantravi kliinilised uuringud Adjuvantravi Gliveciga hinnati mitmekeskuselises topeltpimedas pikaajalises platseebokontrollitud III faasi uuringus (Z9001), milles osales 773 patsienti. Nende patsientide vanus oli vahemikus 18 kuni 91 aastat. Uuringusse kaasatud patsientidel oli immunohistokeemia abil esmane GIST histoloogiline diagnoos koos Kit -valgu ekspressiooni ja kasvaja läbimõõduga üle 3 cm, kusjuures esmane resektsioon oli täielik GIST. 14-70 päeva jooksul enne registreerumist. Pärast esmase GIST resektsiooni randomiseeriti patsiendid ühte kahest ravigrupist: Glivec 400 mg päevas või platseebo ühe aasta jooksul. Uuringu esmane efektiivsuse lõpp-punkt oli retsidiivivaba elulemus (RFS), mis on määratletud kui aeg alates randomiseerimise kuupäevast kuni retsidiivi või mis tahes põhjusel surma kuupäevani. Glivec pikendas oluliselt RFS -i, 75% patsientidest taastus 38 kuu pärast Gliveci rühmas ja 20 kuud platseeborühmas (vastavalt 95% CI [30 - ei ole võimalik hinnata; [14 - ei ole võimalik hinnata]]); (riskisuhe = 0,398 [0,259-0,610], lk Kordumise riski patsientidel pärast esmase GIST resektsiooni hinnati tagasiulatuvalt järgmiste prognostiliste tegurite alusel: kasvaja suurus, mitootiline indeks, kasvaja asukoht. Mitootilise indeksi andmed olid kättesaadavad 556 patsiendil 713-st [ravile kavatsetud (ITT) populatsioon]. Alamrühmade analüüside tulemused vastavalt USA riiklike tervishoiuinstituutide (NIH) riskiklassifikatsioonidele ja relvajõudude patoloogia instituudile (AFIP) , on näidatud tabelis 8. Madala ja väga madala riskiga rühmades kasu ei täheldatud. Üldist kasu ellujäämisest ei täheldatud. Tabel 8 Z9001 uuringu kokkuvõte RFS analüüsid vastavalt NIH ja AFIP riskiklassifikatsioonidele * täielik jälgimisperiood; NS - pole hinnanguline Teises III faasi avatud ja mitmekeskuselises uuringus (SSG XVIII / AIO) võrreldi 12-kuulist ravi Glivec’iga 400 mg ööpäevas võrreldes 36-kuulise raviga patsientidel pärast GIST-i kirurgilist resektsiooni ja ühte järgmistest teguritest: kasvaja > 5 cm ja mitootiline arv> 5/50 suure võimsusega väljad (HPF); o kasvaja läbimõõt> 10 cm ja mis tahes suurusega mitootiline arv või mis tahes suurusega kasvaja, mille mitootiline arv on> 10/50 HPF või kasvaja rebenemine kõhukelmeõõnes. Kokku nõustus ja randomiseeriti uuringus 397 patsienti (199 patsienti 12-kuulises rühmas ja 198 patsienti 36-kuulises rühmas), keskmine vanus oli 61 aastat (vahemik 22–84 aastat). -kuni 54 kuud (randomiseerimise kuupäevast kuni andmete katkestamise kuupäevani), esimese randomiseeritud patsiendi ja lõppkuupäeva vahel oli kokku 83 kuud. Uuringu esmane tulemusnäitaja oli retsidiivivaba elulemus (RFS), mis on määratletud kui aeg randomiseerimise kuupäevast kuni retsidiivi või mis tahes põhjusel surma kuupäevani. Ravi Gliveciga kolmkümmend kuus kuud pikendas oluliselt RFS-i võrreldes Glivec-raviga 12 kuud (üldine riskisuhe (HR) = 0,46 [0,32; 0,65], p Lisaks pikendas Glivec-ravi kolmkümmend kuus kuud oluliselt võrreldes üldise elulemusega (OS) võrreldes 12-kuulise Glivec-raviga (HR = 0,45 [0,22; 0,89], p = 0,0187) (tabel 9). Pikem ravi kestus (> 36 kuud) võib edasiste ägenemiste tekkimist edasi lükata; nende tõendite mõju üldisele elulemusele on siiski teadmata. 12-kuulises ravirühmas oli surmajuhtumeid 25 ja 36-kuulises ravis 12. ITT analüüsis, st kogu uuringupopulatsioonis, oli 36 -kuuline ravi imatiniibiga parem kui 12 -kuuline ravi. Planeeritud alarühma analüüsis mutatsioonitüübi järgi, eksoniga 11 seotud mutatsiooniga patsientidel, HRS 36 kuu jooksul oli 0,35 [95% CI: 0,22; 0,56] .Muude vähem levinud mutatsioonide alarühmade kohta ei saa järeldusi teha, kuna täheldatud sündmusi on vähe. Tabel 9 Ravi Gliveciga 12 kuud ja 36 kuud (uuring SSGXVIII / AIO) C-Kit-positiivsete GIST-iga lastel ei ole kontrollitud uuringuid. Seitseteist GIST -ga patsienti (koos Kit ja PDGFR mutatsioonidega või ilma) on teatatud 7 väljaandes. Nende patsientide vanus oli 8 kuni 18 aastat ja imatiniibi manustati nii adjuvant- kui ka metastaatilises vormis ööpäevastes annustes vahemikus 300 kuni 800 mg. Enamikul GIST-iga ravitud lastel puudusid kinnitavad andmed c-kit või PDGFR mutatsioonide kohta, mis võisid viia vastuoluliste kliiniliste tulemusteni. DFSP kliinilised uuringud Viidi läbi avatud, mitmekeskuseline II faasi kliiniline uuring (uuring B2225), milles osales 12 DFSP-ga patsienti, keda raviti Gliveciga 800 mg ööpäevas.DFSP-ga patsientide vanus oli 23 kuni 75 aastat; DFSP oli metastaatiline, pärast esmast kirurgilist resektsiooni kordus lokaalselt ja seda ei peetud uuringusse sisenemisel enam resekteeritavaks. Esmased tõendid efektiivsuse kohta põhinesid objektiivsel ravivastusel. 12 -st registreeritud patsiendist oli 9 ravivastust, millest üks oli täielik ja 8 osaline. Kolm osalise ravivastusega patsienti muudeti kirurgiliselt haigustest vabaks. Ravi keskmine kestus uuringus B2225 oli 6,2 kuud, maksimaalne kestus 24,3 kuud. Viiest avaldatud kliinilisest juhtumist teatati veel 6 Gliveciga ravitud DFSP -ga patsiendist, nende vanus oli 18 kuud kuni 49 aastat. Avaldatud kirjanduses kirjeldatud täiskasvanud patsiente raviti Gliveciga 400 mg (4 juhtu) või 800 mg päevas (1 juhtum). Viiel patsiendil oli ravivastus, millest 3 olid täielikud ja 2 osalised. Ravi keskmine kestus avaldatud kirjanduses oli 4 nädalat kuni rohkem kui 20 kuud. Translokatsioon t (17:22) [(q22: q13)] või selle geeniprodukt esines peaaegu kõigil Glivec -ravi saanud patsientidel. DFSP -ga lastel ei ole kontrollitud uuringuid. Kolmes väljaandes teatati viiest DFSP ja PDGFR geeni ümberkorraldamisega patsiendist.Nende patsientide vanus varieerus vastsündinust kuni 14 aastani ja imatiniibi manustati annuses 50 mg ööpäevas või annustes 400 kuni 520 mg / m2 päevas. Kõik patsiendid saavutasid osalise ja / või täieliku ravivastuse. Gliveci farmakokineetika Gliveci farmakokineetikat hinnati annuste vahemikus 25 kuni 1000 mg. Plasma farmakokineetilisi profiile analüüsiti 1. ja 7. või 28. või 28. päeval, milleks plasmakontsentratsioon oli saavutanud püsiseisundi. Imendumine Kapslivormi keskmine absoluutne biosaadavus on 98%. Pärast suukaudset annust on imatiniibi plasmakontsentratsiooni AUC tasemed patsientide vahel väga varieeruvad. Suure rasvasisaldusega eine manustamisel vähenes imatiniibi imendumiskiirus minimaalselt (Cmax vähenes 11% ja Tmax pikenes 1,5 tunni võrra). kerge AUC vähenemine (7,4%) võrreldes tühja kõhuga. Eelmise operatsiooni mõju ravimi imendumisele ei ole uuritud. Levitamine Kliiniliselt oluliste imatiniibi kontsentratsioonide korral seondub plasmavalkudega katsete põhjal in vitrooli ligikaudu 95%, peamiselt albumiini ja alfa-happe glükoproteiinidega, minimaalselt seondudes lipoproteiinidega. Biotransformatsioon Inimeste peamine ringlev metaboliit on piperasiini N-demetüleeritud derivaat, millel on in vitro aktiivsus sarnane molekuliga, millest see pärineb. Selle metaboliidi plasma AUC moodustas ainult 16% imatiniibi AUC-st N-desmetüülmetaboliidi seondumine plasmavalkudega on sarnane lähteühendiga. Imatiniib ja N-desmetüülmetaboliit moodustasid kokku ligikaudu 65% ringlevast radioaktiivsusest (AUC (0-48h)). Ülejäänud ringleva radioaktiivsuse põhjuseks olid mitmed väikesed metaboliidid. Tulemused in vitro näitas, et CYP3A4 oli peamine inimese P450 ensüüm, mis katalüüsib imatiniibi biotransformatsiooni. Terve rühma võimalikest ravimitest (paratsetamool, atsükloviir, allopurinool, amfoteritsiin, tsütarabiin, erütromütsiin, flukonasool, hüdroksüuurea, norfloksatsiin, penitsilliin V) näitasid ainult erütromütsiin (IC50 50 mcM) ja flukonasool (IC50 118 mcM inhibeerimine) võib olla kliiniliselt oluline. Imatiniib in vitro osutus CYP2C9, CYP2D6 ja CYP3A4 / 5 märgistatud substraatide konkureerivaks inhibiitoriks. Ki väärtused inimese maksa mikrosoomides olid vastavalt 27, 7,5 ja 7,9 μmol / l. Imatiniibi maksimaalne plasmakontsentratsioon on patsientidel 2 ... 4 μmol / l ja seetõttu on võimalik samaaegselt kasutatavate ravimite CYP2D6 ja / või CYP3A4 / 5 vahendatud metaboolne pärssimine. Imatiniib ei seganud 5-fluorouratsiili biotransformatsiooni, kuid pärssis paklitakseeli metabolismi CYP2C8 konkureeriva pärssimise tagajärjel (Ki = 34,7 mcM). See Ki väärtus on palju kõrgem kui imatiniibi plasmakontsentratsioon, mida patsientidel oodatakse, ja seetõttu ei ole koostoimeid 5-fluorouratsiili või paklitakseeli ja imatiniibi samaaegsel manustamisel oodata. Elimineerimine Põhinedes ühendi (te) taastumisel pärast 14C-märgistatud imatiniibi suukaudset manustamist, leiti ligikaudu 81% annusest 7 päeva jooksul väljaheitega (68% annusest) ja uriiniga (13% annusest). annus koosnes muutumatust imatiniibist (5% uriin, 20% väljaheide), ülejäänud metaboliidid. Plasma farmakokineetika Keskmine AUC suurenemine pärast annuse suurendamist oli pärast suukaudset manustamist lineaarne ja annusega proportsionaalne vahemikus 25 ... 1000 mg imatiniibi, kumulatsioon oli 1,5 ... 2,5 korda suurem kui tasakaalukontsentratsioonis pärast üks kord ööpäevas manustamist. Farmakokineetika GIST -ga patsientidel GIST-ga patsientidel oli püsiseisundi ekspositsioon 1,5 korda suurem kui KML-i patsientidel sama annuse (400 mg päevas) korral. Esialgsete populatsiooni farmakokineetiliste analüüside põhjal GIST-i patsientidel oli kolm muutujat (albumiin, leukotsüütid ja bilirubiin) millel oli statistiliselt oluline korrelatsioon imatiniibi farmakokineetikaga. Albumiini väärtuste vähenemine põhjustas kliirensi vähenemise (CL / f) ja kõrgemate leukotsüütide taseme. on toonud kaasa CL / f vähenemise. Need korrelatsioonid Selles patsiendipopulatsioonis võivad maksa metastaaside esinemine potentsiaalselt põhjustada maksapuudulikkust ja ainevahetushäireid. Populatsiooni farmakokineetika KML -i patsientide populatsiooni farmakokineetiline analüüs näitas vanuse piiratud mõju jaotusruumalale (üle 65 -aastastel patsientidel suurenes see 12%). Seda variatsiooni ei peeta kliiniliselt oluliseks. Kehakaalu mõju imatiniibi kliirensile on selline, et 50 kg kaaluva patsiendi puhul on eeldatav keskmine kliirens 8,5 l / h, samas kui 100 kg kaaluva patsiendi puhul suureneb kliirens kuni 11,8 l / h. Neid variatsioone ei peeta piisavateks, et võimaldada annuse kohandamist vastavalt kehakaalu kilogrammidele. Sugu ei mõjuta imatiniibi kineetikat. Farmakokineetika lastel Nagu täiskasvanud patsientidel, imendus imatiniib lastel pärast suukaudset manustamist kiiresti nii I kui ka II faasi uuringutes. Manustades lastele annuseid 260 ja 340 mg / m2 / päevas, saavutati sarnane kokkupuude täiskasvanutega, keda raviti vastavalt 400 mg ja 600 mg annustega. AUC (0–24) võrdlus 8. ja 1. päeva tasemega annuses 340 mg / m2 / päevas näitas ravimi kogunemist 1,7 korda rohkem kui korduv ühekordse annuse manustamine. Tuginedes populatsiooni kombineeritud farmakokineetilisele analüüsile hematoloogiliste häiretega (KML, Ph + ALL või muud imatiniibiga ravitud hematoloogilised häired) lastel, suureneb imatiniibi kliirens koos kehapinna suurenemisega. Pärast BSA toime korrigeerimist ei näidanud muud demograafilised tegurid, nagu vanus, kehakaal ja kehamassiindeks, kliiniliselt olulist mõju imatiniibi ekspositsioonile. Analüüs kinnitas, et imatiniibi ekspositsioon lastel, kes said 260 mg / m2 üks kord ööpäevas (mitte üle 400 mg üks kord ööpäevas) või 340 mg / m2 üks kord ööpäevas (mitte üle 600 mg üks kord ööpäevas), oli sarnane imatiniibi saanud või 600 mg üks kord ööpäevas. Elundite funktsiooni halvenemine Imatiniib ja selle metaboliidid ei eritu oluliselt neerude kaudu. Kerge ja mõõduka neerukahjustusega patsientidel on plasmakontsentratsioon suurem kui normaalse neerufunktsiooniga patsientidel. Suurenemine on ligikaudu 1,5 kuni 2 korda, mis vastab 1,5-kordsele plasmakontsentratsiooni suurenemisele, millega imatiniib seondub tugevalt. Imatiniibi kliirens vaba ravimina on tõenäoliselt sarnane neerufunktsiooni kahjustusega patsientidel. imatiniibi eritumine ainult neerude kaudu (vt lõigud 4.2 ja 4.4). Kuigi farmakokineetiliste analüüside tulemused näitasid märkimisväärset erinevust patsientide vahel, ei suurenenud imatiniibi keskmine ekspositsioon erineva raskusega maksafunktsiooni häirega patsientidel võrreldes normaalse maksafunktsiooniga patsientidega (vt lõigud 4.2, 4.4 ja 4.8). Imatiniibi prekliinilist ohutusprofiili hinnati hiirtel, koertel, ahvidel ja küülikutel. Mitme annuse toksilisuse uuringud näitasid hiirtel, koertel ja ahvidel kergeid kuni mõõdukaid hematoloogilisi muutusi, millega kaasnesid luuüdi muutused hiirtel ja koertel. Maks oli hiirte ja koerte sihtorgan. Mõlemal liigil täheldati transaminaaside taseme kerget kuni mõõdukat tõusu ning kolesterooli, triglütseriidide, üldvalgu ja albumiini taseme kerget langust. Hiirtel ei täheldatud maksa histopatoloogilisi muutusi. Hiirtel täheldati histopatoloogilist maksamuutust. Raske maksatoksilisuse tase koeri, keda raviti 2 nädalat, maksaensüümide aktiivsuse tõus, hepatotsellulaarne nekroos, nekroos ja sapiteede hüperplaasia. Ahvidel, kes said ravi 2 nädala jooksul, täheldati neerutoksilisuse nähtusi fokaalse mineraliseerumise ja neerutuubulite laienemise ning tubulaarse nefropaatia korral.Mitmetel nendel loomadel täheldati vere uurea lämmastiku (BUN) ja kreatiniini taseme tõusu. 13-nädalase uuringu käigus leiti hiirtel 13-nädalase uuringu käigus teatamata üleminekuepiteeli hüperplaasia neerupapillis ja kusepõies. mis tahes muutused seerumi ja uriini parameetrites. Imatiniibi kroonilise ravi korral täheldatakse oportunistlike infektsioonide esinemissageduse suurenemist. 39-nädalases ahvide uuringus ei tuvastatud NOAEL-i (täheldatud kõrvaltoimete taset) väikseima annuse 15 mg / kg juures, mis vastab ligikaudu kolmandikule inimese maksimaalsest 800 mg annusest. arvutatakse keha pinna järgi. Nendel loomadel läbi viidud ravi halvendas tavaliselt pärsitud malaariainfektsioone. Imatiniibi ei peetud bakterirakkude testis genotoksiliseks ma kutsun (Amesi test), imetajarakkude analüüsiga in vitro (hiire lümfoom) ja hiire mikrotuuma testiga in vivo. Imetajarakkude analüüsis saadi imatiniibile positiivne genotoksiline toime in vitro (Hiina hamstri munasari), mis on tingitud klastogeensusest (kromosomaalne aberratsioon) metaboolse aktiveerimise juuresolekul. Kaks valmistamisprotsessi vaheühendit, mis sisalduvad ka lõpptootes, osutusid Amesi testis mutageneesi suhtes positiivseks ja üks neist oli positiivne ka hiire lümfoomi analüüsis. Isastel hiirtel läbi viidud fertiilsusuuringus, mille annused vastasid ligikaudu kliinilisele maksimaalsele ööpäevasele annusele 800 mg, mis määrati kehapinna alusel ja mida manustati 70 päeva enne paaritumist, munandite ja munandimanuse kaal ja liikuvate sperma protsent langes 60 mg / kg. Seda nähtust ei leitud annustes ≤20 mg / kg. Kerget kuni mõõdukat spermatogeneesi vähenemist täheldati ka koeral suukaudsete annuste ≥30 mg / kg kasutamisel. Kui emastele hiirtele manustati 14 päeva, enne paaritumist ja kuni kuuenda tiinuspäevani, ei avaldanud see mõju paaritumisele ega raseduste arvule. Annuste 60 mg / kg korral esines emastel hiirtel märkimisväärne siirdamisjärgne lootekaotus ja vähem eluslooteid, seda ei täheldatud annuste ≤20 mg / kg korral. Rottidel läbi viidud pre- ja postnataalse arengu häirete uuringus suukaudsel manustamisel täheldati punast tupest eritumist 45 mg / kg / päevas rühmas 14. või 15. tiinuspäeval. Sama annuse korral suurenes surnult sündide ja subjektide arv, kes surid 0–4 päeva jooksul pärast sünnitust. Sama annuse korral vähenes F1 järglaste keskmine kehakaal sünnist kuni lõpliku ohverdamiseni ja eesnaha eraldamise kriteeriumidele vastavate katsealuste arv veidi vähenes. F1 põlvkonna viljakust see ei mõjutanud, samas kui annuses 45 mg / kg päevas täheldati resorptsioonide arvu suurenemist ja elujõuliste loote arvu vähenemist. Nii emade kui ka F1 põlvkonna puhul oli täheldatud toime puudumise tase (NOEL) 15 mg / kg päevas (üks neljandik maksimaalsest inimese annusest 800 mg). Imatiniib oli hiirtel teratogeenne, kui seda manustati organogeneesi ajal annustes ≥100 mg / kg, mis on ligikaudu samaväärne maksimaalse kliinilise annusega 800 mg / päevas, mis määratakse kindlaks kehapinna järgi. eesmised luud ja parietaalsete luude puudumine Neid toimeid ei täheldatud annuste ≤30 mg / kg korral. Arengutoksikoloogia uuringus noorukite rottidega (10. kuni 70. päev pärast sünnitust) ei tuvastatud uusi sihtorganeid võrreldes täiskasvanud rottide teadaolevate sihtorganitega. Noorte loomade toksikoloogilises uuringus täheldati mõju kasvule, aeglustunud tupe avanemisele ja eesnaha eraldumisele ligikaudu 0,3–2-kordse maksimaalse soovitatava annuse 340 mg / m2 kohta lastele. Lisaks täheldati noorloomade suremust (võõrutamise ajal) ligikaudu 2 -kordse laste keskmise ekspositsiooni korral maksimaalse soovitatud annuse 340 mg / m2 korral. Kaheaastane kantserogeensusuuring rottidel, keda raviti imatiniibi annustega 15, 30 ja 60 mg / kg ööpäevas, näitas statistiliselt olulist vähenemist isastel, kes said ravi annusega 60 mg / kg / päevas, ja emasloomadel, keda raviti annustega ≥30 mg / kg päevas. Surnu histopatoloogilisel uurimisel ilmnesid surma või ohverdamise peamised põhjused kardiomüopaatia (mõlemast soost), krooniline progresseeruv nefropaatia (naised) ja eesnäärme papilloom. Neoplastiliste muutuste sihtorganid olid neerud, kusepõis, kusiti. ees- ja kliitornäärmed, peensool, kõrvalkilpnäärmed, neerupealised ja mao mitte-näärmeosa. Annuseid alates 30 mg / kg ööpäevas on täheldatud eesnäärme- ja kliitornäärmete papilloomide / kartsinoomide puhul, mis on ligikaudu 0,5 või 0,3 korda suuremad kui inimese ööpäevane ekspositsioon 400 mg / päevas või 800 mg / päevas (põhineb AUC) ja 0,4 -kordne ööpäevane ekspositsioon lastel annuses 340 mg / m2 / päevas (AUC põhjal). Efekti puudumise tase (NOEL) oli 15 mg / kg / päevas. Neeru adenoom / kartsinoom, kusepõie papilloom 60 mg / kg ööpäevas on ligikaudu 1,7 või 1 kordne inimese ööpäevane ekspositsioon 400 mg / päevas või 800 mg / päevas (vastavalt AUC -le) ja 1,2 -kordne ööpäevane ekspositsioon lastel 340 mg / m2 / päevas (AUC põhjal). ei täheldatud toimet (NOEL) oli 30 mg / kg / päevas. Inimeste puhul ei ole nende leidude mehhanismi ja asjakohasust rottide kartsinogeneesi uuringus veel selgitatud. Mitte-neoplastilised kahjustused, mida varasemates prekliinilistes uuringutes ei tuvastatud, hõlmasid kardiovaskulaarsüsteemi, kõhunääret, endokriinorganeid ja hambaid. Kõige märkimisväärsemad muutused hõlmasid südame hüpertroofiat ja laienemist, mis põhjustas mõnedel loomadel südamepuudulikkuse tunnuseid. Toimeaine imatiniib kujutab endast setteorganismidele keskkonnaohtu. Kapsli sisu: mikrokristalne tselluloos Krospovidoon Magneesiumstearaat Kolloidne ränidioksiid, veevaba Kapsli kest: želatiin Kollane raudoksiid (E172) Titaandioksiid (E171) Trükivärv: punane raudoksiid (E172) Shellac Soja letsitiin Ei ole asjakohane. 2 aastat Hoida temperatuuril kuni 30 ° C. Ravimit niiskuse eest kaitsmiseks hoida originaalpakendis. PVC / alumiinium blister Pakendis 30 kapslit. Kasutamata ravim ja sellest tekkinud jäätmed tuleb hävitada vastavalt kohalikele eeskirjadele. Novartis Europharm Limited Wimblehurst Road Horsham Lääne -Sussex, RH12 5AB Ühendkuningriik EL/1/01/198/001 035372010 Müügiloa esmase väljastamise kuupäev: 7. november 2001 Viimase uuendamise kuupäev: 7. november 2006 Juuli 2014
Üleannustamine Mida teha, kui olete võtnud liiga palju Gliveci
Kõrvaltoimed Millised on Gliveci kõrvaltoimed
Aegumine ja säilitamine
Kõige ajakohasemale versioonile juurdepääsu saamiseks on soovitatav külastada AIFA (Itaalia ravimiamet) veebisaiti. Vastutusest loobumine ja kasulik teave. 01.0 RAVIMPREPARAADI NIMETUS
02.0 KVALITATIIVNE JA KVANTITATIIVNE KOOSTIS
03.0 RAVIMVORM
04.0 KLIINILINE TEAVE
04.1 Näidustused
04.2 Annustamine ja manustamisviis
HES / CEL (algannus 100 mg) ANC 1. Peatage Glivec -ravi, kuni ANC on ≥ 1,5 x 109 / l ja trombotsüüdid ≥ 75 x 109 / l. 2. Jätkake ravi Gliveciga eelmise annusega (nt enne tõsist kõrvaltoimet). Kroonilise faasi CML, MDS / MPD ja GIST (algannus 400 mg) HES / CEL (annus 400 mg) ANC 1. Peatage Glivec -ravi, kuni ANC on ≥ 1,5 x 109 / l ja trombotsüüdid ≥75 x 109 / l. 2. Jätkake ravi Gliveciga eelmise annusega (nt enne tõsist kõrvaltoimet). 3. Korduva esinemise korral ANC Laste kroonilise faasi KML (annus 340 mg / m2) ANC 1. Peatage Glivec -ravi, kuni ANC on ≥ 1,5 x 109 / l ja trombotsüüdid ≥75 x 109 / l. 2. Jätkake ravi Gliveciga eelmise annusega (nt enne tõsist kõrvaltoimet). 3. Kordumise korral NCA 2. Kiirendatud faasi CML ja blastakriis ning Ph + ALL (algannus 600 mg) aANC 1. Kontrollige, kas tsütopeenia on seotud leukeemiaga (luuüdi aspiratsioon või biopsia). 2. Kui tsütopeenia ei ole seotud leukeemiaga, vähendage Gliveci annust 400 mg -ni. 3. Kui tsütopeenia püsib 2 nädalat, vähendage annust veelgi 300 mg -ni. 4. Kui tsütopeenia püsib 4 nädalat ja see ei ole endiselt seotud leukeemiaga, katkestage Glivec -ravi, kuni ANC on ≥ 1 x 109 / l ja trombotsüüdid ≥ 20 x 109 / l, seejärel jätkake ravi annusega 300 mg. Laste kiirendatud faasi KML ja lööklaine (algannus 340 mg / m2) aANC 1. Kontrollige, kas tsütopeenia on seotud leukeemiaga (luuüdi aspiratsioon või biopsia). 2. Kui tsütopeenia ei ole seotud leukeemiaga, vähendage Gliveci annust 260 mg / m2 -ni. 3. Kui tsütopeenia püsib 2 nädalat, vähendage seda veelgi 200 mg / m2 -ni. 4. Kui tsütopeenia püsib 4 nädalat ja ei ole endiselt seotud leukeemiaga, katkestage Glivec -ravi, kuni ANC on ≥ 1 x 109 / l ja trombotsüüdid ≥ 20 x 109 / l, seejärel jätkake ravi annusega 200 mg / m2. DFSP (annus 800 mg) ANC 1. Peatage Glivec -ravi, kuni ANC on ≥ 1,5 x 109 / l ja trombotsüüdid ≥75 x 109 / l. 2. Jätkake ravi Gliveciga annuses 600 mg. 3. Korduva esinemise korral ANC ANC = neutrofiilide absoluutarv
valu ilmneb pärast vähemalt 1 -kuulist ravi Maksafunktsiooni häired Maksafunktsiooni analüüs Kerge Kogu bilirubiin: = 1,5 ULN AST:> ULN (võib olla normaalne või ULN) Mõõdukas Kogu bilirubiin:> 1,5-3,0 ULN AST: ükskõik Tõsine Kogu bilirubiin:> 3–10 ULN
AST: ükskõik
04.3 Vastunäidustused
04.4 Erihoiatused ja asjakohased ettevaatusabinõud kasutamisel
04.5 Koostoimed teiste ravimitega ja muud koostoimed
04.6 Rasedus ja imetamine
04.7 Mõju autojuhtimise ja masinate käsitsemise võimele
04.8 Kõrvaltoimed
Infektsioonid ja infestatsioonid Aeg -ajalt: Herpes zoster, herpes simplex, nasofarüngiit, kopsupõletik1, sinusiit, tselluliit, ülemiste hingamisteede infektsioon, gripp, kuseteede infektsioon, gastroenteriit, sepsis Haruldane: Seenhaigus Healoomulised, pahaloomulised ja täpsustamata kasvajad (sh tsüstid ja polüübid) Haruldane: Kasvaja lüüsi sündroom Vere ja lümfisüsteemi häired Väga tavaline: Neutropeenia, trombotsütopeenia, aneemia Sage: Pantsütopeenia, palavikuline neutropeenia Aeg -ajalt: Trombotsüteemia, lümfopeenia, luuüdi depressioon, eosinofiilia, lümfadenopaatia Haruldane: Hemolüütiline aneemia Ainevahetus- ja toitumishäired Sage: Anoreksia Aeg -ajalt: Hüpokaleemia, söögiisu suurenemine, hüpofosfateemia, isu vähenemine, dehüdratsioon, podagra, hüperurikeemia, hüperkaltseemia, hüperglükeemia, hüponatreemia Haruldane: Hüperkaleemia, hüpomagneseemia Psühhiaatrilised häired Sage: Unetus Aeg -ajalt: Depressioon, vähenenud libiido, ärevus Haruldane: Segadusseisund Närvisüsteemi häired Väga tavaline: Peavalu 2 Sage: Pearinglus, paresteesia, maitsetundlikkuse häired, hüpoesteesia Aeg -ajalt: Migreen, unisus, minestus, perifeerne neuropaatia, mäluhäired, ishias, rahutute jalgade sündroom, värin, ajuverejooks Haruldane: Suurenenud intrakraniaalne rõhk, krambid, optiline neuriit Silma häired Sage: Silmalaugude turse, suurenenud pisaravool, konjunktiivi hemorraagia, konjunktiviit, silmade kuivus, ähmane nägemine Aeg -ajalt: Silmaärritus, silmavalu, orbitaalne turse, skleraverejooks, võrkkesta verejooks, blefariit, makulaarne turse Haruldane: Katarakt, glaukoom, papilloom Kõrva ja labürindi häired Aeg -ajalt: Peapööritus, tinnitus, kuulmislangus Südame patoloogiad Aeg -ajalt: Südamepekslemine, tahhükardia, südame paispuudulikkus3, kopsuturse Haruldane: Arütmia, kodade virvendusarütmia, südameseiskus, müokardiinfarkt, stenokardia, perikardi efusioon Vaskulaarsed häired 4 Sage: Õhetus, verejooks Aeg -ajalt: Hüpertensioon, hematoom, subduraalne hematoom, jäsemete jahutamine, hüpotensioon, Raynaud 'nähtus Hingamisteede, rindkere ja mediastiinumi häired Sage: Düspnoe, ninaverejooks, köha Aeg -ajalt: Pleuraefusioon5, neelupõletiku valu, farüngiit Haruldane: Pleuriitiline valu, kopsufibroos, pulmonaalne hüpertensioon, kopsuverejooks Seedetrakti häired Väga tavaline: Iiveldus, kõhulahtisus, oksendamine, düspepsia, kõhuvalu 6 Sage: Kõhupuhitus, kõhupuhitus, gastroösofageaalne refluks, kõhukinnisus, suukuivus, gastriit Aeg -ajalt: Stomatiit, suuhaavandid, seedetrakti verejooks7, röhitsemine, melaena, ösofagiit, astsiit, maohaavand, hematemees, heiliit, düsfaagia, pankreatiit Haruldane: Koliit, iileus, põletikuline soolehaigus Maksa ja sapiteede häired Sage: Maksaensüümide aktiivsuse suurenemine Aeg -ajalt: Hüperbilirubineemia, hepatiit, ikterus Haruldane: Maksapuudulikkus8, maksanekroos Naha ja nahaaluskoe kahjustused Väga tavaline: Periorbitaalne turse, dermatiit / ekseem / lööve Sage: Sügelus, näo turse, naha kuivus, erüteem, alopeetsia, öine higistamine, valgustundlikkusreaktsioonid Aeg -ajalt: Pustuloosne lööve, verevalumid, suurenenud higistamine, nõgestõbi, ekhümoos, suurenenud kalduvus verevalumitele, hüpotrichoos, naha hüpopigmentatsioon, eksfoliatiivne dermatiit, onühhoklaas, follikuliit, petehhiad, psoriaas, purpur, naha hüperpigmentatsioon, bulloossed lööbed Haruldane: Äge palavikuline neutrofiilne dermatoos (Sweet'i sündroom), küünte värvimuutus, angioneurootiline turse, vesikulaarne lööve, multiformne erüteem, leukotsütoklastiline vaskuliit, Stevensi-Johnsoni sündroom, äge generaliseerunud eksantematoosne pustuloos (AGEP) Lihas -skeleti ja sidekoe kahjustused Väga tavaline: Lihaste spasmid ja krambid, luu- ja lihaskonna valu, sealhulgas müalgia, artralgia, luuvalu9 Sage: Liigeste turse Aeg -ajalt: Liigeste ja lihaste jäikus Haruldane: Lihasnõrkus, artriit, rabdomüolüüs / müopaatia Neerude ja kuseteede häired Aeg -ajalt: Neeruvalu, hematuuria, äge neerupuudulikkus, pollakiuria Reproduktiivse süsteemi ja rinnanäärme haigused Aeg -ajalt: Günekomastia, erektsioonihäired, menorraagia, ebaregulaarne menstruatsioon, seksuaalne düsfunktsioon, nibuvalu, rindade suurenemine, munandikoti turse Haruldane: Hemorraagiline kollane keha / hemorraagiline munasarja tsüst Üldised häired ja manustamiskoha reaktsioonid Väga tavaline: Veepeetus ja turse, väsimus Sage: Nõrkus, palavik, anasarca, külmavärinad, värin Aeg -ajalt: Valu rinnus, halb enesetunne Diagnostilised testid Väga tavaline: Kaalutõus Sage: Kaalukaotus Aeg -ajalt: Vere kreatiniinisisalduse suurenemine, vere kreatiinfosfokinaasi taseme tõus, laktaatdehüdrogenaasi sisalduse suurenemine veres, leeliselise fosfataasi taseme tõus
Haruldane: Suurenenud vere amülaas Healoomulised, pahaloomulised ja täpsustamata kasvajad (sh tsüstid ja polüübid) Teadmata: Kasvaja verejooks / kasvaja nekroos Immuunsüsteemi häired Teadmata: Anafülaktiline šokk Närvisüsteemi häired Teadmata: Aju turse Silma häired Teadmata: Klaaskeha hemorraagia Südame patoloogiad Teadmata: Perikardiit, südame tamponaad Vaskulaarsed patoloogiad Teadmata: Tromboos / emboolia Hingamisteede, rindkere ja mediastiinumi häired Teadmata: Äge hingamispuudulikkus1, interstitsiaalne kopsuhaigus Seedetrakti häired Teadmata: Iileus / soole obstruktsioon, seedetrakti perforatsioon, divertikuliit Naha ja nahaaluskoe kahjustused Teadmata: Palmar-plantaarne erütrodüsesteesia sündroom Teadmata: Lichenoidne keratoos, samblik planus Teadmata: Toksiline epidermaalne nekrolüüs Teadmata: Nahareaktsioon eosinofiilia ja süsteemsete sümptomitega (DRESS) Lihas -skeleti ja sidekoe kahjustused Teadmata: Avaskulaarne nekroos / puusa nekroos
Teadmata: Laste kasvupeetus
04.9 Üleannustamine
05.0 FARMAKOLOOGILISED OMADUSED
05.1 Farmakodünaamilised omadused
(Parimad vastusmäärad) Glivec n = 553 IFN + Ara-C n = 553 Hematoloogiline reaktsioon REC n (%) 534(96,6%)* 313 (56,6%)* [95% CI] [94,7%, 97,9%] [52,4%, 60,8%] Tsütogeneetiline vastus Peamine vastus n (%) 490 (88,6%)* 129 (23,3%)* [95% CI] [85,7%, 91,1%] [19,9%, 27,1%] Täielik CyR n (%) 456 (82,5%)* 64 (11,6%)* Osaline CyR n (%) 34 (6,1%) 65 (11,8%) Molekulaarne reaktsioon ** Suur vastus 12 kuu pärast (%) 153/305=50,2% 8/83=9,6% Suur vastus 24 kuu pärast (%) 73/104=70,2% 3/12=25%
Suur vastus 84 kuu pärast (%) 102/116=87,9% 3/4=75% Uuring 0110 37 kuu andmed Krooniline faas, IFN ebaõnnestumine (n = 532) Uuringu 0109 andmed 40,5 kuu pärast Kiirendatud faas (n = 235) Uuring 0102 38 kuu andmed Müeloidne lööklaine (n = 260) % patsientidest (95% CI) Hematoloogiline reaktsioon 1 95% (92,3-96,3) 71% (65,3-77,2) 31% (25,2-36,8) Täielik hematoloogiline reaktsioon (REC) 95% 42% 8% Puuduvad tõendid leukeemia (NEL) kohta Ei ole asjakohane 12% 5% Tagasi kroonilisse faasi (RFC) Ei ole asjakohane 17% 18% Peamine tsütogeneetiline reaktsioon 2 65% (61,2-69,5) 28% (22,0-33,9) 15% (11,2-20,4) Täielik 53% 20% 7% (Kinnitatud3) [95% CI] (43%) [38,6-47,2] (16%) [11,3-21,01] (2%) [0,6-4,4] Osaline 12% 7% 8% 1 Hematoloogilise ravivastuse kriteeriumid (kõik vastused tuleb kinnitada ≥ 4 nädala pärast): REC Studio 0110 [WBC NEL Samad kriteeriumid nagu REC, kuid ANC ≥ 1 x 109 / l ja trombotsüüdid ≥ 20 x 109 / l (ainult 0102 ja 0109) Põrna ja maksa RFC (ainult 0102 ja 0109). MO = luuüdi, SP = perifeerne veri 2 Tsütogeneetilise ravivastuse kriteeriumid: Asjakohane vastus ühendab nii täielikud kui ka osalised vastused: täielik (0% P Ph + metafaasid), osaline (1–35%).
3 Täielik tsütogeneetiline vastus, mida kinnitab teine luuüdi tsütogeneetiline uuring, mis viiakse läbi vähemalt kord kuus pärast esialgset luuüdi uuringut. Uuring ADE10 Eeltöötlus DEX 10 mg / m2 suu kaudu, päevad 1-5; CP 200 mg / m2 i.v., päevad 3, 4, 5; MTX 12 mg intratekaalselt, 1. päev Induktsioon DEX 10 mg / m2 suu kaudu, päevad 6-7, 13-16; VCR 1 mg i.v., päevad 7, 14; IDA 8 mg / m2 i.v. (0,5 h), päevad 7, 8, 14, 15; CP 500 mg / m2 i.v. (1 h) 1. päev; Ara-C 60 mg / m2 i.v., päevadel 22-25, 29-32 Konsolideerimine I, III, V MTX 500 mg / m2 i.v. (24 h), päevad 1, 15; 6-MP 25 mg / m2 suu kaudu, päevadel 1-20 Konsolideerimine II, IV Ara-C 75 mg / m2 i.v. (1 h), päevad 1-5; VM & SUP2; 6 60 mg / m2 i.v. (1 h), päevad 1–5 Uuring AAU02 Induktsioon (de novo Ph + ALL) Daunorubitsiin 30 mg / m2 i.v., päevad 1-3, 15-16; Videomaki koguannus 2 mg i.v., päevadel 1, 8, 15, 22; CP 750 mg / m2 i.v., päevad 1, 8; Prednisoon 60 mg / m2 suu kaudu, päevad 1-7, 15-21; IDA 9 mg / m2 suu kaudu, päevad 1-28; MTX 15 mg intratekaalselt, päevad 1, 8, 15, 22; Ara-C 40 mg intratekaalselt, päevadel 1, 8, 15, 22; Metüülprednisoloon 40 mg intratekaalselt, päevadel 1, 8, 15, 22 Konsolideerimine (de novo Ph + ALL) Ara-C 1000 mg / m2 / 12 h i.v. (3 h), päevad 1-4; Mitoksantroon 10 mg / m2 i.v. 3-5 päeva; MTX 15 mg intratekaalselt, 1. päev; Metüülprednisoloon 40 mg intratekaalselt, 1. päev Uuring ADE04 Eeltöötlus DEX 10 mg / m2 suu kaudu, päevad 1-5; CP 200 mg / m2 i.v., päevad 3-5; MTX 15 mg intratekaalselt, 1. päev Induktsioon I DEX 10 mg / m2 suu kaudu, päevad 1-5; VCR 2 mg i.v., päevad 6, 13, 20; Daunorubitsiin 45 mg / m2 i.v., päevad 6-7, 13-14 Induktsioon II CP 1 g / m2 i.v. (1 h), päevad 26, 46; Ara-C 75 mg / m2 i.v. (1 h), päevad 28-31, 35-38, 42-45; 6-MP 60 mg / m2 suu kaudu, päevad 26-46 Konsolideerimine DEX 10 mg / m2 suu kaudu, päevad 1-5; Vindesiin 3 mg / m2 i.v., päev 1; MTX 1,5 g / m2 i.v. (24 h), 1. päev; Etoposiid 250 mg / m2 i.v. (1 h) päeva 4-5; Ara-C 2x 2 g / m2 i.v. (3 h, q 12 h), 5. päev Uuring AJP01 Induktsioon CP 1,2 g / m2 i.v. (3 h), 1. päev; Daunorubitsiin 60 mg / m2 i.v. (1 h), päevad 1-3; Vinkristiin 1,3 mg / m2 i.v., päevadel 1, 8, 15, 21; Prednisoloon 60 mg / m2 / päevas suu kaudu Konsolideerimine Alternatiivne keemiaravi kuur: suure annusega MTX keemiaravi 1 g / m2 i.v. (24 h), 1. päev ja Ara-C 2 g / m2 i.v. (q 12 h), päevad 2-3, 4 tsüklit Hooldus Videomakk 1,3 g / m2 i.v., päev 1; Prednisoloon 60 mg / m2 suu kaudu, päevad 1-5 Uuring AUS01 Induktsioon-konsolideerimine Hyper-CVAD annustamisskeem: CP 300 mg / m2 i.v. (3 h, q 12 h), päevad 1-3; Vinkristiin 2 mg i.v., päevad 4, 11; Doksorubitsiin 50 mg / m2 i.v. (24 h), 4. päev; DEX 40 mg / päevas 1.-4. Ja 11.-14. Päeval vaheldumisi MTX-ga 1 g / m2 i.v. (24 h), 1. päev, Ara-C 1 g / m2 i.v. (2 h, q 12 h), 2-3 päeva (kokku 8 tsüklit) Hooldus VCR 2 mg i.v. üks kord kuus 13 kuud; Prednisoloon 200 mg suu kaudu, 5 päeva kuus 13 kuud Kõik raviskeemid hõlmavad steroidide manustamist kesknärvisüsteemi profülaktikaks.
Ara-C: tsütarabiin; CP: tsüklofosfamiid; DEX: deksametasoon; MTX: metotreksaat; 6-MP: 6-merkaptopuriin; VM & SUP2; 6: teniposiid; Videomakk: vincristina; IDA: idarubitsiin; i.v .: intravenoosne Konsolideerimisplokk 1 (3 nädalat) VP-16 (100 mg / m2 / päevas, IV): päevad 1-5 Ifosfamiid (1,8 g / m2 / päevas, IV): päevad 1-5 MESNA (360 mg / m2 / annus iga 3 tunni järel, x 8 annust päevas, IV): päevad 1-5 G-CSF (5 mcg / kg, SC): päevad 6-15 või kuni ANC> 1500 pärast madalaimat taset Metotreksaat IT (vanusega kohandatud): ON päev 1 Kolmekordne IT -ravi (kohandatud vanusega): 8., 15. päev Konsolideerimisplokk 2 (3 nädalat) Metotreksaat (5 g / m2 24 tundi, IV): 1. päev Leukovoriin (75 mg / m2 36 tunni pärast, IV; 15 mg / m2 IV või PO 6 korda x 6 annust) iii: 2. ja 3. päev Kolmekordne IT -ravi (kohandatud vanusega): 1. päev ARA-C (3 g / m2 / annus q 12 h x 4, IV): 2. ja 3. päev G-CSF (5 mcg / kg, SC): päevad 4-13 või kuni ANC> 1500 pärast madalaimat taset Taaskasutamise plokk 1 (3 nädalat) VCR (1,5 mg / m2 / päevas, IV): 1., 8. ja 15. päev DAUN (45 mg / m2 / päevas boolus, IV): 1. ja 2. päev CPM (250 mg / m2 / annus iga 12 tunni järel x 4 annust, IV): 3. ja 4. päev PEG-ASP (2500 RÜ / m2, IM): 4. päev G-CSF (5 mcg / kg, SC): päevad 5-14 või kuni ANC> 1500 pärast madalaimat Kolmekordne IT -ravi (kohandatud vanusega): 1. ja 15. päev DEX (6 mg / m2 / päevas, PO): päevad 1-7 ja 15-21 Tugevdamise plokk 1 (9 nädalat) Metotreksaat (5 g / m2 24 tundi, IV): 1. ja 15. päev Leukovoriin (75 mg / m2 36 tunni pärast, IV; 15 mg / m2 IV või PO q6h x 6 annust) iii: 2., 3., 16. ja 17. päev Kolmekordne IT -ravi (kohandatud vanusega): 1. ja 22. päev VP-16 (100 mg / m2 / päev, IV): päevad 22-26 CPM (300 mg / m2 / päev, IV): päevad 22-26 MESNA (150 mg / m2 / päevas, IV): päevadel 22–26 G-CSF (5 mcg / kg, SC): päevad 27–36 või kuni ANC> 1500 pärast madalaimat taset ARA-C (3 g / m2, iga 12 tunni järel, IV): päevad 43, 44 L-ASP (6000 ühikut / m2, IM): 44. päev Taaskasutamise plokk 2 (3 nädalat) VCR (1,5 mg / m2 / päevas, IV): 1., 8. ja 15. päev DAUN (45 mg / m2 / päevas boolus, IV): 1. ja 2. päev CPM (250 mg / m2 / annus iga 12 tunni järel x 4 annust, iv): 3. ja 4. päev PEG-ASP (2500 RÜ / m2, IM): 4. päev G-CSF (5 mcg / kg, SC): päevad 5-14 või kuni ANC> 1500 pärast madalaimat Kolmekordne IT -ravi (kohandatud vanusega): 1. ja 15. päev DEX (6 mg / m2 / päevas, PO): päevad 1-7 ja 15-21 Tugevdamise plokk 2 (9 nädalat) Metotreksaat (5 g / m2 24 tundi, IV): 1. ja 15. päev Leukovoriin (75 mg / m2 36 tunni pärast, IV; 15 mg / m2 IV või PO q6h x 6 annust) iii: 2., 3., 16. ja 17. päev Kolmekordne IT -ravi (kohandatud vanusega): 1. ja 22. päev VP-16 (100 mg / m2 / päev, IV): päevad 22-26 CPM (300 mg / m2 / päev, IV): päevad 22-26 MESNA (150 mg / m2 / päevas, IV): päevadel 22–26 G-CSF (5 mcg / kg, SC): päevad 27–36 või kuni ANC> 1500 pärast madalaimat taset ARA-C (3 g / m2, iga 12 tunni järel, IV): päevad 43, 44 L-ASP (6000 ühikut / m2, IM): 44. päev Hooldus (8-nädalased tsüklid) Tsüklid 1-4 MTX (5 g / m2 24 tundi, IV): 1. päev Leukovoriin (75 mg / m2 36 tunni pärast, IV; 15 mg / m2 IV või PO 6 korda x 6 annust) iii: 2. ja 3. päev Kolmekordne IT -ravi (kohandatud vanusega): päevad 1, 29 Videomakk (1,5 mg / m2, IV): päevad 1, 29 DEX (6 mg / m2 / päevas PO): päevad 1-5; 29-33 6-MP (75 mg / m2 / päevas, PO): päevad 8-28 Metotreksaat (20 mg / m2 nädalas, PO): 8., 15., 22. päev VP-16 (100 mg / m2, IV): päevad 29-33 CPM (300 mg / m2, IV): päevad 29-33 IV KUU päevad 29-33 G-CSF (5 mcg / kg, SC): päevad 34-43 Hooldus (8 -nädalased tsüklid) Tsükkel 5 Kraniaalne kiiritus (ainult plokk 5) 12 Gy 8 fraktsioonis kõigile patsientidele, kellel on diagnoosimisel KNS1 ja KNS2 18 Gy 10 fraktsioonis kõigile patsientidele, kellel on diagnoosimisel kesknärvisüsteem VCR (1,5 mg / m2 / päevas, IV): päevad 1, 29 DEX (6 mg / m2 / päevas, PO): päevad 1-5; 29-33 6-MP (75 mg / m2 / ööpäevas, PO): päevad 11–56 (hoidke 6-MP-d päikesekiirguse 6. – 10. Päeval, mis algas 5. tsükli 1. päeval. Alustage 6-MP-ga esimesel päeval pärast tsükli lõppu kraniaalne kiiritus.) Metotreksaat (20 mg / m2 nädalas, PO): päevad 8, 15, 22, 29, 36, 43, 50 Hooldus (8-nädalased tsüklid) Tsüklid 6-12 VCR (1,5 mg / m2 / päevas, IV): päevad 1, 29 DEX (6 mg / m2 / päevas, PO): päevad 1-5; 29-33 6-MP (75 mg / m2 / päevas, PO): päevad 1-56
Metotreksaat (20 mg / m2 nädalas, PO): päevad 1, 8, 15, 22, 29, 36, 43, 50 Parim vastus Kõik annused (n = 147) 400 mg (n = 73) 600 mg (n = 74) n (%) Täielik vastus 1 Osaline vastus 98 Stabiilne haigus 23 Haiguse progresseerumine 18 Ei ole hinnatav 5
Teadmata 2 Riskikriteeriumid Riskiklass % patsientidest Sündmuste arv / nr. patsientidest Üldine riskisuhe (95% CI) * RFS väärtused (%) 12 kuud 24 kuud Glivec vs. platseebo Glivec vs. platseebo Glivec vs. platseebo NIH Bass 29,5 0/86 vs. 2/90 N.S. 100 vs. 98,7 100 vs. 95,5 Vahepealne 25,7 4/75 vs. 6/78 0,59 (0,17; 2,10) 100 vs. 94,8 97,8 vs. 89,5 Pikk 44,8 21/140 vs. 51/127 0,29 (0,18; 0,49) 94,8 vs. 64,0 80,7 vs. 46,6 AFIP Väga madal 20,7 0/52 vs. 2/63 N.S. 100 vs. 98,1 100 vs. 93,0 Bass 25,0 2/70 vs. 0/69 N.S. 100 vs. 100 97,8 vs. 100 Mõõdukas 24,6 2/70 vs. 11/67 0,16 (0,03; 0,70) 97,9 vs. 90,8 97,9 vs. 73.3
Pikk 29,7 16/84 vs. 39/81 0,27 (0,15; 0,48) 98,7 vs. 56.1 79,9 vs. 41,5 RFS 12-kuuline ravigrupp (CI) 36-kuuline ravirühm% (CI) 12 kuud 93,7 (89,2-96,4) 95,9 (91,9-97,9) 24 kuud 75,4 (68,6-81,0) 90,7 (85,6-94,0) 36 kuud 60,1 (52,5-66,9) 86,6 (80,8-90,8) 48 kuud 52,3 (44,0-59,8) 78,3 (70,8-84,1) 60 kuud 47,9 (39,0-56,3) 65,6 (56,1-73,4) Ellujäämine 36 kuud 94,0 (89,5-96,7) 96,3 (92,4-98,2) 48 kuud 87,9 (81,1-92,3) 95,6 (91,2-97,8)
60 kuud 81,7 (73,0-87,8) 92,0 (85,3-95,7)
05.2 "Farmakokineetilised omadused
05.3 Prekliinilised ohutusandmed
06.0 FARMATSEUTILINE TEAVE
06.1 Abiained
06.2 Sobimatus
06.3 Kehtivusaeg
06.4 Säilitamise eritingimused
06.5 Vahetu pakendi olemus ja pakendi sisu
06.6 Kasutamis- ja käsitsemisjuhised
07.0 MÜÜGILOA HOIDJA
08.0 MÜÜGILOA NUMBER
09.0 MÜÜGILOA VÕI UUENDAMISE KUUPÄEV
10.0 TEKSTI LÄBIVAATAMISE KUUPÄEV
11.0 RAADIO -NARKOLOOGIDE TÄIELIKUD SISEMISE KIIRGUSDOSIMETRIA ANDMED
12.0 RAADIO -NARKOOTIKUTE TÄIENDAVAD ÜKSIKASJALIKUD JUHISED AJALISE ETTEVALMISTUSE JA KVALITEEDIKONTROLLI KOHTA