Toimeained: esetimiib
ABSORCOL 10 mg tabletid
Miks Absorcolit kasutatakse? Milleks see mõeldud on?
ABSORCOL on ravim kõrgenenud kolesteroolitaseme vähendamiseks.
ABSORCOL vähendab üldkolesterooli, "halva" kolesterooli (LDL -kolesterooli) ja triglütseriidideks nimetatud rasvade taset veres. ABSORCOL suurendab ka "hea" kolesterooli (HDL -kolesterool) taset.
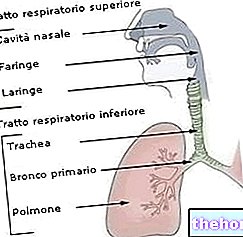
ABSORCOLi toimeaine esetimiib vähendab kolesterooli imendumist soolest.
ABSORCOLi põhjustatud kolesteroolitaseme langus on lisaks statiinidele (ravimite rühm, mis vähendab organismi enda kolesterooli tootmist). Kolesterool on üks paljudest vereringes leiduvatest rasvadest.
Üldkolesterool koosneb peamiselt LDL- ja HDL -kolesteroolist.
LDL -kolesterooli nimetatakse sageli "halvaks" kolesterooliks, kuna see võib koguneda arterite seintesse ja moodustada naastusid. Aja jooksul võib see naastude kogunemine põhjustada arterite ahenemist. See ahenemine võib aeglustada või blokeerida verevoolu elutähtsatesse organitesse, nagu süda ja aju. See verevoolu blokeerimine võib põhjustada südameataki või insuldi.
HDL -kolesterooli nimetatakse sageli "heaks" kolesterooliks, kuna see aitab vältida halva kolesterooli kogunemist arteritesse ja kaitseb südamehaiguste eest.
Triglütseriidid on veel üks rasvavorm veres, mis võib suurendada südamehaiguste riski.
Seda kasutatakse patsientidel, kes ei suuda oma dieediga kolesteroolitaset alandades oma kolesteroolitaset kontrollida. Selle ravimi võtmise ajal peate järgima kolesterooli alandavat dieeti.
ABSORCOLi kasutatakse teie kolesteroolitaset alandava dieedi lisana, kui teil on:
- vere kolesteroolitaseme tõus (primaarne hüperkolesteroleemia [perekondlik ja mitteperekondlik heterosügoot])
- koos statiiniga, kui teie kolesterool ei ole piisava kontrolli all ainult statiiniga
- üksi, kui statiinravi ei ole sobiv või ei ole talutav
- pärilik haigus (homosügootne perekondlik hüperkolesteroleemia), mis suurendab kolesterooli taset veres. Teile määratakse ka statiin ja teile võidakse määrata muu ravi
- pärilik haigus (homosügootne sitosteroleemia, tuntud ka kui fütosteroleemia) - mis suurendab taimsete steroolide taset veres
. ABSORCOL ei aita teil kaalust alla võtta.
Vastunäidustused Absorcol'i ei tohi kasutada
Ärge võtke ABSORCOL'i, kui:
- kui te olete allergiline (ülitundlik) esetimiibi või selle ravimi mõne koostisosa suhtes (vt lõik 6. Pakendi sisu ja muu teave).
Ärge võtke ABSORCOL'i koos statiiniga, kui:
- teil on praegu maksaprobleemid;
- olete rase või toidate last rinnaga.
Ettevaatusabinõud kasutamisel Mida on vaja teada enne Absorcol'i võtmist
Kui teile määratakse ABSORCOL koos statiiniga, lugege palun selle konkreetse ravimi pakendi infolehte.
Rääkige oma arstile kõigist teie seisunditest, sealhulgas allergiatest.
Enne ravi alustamist ABSORCOL -iga koos statiiniga peab arst määrama vereanalüüsi. Selle eesmärk on kontrollida, kuidas tema maks töötab.
Arst võib paluda teil teha vereanalüüse, et kontrollida teie maksa tööd pärast ABSORCOLi võtmist koos statiiniga.
Kui teil on mõõdukad või rasked maksaprobleemid, ei ole ABSORCOLi kasutamine soovitatav.
ABSORCOLi ohutus ja efektiivsus koos mõnede kolesterooli alandavate ravimite, fibraatidega, ei ole tõestatud.
Lapsed
ABSORCOLi ei soovitata alla 10 -aastastele lastele.
Koostoimed Millised ravimid või toidud võivad muuta Absorcol'i toimet
Teatage oma arstile või apteekrile, kui te kasutate või olete hiljuti kasutanud mingeid muid ravimeid, isegi ilma retseptita ostetud.
Eelkõige rääkige oma arstile, kui te võtate ravimeid koos järgmiste toimeainetega:
- tsüklosporiin (kasutatakse sageli elundisiirdamisega patsientidel)
- ravimid, mille toimeaine takistab vere hüübimist, nagu varfariin, fenprokumoon, atsenokumarool või fluindioon (antikoagulandid)
- kolestüramiin (kasutatakse ka kolesterooli alandamiseks), kuna see muudab ABSORCOLi efektiivsust
- fibraadid (kasutatakse ka kolesterooli alandamiseks).
Hoiatused Oluline on teada, et:
Rasedus ja imetamine
Ärge võtke ABSORCOL'i koos statiiniga, kui olete rase, proovite rasestuda või kui arvate end olevat rase. Kui rasestute, kui võtate ABSORCOLi koos statiiniga, peate mõlemad ravimid kohe lõpetama ja pöörduma oma arsti poole. Puuduvad kogemused ABSORCOLi kasutamise kohta raseduse ajal ilma statiinita. Kui olete rase, küsige enne ABSORCOLi kasutamist nõu oma arstilt.
Ärge võtke ABSORCOL'i koos statiiniga, kui toidate last rinnaga, sest ei ole teada, kas need kaks ravimit erituvad rinnapiima. ABSORCOLi ei tohi imetamise ajal kasutada isegi siis, kui seda võetakse iseseisvalt ilma statiinita. Küsige oma arstilt asjakohaseid soovitusi.
Enne mis tahes ravimi kasutamist pidage nõu oma arsti või apteekriga.
Autojuhtimine ja masinatega töötamine
ABSORCOL ei mõjuta autojuhtimise ega masinate käsitsemise võimet. Siiski tuleb arvestada, et mõnedel inimestel võib pärast ABSORCOLi võtmist tekkida pearinglus.
ABSORCOL sisaldab laktoosi
ABSORCOL tabletid sisaldavad suhkrut, mida nimetatakse laktoosiks.
Kui arst on teile öelnud, et te ei talu teatud suhkruid, võtke enne selle ravimi kasutamist ühendust oma arstiga.
Annus, manustamisviis ja aeg Kuidas Absorcol'i kasutada: Annustamine
Võtke ABSORCOLi alati täpselt nii, nagu arst on teile rääkinud.
Jätkake teiste kolesterooli alandavate ravimite võtmist, välja arvatud juhul, kui arst on käskinud nende kasutamise lõpetada. Kui te pole milleski kindel, pidage nõu oma arsti või apteekriga.
- Enne ABSORCOLi võtmist peate järgima kolesterooli alandavat dieeti.
- ABSORCOLi võtmise ajal peate jätkama selle kolesterooli alandava dieedi järgimist.
Täiskasvanud, noorukid ja lapsed (vanuses 10 kuni 17 aastat): Annus on üks 10 mg ABSORCOLi tablett üks kord ööpäevas suu kaudu.
Võite võtta ABSORCOLi igal ajal ja sõltumata söögikordadest.
Kui arst on teile määranud ABSORCOLi koos statiiniga, võib neid kahte ravimit võtta korraga. Sel juhul lugege palun ka teiste retseptiravimite pakendi infolehel sisalduvaid konkreetseid annustamisjuhiseid.
Kui teie arst on teile määranud ABSORCOLi koos mõne teise kolesterooli alandava ravimiga, mis sisaldab toimeainena kolestüramiini või mõnda muud sapi sekvestrante sisaldavat ravimit, peate te võtma ABSORCOLi vähemalt 2 tundi enne või 4 tundi pärast sapi siduva aine võtmist.
Kui te unustate ABSORCOLi võtta
Ärge võtke kahekordset annust; jätkake tavalise annusega järgmisel päeval tavalisel ajal.
Kui teil on lisaküsimusi selle ravimi kasutamise kohta, pidage nõu oma arsti või apteekriga.
Üleannustamine Mida teha, kui olete võtnud liiga palju Absorcol'i?
Võtke ühendust oma arsti või apteekriga.
Kõrvaltoimed Mis on Absorcol'i kõrvaltoimed
Nagu kõik ravimid, võib ka ABSORCOL põhjustada kõrvaltoimeid, kuigi kõigil neid ei teki.
Järgmisi termineid kasutatakse kirjeldamaks, kui sageli on teatatud kõrvaltoimetest:
Väga sage (võib esineda rohkem kui 1 patsiendil 10 -st) • Sage (võib esineda kuni 1 patsiendil 10 -st) • Aeg -ajalt (võib esineda kuni 1 patsiendil 100 -st) Harv (võib esineda kuni 1 patsiendil 1000 -st) • Väga harv (võib esineda kuni 1 patsiendil 10 000 -st, sealhulgas üksikjuhtudel)
Võtke viivitamatult ühendust oma arstiga, kui teil tekib seletamatu lihasvalu, lihaste hellus või nõrkus. Seda seetõttu, et harvadel juhtudel võivad lihasprobleemid, sealhulgas lihaskoe vigastus, mis põhjustab neerukahjustusi, olla tõsised ja potentsiaalselt eluohtlikud.
Ravimi tavalisel kasutamisel on teatatud allergilistest reaktsioonidest, sealhulgas näo, huulte, keele ja / või kõri turse, mis võib põhjustada hingamis- või neelamisraskusi (mis nõuab kohest ravi).
Üksinda kasutamisel on teatatud järgmistest kõrvaltoimetest:
- Sage: kõhuvalu; kõhulahtisus; kõhupuhitus; väsimustunne.
- Aeg -ajalt: mõnede maksa laboratoorsete analüüside (transaminaaside) või lihaste funktsiooni (CK) suurenemine; köha; seedehäired; kõhuvalu; iiveldus; liigesevalu; lihasspasmid; kaelavalu; söögiisu vähenemine; valu; valu rinnus; kuumahood, kõrge vererõhk.
Lisaks on ravimi koos statiiniga kasutamisel teatatud järgmistest kõrvaltoimetest:
- Sage: maksafunktsiooni (transaminaaside) mõnede laboratoorsete testide tõus; peavalu; lihasvalu; lihaste hellus või nõrkus.
- Aeg -ajalt: kipitustunne; kuiv suu; sügelema; lööve; urtikaaria; seljavalu; lihaste nõrkus; valu kätes ja jalgades; ebatavaline väsimus või nõrkus; turse, eriti kätes ja jalgades.
Koos fenofibraadiga kasutamisel on teatatud järgmistest sagedastest kõrvaltoimetest: kõhuvalu.
Lisaks on ravimi üldisel kasutamisel teatatud järgmistest kõrvaltoimetest: pearinglus; lihasvalu; maksaprobleemid; allergilised reaktsioonid, sealhulgas lööve ja nõgestõbi; punetav lööve, mõnikord koos sihtkujuliste kahjustustega (multiformne erüteem); lihasvalu, lihaste hellus või nõrkus; lihaskoe vigastus; sapipõie kivid või sapipõie põletik (mis võib põhjustada kõhuvalu, iiveldust, oksendamist); kõhunäärmepõletik, millega sageli kaasneb tugev kõhuvalu; kõhukinnisus; vererakkude arvu vähenemine, mis võib põhjustada verevalumeid / verejooks (trombotsütopeenia); kipitustunne; depressioon; ebatavaline väsimus või nõrkus; õhupuudus.
Kui teil tekib ükskõik milline kõrvaltoime, pidage nõu oma arsti või apteekriga, sealhulgas selles infolehes loetlemata.
Aegumine ja säilitamine
Hoidke seda ravimit laste eest varjatud ja kättesaamatus kohas.
Ärge kasutage seda ravimit pärast kõlblikkusaega, mis on märgitud karbil või pakendil pärast „EXP“. Kõlblikkusaeg viitab selle kuu viimasele päevale.
Ärge hoidke ABSORCOLi temperatuuril üle 30 ° C.
Blistrid: Hoida originaalpakendis.
Pudelid: hoidke pudel tihedalt suletuna. Need meetmed aitavad kaitsta ravimit niiskuse eest.
Ärge visake ravimeid kanalisatsiooni ega olmejäätmete hulka. Küsige oma apteekrilt, kuidas visata ära ravimeid, mida te enam ei kasuta. See aitab kaitsta keskkonda.
Muu info
Mis ABSORCOL
- Toimeaine on esetimiib .Üks tablett sisaldab 10 mg esetimiibi.
- Abiained: laktoosmonohüdraat, mikrokristalne tselluloos, povidoon, naatriumkroskarmelloos, naatriumlaurüülsulfaat, magneesiumstearaat.
Kuidas ABSORCOL välja näeb ja pakendi sisu
ABSORCOL tabletid on valged või valkjad kapslikujulised tabletid, mille ühele küljele on pressitud "414".
Pakend:
- 7, 10, 14, 20, 28, 30, 50, 98, 100 või 300 tabletti lahtikäivates blisterpakendites või ühekordse annusega blistrites, millel on laminaadi tõstmine;
- 84 või 90 tabletti lahtikäivas blistris;
- 50, 100 või 300 tabletti lahtikäivas blistris annuseühiku kohta;
- 100 tabletti pudelites.
Kõik pakendi suurused ei pruugi olla müügil.
Allika pakendi infoleht: AIFA (Itaalia ravimiamet). Sisu avaldati jaanuaris 2016. Esitatud teave ei pruugi olla ajakohane.
Kõige ajakohasemale versioonile juurdepääsu saamiseks on soovitatav külastada AIFA (Itaalia ravimiamet) veebisaiti. Vastutusest loobumine ja kasulik teave.
01.0 RAVIMPREPARAADI NIMETUS
ABSORCOL 10 MG TABLETID
02.0 KVALITATIIVNE JA KVANTITATIIVNE KOOSTIS
Üks tablett sisaldab 10 mg esetimiibi. Abiaine (d):
Üks tablett sisaldab 55 mg laktoosmonohüdraati.
Abiainete täielik loetelu vt lõik 6.1.
03.0 RAVIMVORM
Tahvelarvuti.
Kapslikujulised, valged või valkjad tabletid, paksusega ligikaudu 2,60 mm, mille ühele küljele on pressitud "414".
04.0 KLIINILINE TEAVE
04.1 Näidustused
Primaarne hüperkolesteroleemia
ABSORCOL koos HMG-CoA reduktaasi inhibiitoriga (statiin) on näidustatud dieedi lisana primaarse hüperkolesteroleemiaga (heterosügootne perekondlik ja mitteperekondlik) patsientidele, kellel ei ole piisavat kontrolli ainult statiinidega.
ABSORCOL monoteraapia on näidustatud dieedi lisana esmase hüperkolesteroleemiaga (heterosügootne perekondlik ja mitteperekondlik) patsientidele, kellele statiine peetakse sobimatuks või ei taluta.
Homosügootne perekondlik hüperkolesteroleemia (homosügootne IF)
ABSORCOL koos statiiniga on näidustatud dieedi täiendava ravina homosügootse perekondliku hüperkolesteroleemiaga patsientidel. Patsiendile võidakse rakendada ka täiendavaid terapeutilisi meetmeid (näiteks LDL -aferees).
Homosügootne perekondlik sitosteroleemia (fütosterolemia)
ABSORCOL on näidustatud toidulisandina homosügootse perekondliku sitosteroleemiaga patsientidel.
ABSORCOLi kasulikku toimet südame -veresoonkonna haigestumusele ja suremusele ei ole veel tõestatud.
04.2 Annustamine ja manustamisviis
Patsient peab järgima piisavat kolesterooli alandavat dieeti ja jätkama dieeti ravi ajal ABSORCOLiga.
Ravimit tuleb manustada suu kaudu. Soovitatav annus on üks 10 mg ABSORCOL tablett üks kord ööpäevas. ABSORCOL'i võib manustada igal ajal, olenemata söögikordadest.
Kui ABSORCOLi lisatakse statiinile, tuleb ravi jätkata konkreetsele statiinile näidatud ühise algannusega või kasutada kõrgemat eelnevalt määratud annust. Sel juhul tuleks tutvuda konkreetse statiini andmelehega.
Samaaegne manustamine sapphappe sekvestrantidega
ABSORCOL tuleb manustada vähemalt 2 tundi enne või vähemalt 4 tundi pärast sapphappe siduva aine manustamist.
Kasutamine eakatel
Eakatel patsientidel ei ole annuse kohandamine vajalik (vt lõik 5.2).
Kasutamine lastel
Ravi alustamine peab toimuma spetsialisti järelevalve all.
Lapsed ja noorukid vanuses ≥10 aastat (puberteedieas: poisid II astme Tanneri staadiumis ja kõrgemad ning tüdrukud, kellel on olnud menstruatsioonijärgne vähemalt üks aasta): annust ei ole vaja kohandada (vt lõik 5.2). Siiski on kliiniline kogemus lastel ja noorukitel (10 ... 17 aastat) piiratud.
Kui ABSORCOLi manustatakse koos statiiniga, tuleb tutvuda statiini annustamisjuhistega lastel.
Lapsed> 6 ja
Lapsed
Kasutamine maksakahjustuse korral
Kerge (Child-Pugh skoor 5 ... 6) maksakahjustuse korral ei ole annuse kohandamine vajalik. Ravi ABSORCOLiga ei ole soovitatav mõõduka (Child-Pugh skoor 7 ... 9) või raske (Child-Pugh skoor> 9) patsientidel, vt lõigud 4.4 ja 5.2).
Kasutamine neerukahjustuse korral
Neerukahjustuse korral ei ole annuse kohandamine vajalik (vt lõik 5.2).
04.3 Vastunäidustused
Ülitundlikkus toimeaine või ravimi ükskõik millise abiaine suhtes.
Kui ABSORCOLi manustatakse koos statiiniga, lugege ravimi tehnilist andmelehte.
Ravi ABSORCOL'iga koos statiiniga on raseduse ja imetamise ajal vastunäidustatud.
ABSORCOL koos statiiniga on vastunäidustatud patsientidele, kellel on aktiivne maksahaigus või püsiv ja määramatu seerumi transaminaaside aktiivsuse tõus.
04.4 Erihoiatused ja asjakohased ettevaatusabinõud kasutamisel
Kui ABSORCOLi manustatakse koos statiiniga, lugege ravimi tehnilist andmelehte.
Maksaensüümid
Kontrollitud kliinilistes uuringutes, kus patsiente raviti ABSORCOLi ja statiiniga, täheldati järjestikuseid transaminaaside taseme tõuse (≥3 korda üle normi ülemise piiri). Kui ABSORCOLi manustatakse koos statiiniga, tuleb ravi alustamisel ja statiini puhul soovitatud maksafunktsiooni testid teha (vt lõik 4.8).
Kontrollitud kliinilises uuringus, kus randomiseeriti üle 9000 kroonilise neeruhaigusega patsiendi saama 10 mg ABSORCOLi kombinatsioonis simvastatiiniga 20 mg ööpäevas (n = 4650) või platseeboga (n = 4620) (keskmine jälgimisperiood 4,9 aastat) oli transaminaaside järjestikuse tõusu (> 3 ULN) esinemissagedus ABSORCOLi ja simvastatiini kombinatsioonis 0,7% ja platseebo puhul 0,6% (vt lõik 4.8).
Skeletilihased
Turuletulekujärgselt on ABSORCOLi kasutamisel teatatud müopaatia ja rabdomüolüüsi juhtudest. Enamik patsiente, kellel tekkis rabdomüolüüs, said samaaegselt ravi ABSORCOLi ja statiiniga. Rabdomüolüüsist teatati aga väga harva ABSORCOLi monoteraapia ja väga harva ABSORCOLi lisamisega muud ained, mis teadaolevalt on seotud suurenenud rabdomüolüüsi riskiga. Kui müopaatiat kahtlustatakse lihasümptomite põhjal või kui seda kinnitavad kreatiinfosfokinaasi (CPK) tasemed, mis on> 10 korda kõrgemad normi ülemisest piirist, võtavad nad ABSORCOLi, statiine ja muid seda tüüpi ravimeid, siis tuleb patsientide samaaegne ravi kohe katkestada Kõiki patsiente, kes alustavad ravi ABSORCOLiga, tuleb teavitada müopaatia riskist ja soovitada viivitamatult teatada mis tahes seletamatust lihasvalust, hellusest või nõrkusest (vt lõik 4.8).
Kliinilises uuringus, milles randomiseeriti üle 9000 kroonilise neeruhaigusega patsiendi saama 10 mg ABSORCOLi kombinatsioonis simvastatiiniga 20 mg ööpäevas (n = 4650) või platseeboga (n = 4620) (keskmine jälgimisperiood 4,9 aastat), Müopaatia / rabdomüolüüsi esinemissagedus oli ABSORCOLi ja simvastatiini kombinatsioonis 0,2% ja platseebo puhul 0,1% (vt lõik 4.8).
Maksapuudulikkus
Kuna mõõduka või raske maksakahjustusega patsientidel on suurenenud esetimiibi ekspositsiooni tundmatu toime, ei ole ABSORCOL soovitatav (vt lõik 5.2).
Lapsed (vanuses 6 kuni 17 aastat)
ABSORCOLi ohutust ja efektiivsust 6 ... 10-aastastel patsientidel, kellel oli heterosügootne või harjumatu perekondlik hüperkolesteroleemia, hinnati 12-nädalases platseebokontrollitud kliinilises uuringus. Esetimiibi toimet> 12-aastastele raviperioodidele ei ole uuritud. nädalat (vt lõigud 4.2, 4.8, 5.1 ja 5.2).
ABSORCOLi ei ole uuritud alla 6 -aastastel patsientidel (vt lõigud 4.2 ja 4.8).
ABSORCOLi ja simvastatiini samaaegse manustamise ohutust ja efektiivsust 10–17-aastastel patsientidel, kellel oli heterosügootne perekondlik hüperkolesteroleemia, hinnati kontrollitud kliinilises uuringus noorukitel (Tanneri II ja kõrgemad staadiumid) ja tüdrukutel vähemalt pärast menstruatsiooni. aasta.
Selles piiratud kontrollitud uuringus ei avaldanud noorukite poiste või tüdrukute seksuaalsele kasvule ega küpsemisele üldist mõju ega tüdrukute menstruaaltsükli pikkusele mingit mõju. Siiski ei ole uuritud esetimiibi mõju üle 33 -nädalase raviperioodi kasvule või suguküpsusele (vt lõigud 4.2 ja 4.8).
ABSORCOLi ohutust ja efektiivsust koos manustatavate simvastatiini annustega üle 40 mg ööpäevas ei ole uuritud 10 ... 17-aastastel lastel.
ABSORCOLi ja simvastatiini koosmanustamise ohutust ja efektiivsust ei ole lastel vanuses uuritud
ABSORCOL-ravi pikaajalist efektiivsust haigestumuse ja suremuse vähendamisel täiskasvanueas ei ole uuritud alla 17-aastastel patsientidel.
Kimbud
Fibraatidega manustatava ABSORCOLi ohutust ja efektiivsust ei ole tõestatud.
Kui patsiendil, keda ravitakse ABSORCOLi ja fenofibraadiga, kahtlustatakse sapikivitõbe, on näidustatud sapipõie uuringud ja ravi tuleb katkestada (vt lõigud 4.5 ja 4.8).
Tsüklosporiin
ABSORCOL -ravi alustamisel terapeutilistes tingimustes, sealhulgas tsüklosporiini kasutamisel, tuleb olla ettevaatlik. ABSORCOLi ja tsüklosporiiniga ravitud patsientidel tuleb jälgida tsüklosporiini kontsentratsiooni (vt lõik 4.5).
Antikoagulandid
Kui varfariinile, mõnele teisele kumariini antikoagulandile või fluindioonile lisatakse ABSORCOLi, tuleb asjakohaselt jälgida rahvusvahelist normaliseeritud suhet (INR) (vt lõik 4.5).
Abiained
Patsiendid, kellel esineb harva galaktoosi talumatust, Lappi laktaasi puudulikkust või glükoosi-galaktoosi imendumishäireid, ei tohi seda ravimit võtta.
04.5 Koostoimed teiste ravimitega ja muud koostoimed
Koostoimeuuringuid on läbi viidud ainult täiskasvanutel.
Prekliinilistes uuringutes on näidatud, et esetimiib ei indutseeri ravimite metabolismis osalevaid tsütokroom P450 ensüüme. Esetimiibi ja tsütokroomide P450 1A2, 2D6, 2C8 poolt metaboliseeritavate ravimite vahel ei täheldatud kliiniliselt olulisi farmakokineetilisi koostoimeid.
2C9 ja 3A4 või N-atsetüültransferaasi.
Kliinilistes koostoimeuuringutes ei mõjutanud esetimiib samaaegsel manustamisel dapsooni, dekstrometorfaani, digoksiini, suukaudsete rasestumisvastaste vahendite (etinüülöstradiool ja levonorgestreel), glipisiidi, tolbutamiidi ega midasolaami farmakokineetikat. Tsimetidiin koos esetimiibiga ei mõjutanud esetimiibi biosaadavust.
Antatsiidid : Antatsiidide samaaegne manustamine vähendas esetimiibi imendumist, kuid ei mõjutanud esetimiibi biosaadavust. Seda imendumise vähenemist ei peeta kliiniliselt oluliseks.
Kolestüramiin: Kolestüramiini samaaegne manustamine vähendas kogu esetimiibi (esetimiib + esetimiib-glükuroniid) keskmine kõvera alune pindala (AUC) ligikaudu 55%. See koostoime võib vähendada madala tihedusega lipoproteiinide (LDL-C) kolesterooli (LDL-C) edasist vähenemist, mis on tingitud kolestüramiinile lisamisest (vt lõik 4.2).
Kimbud : Fenofibraadi ja ABSORCOLiga ravitavatel patsientidel peavad arstid kaaluma sapikivitõve ja sapipõie haiguse võimalikku riski (vt lõigud 4.4 ja 4.8).
Kui patsiendil, keda ravitakse ABSORCOLi ja fenofibraadiga, kahtlustatakse sapikivitõbe, on näidustatud sapipõie uuringud ja ravi tuleb katkestada (vt lõik 4.8).
Fenofibraadi või gemfibrosiili samaaegne manustamine suurendas mõõdukalt esetimiibi üldkontsentratsiooni (vastavalt ligikaudu 1,5 ja 1,7 korda).
ABSORCOLi samaaegset manustamist teiste fibraatidega ei ole uuritud.
Fibraadid võivad suurendada kolesterooli eritumist sapiga, põhjustades sapikivitõbe. Loomkatsetes tõstis esetimiib mõnikord sapipõie sapi kolesterooli, kuid mitte kõigil liikidel (vt lõik 5.3). ei saa välistada.
Statiinid : Esetimiibi manustamisel koos atorvastatiini, simvastatiini, pravastatiini, lovastatiini, fluvastatiini või rosuvastatiiniga ei täheldatud kliiniliselt olulisi farmakokineetilisi koostoimeid.
Tsüklosporiin: Uuringus, milles osales kaheksa neerusiirdamisjärgset patsienti kreatiniini kliirensiga> 50 ml / min stabiilsete tsüklosporiiniannuste korral, tõi ABSORCOLi ühekordse 10 mg annuse manustamine kogu esetimiibi keskmine AUC võrreldes terve kontrollrühmaga (n = 17), keda raviti ainult esetimiibiga. Teises uuringus näitas raske neerupuudulikkusega neerutransplantaadiga patsient, kes sai ravi tsüklosporiini ja mitmete teiste ravimitega. kokkupuude esetimiibi koguhulgaga on 12 korda suurem kui ainult esetimiibiga ravitud suhtelistel kontrollidel. Kaheperioodilises ristuva uuringus, milles osales kaksteist tervet isikut, põhjustas 20 mg esetimiibi igapäevane manustamine 8 päeva jooksul koos ühekordse 100 mg tsüklosporiiniannusega 7. päeval tsüklosporiini AUC keskmiselt 15% (vahemikus 10%). vähenemine 51% -ni) võrreldes ühekordse 100 mg tsüklosporiini annusega. Kontrollitud uuringut esetimiibi samaaegse manustamise mõju kohta tsüklosporiini ekspositsioonile neerusiirdamisega patsientidel ei ole läbi viidud. ABSORCOL -ravi alustamisel ravi ajal, sealhulgas tsüklosporiini kasutamisel, tuleb olla ettevaatlik. ABSORCOLi ja tsüklosporiiniga ravitud patsientidel tuleb jälgida tsüklosporiini kontsentratsiooni (vt lõik 4.4).
Antikoagulandid: Esetimiibi (10 mg üks kord päevas) samaaegne manustamine ei mõjutanud märkimisväärselt varfariini biosaadavust ja protrombiini aega uuringus, milles osales kaksteist tervet täiskasvanud meest. Turuletulekujärgselt on aga teatatud rahvusvahelise normaliseeritud suhte (INR) suurenemisest patsientidel, kes olid lisanud varfariinile või fluindioonile ABSORCOLi. Kui varfariinile, teisele kumariini antikoagulandile või fluindioonile lisatakse ABSORCOLi, tuleb INR väärtust piisavalt jälgida (vt lõik 4.4).
04.6 Rasedus ja imetamine
ABSORCOLi ja statiinide samaaegne manustamine on raseduse ja imetamise ajal vastunäidustatud (vt lõik 4.3), vt statiinide spetsiifilist andmelehte.
Rasedus:
ABSORCOLi tohib rasedatele manustada ainult äärmise vajaduse korral. Kliinilised andmed puuduvad.
Toitmisaeg:
ABSORCOLi ei tohi imetamise ajal kasutada. Uuringud rottidega on näidanud, et esetimiib eritub rinnapiima. Ei ole teada, kas esetimiib eritub rinnapiima.
Viljakus:
Esetimiibi toime kohta inimese fertiilsusele puuduvad kliinilised uuringud. Esetimiib ei mõjutanud isaste või emaste rottide viljakust (vt lõik 5.3).
04.7 Mõju autojuhtimise ja masinate käsitsemise võimele
Autojuhtimise ja masinate käsitsemise võime kohta ei ole uuringuid läbi viidud, kuid sõidukite juhtimisel või masinatega töötamisel tuleb arvestada pearingluse esinemisega.
04.8 Kõrvaltoimed
Kliinilised uuringud ja turustamisjärgne kogemus
Kuni 112 nädalat kestnud kliinilistes uuringutes manustati ABSORCOL 10 mg ööpäevas ainuüksi 2396 patsiendile, koos statiiniga 11 308 patsiendile või fenofibraadiga 185 patsiendile. Kõrvaltoimed olid tavaliselt kerged ja mööduvad. Kõrvaltoimete üldine esinemissagedus ABSORCOLi ja platseebo vahel oli sarnane. Samamoodi oli kõrvaltoimete tõttu katkestamise määr ABSORCOLi ja platseebo vahel võrreldav.
ABSORCOL üksinda või kombinatsioonis statiiniga:
Järgmisi kõrvaltoimeid täheldati patsientidel, keda raviti ABSORCOLiga (N = 2396) ja sagedamini kui platseebo (N = 1159) või patsientidel, keda raviti ABSORCOLiga kombinatsioonis statiiniga (N = 11,308) ja esinemissagedus oli suurem kui ainult statiiniga (N = 9,361). Turuletulekujärgsed kõrvaltoimed on tuletatud aruannetest, sealhulgas ABSORCOList, manustatuna üksi või koos statiiniga.
Esinemissagedused on määratletud järgmiselt: väga sage (≥1 / 10); sage (≥1 / 100,
ABSORCOL koos fenofibraadiga: Seedetrakti häired: kõhuvalu (sage).
Mitmekeskuselises topeltpimedas platseebokontrollitud kliinilises uuringus segatüüpi hüperlipideemiaga patsientidel raviti 625 patsienti kuni 12 nädalat ja 576 patsienti kuni 1 aasta. Selles uuringus lõpetas 172 patsienti, keda raviti ABSORCOLi ja fenofibraadiga, 12 -nädalase ravi ning 230 patsienti, keda raviti ABSORCOL -i ja fenofibraadiga (sealhulgas 109, keda raviti esimese 12 nädala jooksul ainult ABSORCOL -iga), lõpetasid üheaastase ravi. Uuringu eesmärk ei olnud võrrelda ravirühmi harvade sündmuste korral. Esinemissagedus (95% CI) kliiniliselt oluliste seerumi transaminaaside taseme tõusu korral (> 3 korda üle normi ülemise piiri, järjest) oli 4,5% ja 2,7% fenofibraadi monoteraapia ja ABSORCOLi manustamisel koos fenofibraadiga, kohandatud vastavalt raviga kokkupuutumisele. Vastav esinemissagedus koletsüstektoomia esinemissagedus oli vastavalt 0,6% ja 1,7% fenofibraadi monoteraapia ja ABSORCOLi kasutamisel koos fenofibraadiga (vt lõigud 4.4 ja 4.5).
Lapsed (vanuses 6 kuni 17 aastat)
Uuringus, mis viidi läbi heterosügootse või harjumatu perekondliku hüperkolesteroleemiaga (n = 138) lastel (vanuses 6 kuni 10 aastat), täheldati ALAT ja / või ASAT taseme tõusu (≥3 korda üle normi ülemise piiri, järjest) 1,1% (1 esetimiibirühma patsientidest võrreldes 0% platseeborühma patsientidega. CPK väärtused ei suurenenud (≥10 korda üle normi ülemise piiri). Müopaatia juhtudest ei teatatud.
Eraldi uuringus noorukitega (vanuses 10 kuni 17 aastat), kellel oli heterosügootne perekondlik hüperkolesteroleemia (n = 248), täheldati ALAT ja / või ASAT taseme tõusu (≥ 3 korda üle normi ülemise piiri, järjest) 3% patsientidest (4 patsienti) ) esetimiibi / simvastatiini rühmas võrreldes 2% patsientidega (2 patsienti) simvastatiini monoteraapia rühmas; CPK väärtuste suurenemise protsent (≥ 10 korda üle normi ülemise piiri) oli vastavalt 2% (2 patsienti) ja 0%. Müopaatia juhtudest ei ole teatatud.
Need uuringud ei sobi haruldaste kõrvaltoimete võrdlemiseks.
Kroonilise neeruhaigusega patsiendid
Südame- ja neerukaitse uuringus (SHARP) (vt lõik 5.1), milles osales üle 9000 patsiendi, keda raviti 10 mg ABSORCOLi ja 20 mg simvastatiini ööpäevase fikseeritud annuse kombinatsiooniga (n = 4650) või platseeboga (n = 4620), ohutusprofiilid olid keskmiselt 4,9-aastase jälgimisperioodi jooksul võrreldavad. Selles uuringus registreeriti ainult tõsiseid kõrvaltoimeid ja katkestusi mis tahes kõrvaltoimete tõttu. Kõrvaltoimete tõttu katkestamise sagedus oli võrreldav (10,4% patsientidel, keda raviti ABSORCOLiga kombinatsioonis simvastatiiniga, 9,8% platseebot saanud patsientidel). Müopaatia / rabdomüolüüsi esinemissagedus oli ABSORCOL -iga kombinatsioonis simvastatiiniga ravitud patsientidel 0,2% ja platseebot saanud patsientidel 0,1%. Transaminaaside taseme tõus (> 3 korda üle normi ülemise piiri) esines 0, 7% -l patsientidest, keda raviti kombinatsioonis ABSORCOL -iga simvastatiiniga võrreldes 0,6% platseeboga ravitud patsientidest. Selles uuringus ei täheldatud statistiliselt olulist suurenemist etteantud kõrvaltoimete, sealhulgas vähi esinemissageduses (9,4% ABSORCOLi kombinatsioonis simvastatiiniga, 9,5% platseebo puhul). ), hepatiit, koletsüstektoomia või sapikivide või pankreatiidi tüsistused.
Diagnostilised uuringud
Monoteraapiaga kontrollitud kliinilistes uuringutes oli kliiniliselt oluliste seerumi transaminaaside (ALAT ja / või AST esinemissagedus oli 1,3% patsientidel, keda raviti ABSORCOLiga kombinatsioonis statiiniga, ja 0,4% patsientidega, keda raviti ainult statiiniga. Kõrgenemine oli üldiselt asümptomaatiline, ei olnud seotud kolestaasiga ja taastus pärast ravi katkestamist või ravi jätkamisel algtasemele (vt lõik 4.4).
Kliinilistes uuringutes teatati CPK väärtustest> 10 X ULN 4 -l 1674 -st (0,2%) patsiendist, keda raviti ainult ABSORCOL -iga, võrreldes 1 -ga 786 -st (0,1%) platseebot saanud patsiendist ja 1 -l 917 -st patsiendist (0,1%) -manustati koos ABSORCOLi ja statiiniga, võrreldes 4 patsiendiga 929 -st (0,4%), keda raviti ainult statiiniga. ABSORCOLiga ei kaasnenud liigset müopaatiat ega rabdomüolüüsi võrreldes selle kontrollrühmaga (platseebo või ainult statiin) (vt lõik 4.4).
04.9 Üleannustamine
Kliinilistes uuringutes taluti esetimiibi 50 mg päevas 15 tervele isikule kuni 14 päeva või 40 mg päevas 18 primaarse hüperkolesteroleemiaga patsiendile kuni 56 päeva jooksul üldiselt hästi. Loomadel ei täheldatud toksilisust pärast esetimiibi ühekordse suukaudse annuse 5000 mg / kg manustamist rottidel ja hiirtel ning 3000 mg / kg koertel.
Teatatud on mõnest ABSORCOLi üleannustamise juhtumist; enamik neist ei olnud seotud ebasoodsate kogemustega. Teatatud kahjulikud kogemused ei olnud tõsised. Üleannustamise korral tuleb kasutada sümptomaatilisi ja toetavaid meetmeid.
05.0 FARMAKOLOOGILISED OMADUSED
05.1 Farmakodünaamilised omadused
Farmakoterapeutiline rühm: muud lipiide modifitseerivad ained. ATC -kood: C10AX09
ABSORCOL on osa uuest lipiidide taset alandavate ainete klassist, mis pärsivad selektiivselt kolesterooli ja sellega seotud taimsete steroolide imendumist soolestikus. ABSORCOL on suukaudne ja sellel on spetsiifiline toimemehhanism, mis erineb teiste kolesterooli alandavate ainete klassidest (nt. : statiinid, sapphappe sekvestrandid [vaigud], fibriinhappe derivaadid ja taimsed stanoolid) Esetimiibi molekulaarne sihtmärk on steroolitransportöör Niemann-Pick C1-like 1 (NPC1L1), mis vastutab kolesterooli ja fütosteroolide omastamise eest soolestikus.
Esetimiib paikneb peensoole harjapiiril ja pärsib kolesterooli imendumist, põhjustades soolestiku kolesterooli imendumist maksa.
Statiinid vähendavad kolesterooli sünteesi maksas ja need erinevad mehhanismid koos vähendavad kolesterooli. Kahenädalases kliinilises uuringus, milles osales 18 hüperkolesteroleemiaga patsienti, pärssis esetimiib platseeboga võrreldes kolesterooli imendumist soolestikus 54%.
Esetimiibi selektiivsuse kolesterooli imendumise pärssimisel tehti rea prekliinilisi uuringuid. Esetimiib pärssis [14C] -kolesterooli imendumist, mõjutamata seejuures triglütseriidide, rasvhapete, sapphapete, progesterooni, etinüülöstradiooli ega rasvlahustuvate A- ja D -vitamiinide imendumist.
Epidemioloogilised uuringud on näidanud, et südame -veresoonkonna haigestumus ja suremus varieeruvad otseselt üldkolesterooli ja LDL -kolesterooli tasemest ning vastupidi HDL -kolesterooli tasemest. ABSORCOLi kasulikku toimet südame -veresoonkonna haigestumusele ja suremusele ei ole veel tõestatud.
KLIINILISED UURINGUD
Kontrollitud kliinilistes uuringutes vähendas ABSORCOL kas eraldi või kombinatsioonis statiiniga oluliselt üld- (C-üld) kolesterooli, madala tihedusega lipoproteiini (LDL-C) kolesterooli, apolipoproteiin B (Apo B) ja triglütseriidide (TG) taset ning suurendas kõrge tihedusega lipoproteiinide (HDL-C) kolesterool hüperkolesteroleemiaga patsientidel.
Primaarne hüperkolesteroleemia
8-nädalases topeltpimedas platseebokontrollitud uuringus osales 769 hüperkolesteroleemiaga patsienti, kes said statiinmonoteraapiat ja kellel ei õnnestunud riikliku kolesteroolikasvatusprogrammi (NCEP) kohaselt saavutada LDL-C eesmärki (alates 2, 6 kuni 4,1 mmol / l [100 ... 160 mg / dl] sõltuvalt algtaseme omadustest) randomiseeriti saama 10 mg ABSORCOLi või platseebot lisaks olemasolevale statiinravile.
Statiiniga ravitud patsientide seas, kes ei saavutanud LDL-kolesterooli algtaset (? 82%), saavutas uuringu lõpp-punkti LDL-C eesmärgi oluliselt rohkem patsiente, kes olid randomiseeritud ABSORCOLi uuringusse, võrreldes platseeboga randomiseeritud patsientidega, vastavalt 72%ja 19%. LDL-C sisaldus oli oluliselt erinev (25% ja 4% ABSORCOLi puhul) vs vastavalt platseebo). Lisaks vähendas statiinravile lisatud ABSORCOL oluliselt platseeborühmaga võrreldes üldkolesterooli, Apo B, TG ja HDL-kolesterooli taset.
Statiinravile lisatud ABSORCOL või platseebo vähendasid C-reaktiivse valgu mediaani vastavalt 10% või 0% võrreldes algväärtusega.
Kahel 12-nädalasel, platseebokontrolliga randomiseeritud topeltpimedal 1719 primaarse hüperkolesteroleemiaga patsiendil vähenes 10 mg ABSORCOL-i kogusumma (13%), LDL-kolesterooli (19%), Apo-B (14%) ja TG (8%) ja suurenenud HDL-C (3%) võrreldes platseeboga. Samuti ei mõjutanud ABSORCOL rasvlahustuvate vitamiinide A, D ja E plasmakontsentratsiooni protrombiini aja jooksul ja sarnaselt teiste lipiidide taset alandavate ravimitega ei muuda adrenokortikosteroidide tootmist.
Mitmekeskuselises topeltpimedas kontrollitud kliinilises uuringus (ENHANCE) randomiseeriti 720 heterosügootse perekondliku hüperkolesteroleemiaga patsienti, kes said 10 mg esetimiibi kombinatsioonis 80 mg simvastatiiniga (n = 357) või 80 mg simvastatiiniga (n = 363) aastat. Uuringu esmane eesmärk oli uurida kombineeritud ravi esetimiibi / simvastatiini mõju unearteri tuunika intima ja paksuse (IMT) paksusele võrreldes ainult simvastatiiniga. Selle markeri mõju ei ole veel tõestatud. Surrogaat kardiovaskulaarse haigestumuse ja suremuse puhul.
Esmane tulemusnäitaja, kõigi kuue unearteri segmendi keskmise IMT muutus, ei erinenud kahe ravirühma B-režiimi ultraheli mõõtmiste põhjal oluliselt (p = 0,29). Kui esetimiibi manustati 10 mg kombinatsioonis simvastatiiniga 80 mg või simvastatiiniga 80 mg üksinda, suurenes kaheaastase uuringu kestel intima ja mediaalsete tuunikate paksus vastavalt 0,0111 mm ja 0,0058 mm (esialgse unearteri IMT keskmine väärtus oli Vastavalt 0,68 mm ja 0,69 mm).
Esetimiibi 10 mg kombinatsioonis 80 mg simvastatiiniga vähendas LDL-kolesterooli, üldkolesterooli, Apo B ja TG oluliselt rohkem kui simvastatiin 80 mg. Kahe ravigrupi puhul oli C-HDL-i protsendi tõus sarnane. 10 mg esetimiibi ja 80 mg simvastatiini kombinatsiooniga teatatud kõrvaltoimed olid kooskõlas selle teadaoleva ohutusprofiiliga.
Kliinilised uuringud lastel (vanuses 6 kuni 17 aastat)
Mitmekeskuselises topeltpimedas kontrollitud uuringus osales 138 patsienti (59 poissi ja 79 tüdrukut), vanuses 6 kuni 10 aastat (keskmine vanus 8,3 aastat), kellel oli heterosügootne perekondlik hüperkolesteroleemia (IF heterosügootne) või mitteperekondlikud väärtused LDL-C määrad vahemikus 3,74 kuni 9,92 mmol / l randomiseeriti 12 nädala jooksul 10 mg ABSORCOLi või platseeboga.
12. nädalal vähendas ABSORCOL oluliselt üldkolesterooli (-21% vs. 0%), LDL-kolesterooli (-28% vs. -1%), Apo-B (-22% vs. -1%) ja mitte- HDL-C (-26% vs 0%) võrreldes platseeboga. Tulemused olid TG ja HDL-C kahe ravigrupi vahel sarnased (-6% vs + 8% ja + 2% vs + 1%, vastavalt).
Mitmekeskuselises topeltpimedas kontrollitud uuringus osales 142 poissi (II astme Tanneri staadium ja kõrgem) ja 106 menstruatsioonijärgset tüdrukut vanuses 10 kuni 17 aastat (keskmine vanus 14,2 aastat), kellel oli heterosügootne perekondlik hüperkolesteroleemia (IF heterosügootne) ja algtaseme LDL-C väärtused vahemikus 4,1 kuni 10,4 mmol / l randomiseeriti 10 mg ABSORCOL’i manustamiseks koos simvastatiiniga (10, 20 või 40 mg) või simvastatiiniga (10, 20 või 40 mg) 6 nädala jooksul, absorcooliga ja simvastatiiniga 40 mg koos -manustati või simvastatiini 40 mg üksinda järgmise 27 nädala jooksul ning seejärel absorcooli ja simvastatiini (10 mg, 20 mg või 40 mg) avalikult 20 nädala jooksul.
6. nädalal vähendas ABSORCOL koos simvastatiiniga (kõik annused) oluliselt üldkolesterooli (38% vs 26%), LDL-kolesterooli (49% vs 34%), Apo B (39% vs 27%) ja HDL-C (47% vs 33%) võrreldes ainult simvastatiiniga (kõik annused). TG ja HDL-C kahe ravigrupi tulemused olid sarnased (-17% vs -12% ja + 7% vs + 6%, 33. nädalal olid tulemused kooskõlas 6. nädala tulemustega ning oluliselt rohkem patsiente, kes said ABSORCOLi ja 40 mg simvastatiini (62%), saavutasid ideaalse ravieesmärgi vastavalt NCEP AAP (
ABSORCOLi ohutust ja efektiivsust koos manustatavate simvastatiini annustega üle 40 mg ööpäevas ei ole uuritud 10 ... 17-aastastel lastel. ABSORCOLi ja simvastatiini koosmanustamise ohutust ja efektiivsust ei ole uuritud pediaatrilised patsiendid
Homosügootne perekondlik hüperkolesteroleemia (homosügootne IF)
12-nädalases topeltpimedas randomiseeritud uuringus osales 50 homosügootse IF kliinilise ja / või genotüüpilise diagnoosiga patsienti, keda raviti atorvastatiini või simvastatiiniga (40 mg) koos samaaegse LDL-afereesiga või ilma. ABSORCOL koos atorvastatiiniga (40 või 80 mg) või simvastatiiniga (40 või 80 mg) vähendas LDL-kolesterooli taset märkimisväärselt 15%, võrreldes simvastatiini või atorvastatiini monoteraapia annuse suurendamisega 40-lt 80 mg-le.
Homosügootne sitosterolemia (fütosteroleemia)
8-nädalases topeltpimedas platseebo-kontrollitud uuringus randomiseeriti 37 homosügootse sitosteroleemiaga patsienti, kes said 10 mg ABSORCOLi (n = 30) või platseebot (n = 7). Mõnda patsienti raviti teiste ravimitega (nt statiinid, vaigud). ABSORCOL vähendas oluliselt kahte peamist taimset sterooli, sitosterooli ja kampesterooli, vastavalt 21% ja 24% võrreldes algväärtusega. Sitosterooli taseme languse mõju haigestumusele ja suremusele selles populatsioonis ei ole teada.
Suurte vaskulaarsete sündmuste ennetamine kroonilise neeruhaiguse (CKD) korral
Südame- ja neerukaitse uuring (SHARP) oli rahvusvaheline, randomiseeritud, platseebokontrollitud topeltpimeuuring, milles osales 9438 kroonilise neeruhaigusega patsienti, kellest kolmandik oli esialgu dialüüsis. Kokku 4650 patsiendile määrati ABSORCOL 10 mg fikseeritud annuse kombinatsioon 20 mg simvastatiiniga ja 4620 platseeboga ning neid jälgiti keskmiselt 4,9 aastat. Patsientide keskmine vanus oli 62 aastat ja 63% olid meessoost, 72% kaukaasia päritolu, 23% diabeediga ning dialüüsi mitte saanud patsientide keskmine hinnanguline glomerulaarfiltratsiooni kiirus (eGFR) oli 26,5 ml / min / 1,73 m2. lipiididel põhineva uuringu kaasamise kriteerium puudub. Keskmine LDL-kolesterooli algväärtus oli 108 mg / dl. Ühe aasta pärast, sh patsiendid, kes enam uuringuravimeid ei kasutanud, vähenes LDL-kolesterooli sisaldus 26% võrreldes platseeboga 20 mg simvastatiini ja 38% ABSORCOL 10 mg kombinatsioonis simvastatiiniga 20 mg.
SHARPi protokollis täpsustatud esmane võrdlus oli "kavatsus ravida" suurte vaskulaarsete sündmuste "analüüsi (MVE; määratletud kui mittesurmav müokardiinfarkt või südame surm, insult või mis tahes revaskularisatsiooniprotseduur) ainult neil patsientidel, kes olid esialgu randomiseeritud ABSORCOL kombinatsioonis simvastatiiniga (n = 4193) või platseeboga (n = 4191). Sekundaarsed analüüsid hõlmasid sama komposiiti, mida analüüsiti kogu randomiseeritud kohordi kohta (uuringu algväärtus või 1 aasta) koos ABSORCOLiga kombinatsioonis simvastatiiniga (n = 4650) või platseeboga (n = 4620), samuti selle komposiidi komponente.
Esmane tulemusnäitaja analüüs näitas, et ABSORCOL koos simvastatiiniga vähendas märkimisväärselt suurte veresoonkonnahäirete riski (platseeborühmas 749 patsienti vs 639 ABSORCOLi kombinatsioonis simvastatiinigrupiga), suhteline risk vähenes 16% (p = 0,001).
Selle uuringu ülesehitus ei võimaldanud aga ühekomponendilise esetimiibi eraldi panust efektiivsusse, et oluliselt vähendada suurte vaskulaarsete sündmuste riski kroonilise neeruhaigusega patsientidel.
Kõigi randomiseeritud patsientide MVE üksikud komponendid on toodud tabelis 1. ABSORCOL kombinatsioonis simvastatiiniga vähendas oluliselt insuldi ja mis tahes revaskularisatsiooniprotseduuri riski, ilma oluliste arvuliste erinevusteta, mis eelistaks ABSORCOLi ja simvastatiini kombinatsiooni mittefataalse müokardiinfarkti korral ja südame surm.
Tabel 1
Peamised vaskulaarsed sündmused ravirühmade kaupa kõigil SHARPa randomiseeritud patsientidel
a ravi kavatsuse analüüs kõigi SHARP-ga patsientide kohta, kes randomiseeriti ABSORCOLi kombinatsioonis simvastatiini või platseeboga algul või 1 aasta
b MAE; määratletud kui mittesurmav müokardiinfarkt, koronaarsurm, mitteheemorraagiline insult või mis tahes tüüpi revaskularisatsioon
LDL-kolesterooli absoluutne vähenemine, mis saavutati ABSORCOLiga kombinatsioonis simvastatiiniga, oli madalam LDL-C algtasemega patsientide seas (
Aordi stenoos
Simvastatiin ja esetimiib aordi stenoosi raviks (SEAS) oli mitmekeskuseline, topeltpime, platseebokontrollitud uuring, mille kestus oli keskmiselt 4,4 aastat 1873 asümptomaatilise aordi stenoosiga (AS) patsiendil, mis oli dokumenteeritud mõõdetud aordi voolukiiruse järgi Doppleri abil vahemikus 2,5 kuni 4,0 m / s. Registreeriti ainult patsiente, kellele statiinravi ei peetud vajalikuks aterosklerootiliste kardiovaskulaarsete haiguste riski vähendamiseks. Patsiendid randomiseeriti suhtega 1: 1 platseebo või esetimiibi 10 mg ja simvastatiini 40 mg päevas koosmanustamiseks.
Esmane tulemusnäitaja oli suurte kardiovaskulaarsete sündmuste (MCE) kombinatsioon, mis koosnes kardiovaskulaarsest surmast, aordiklapi kirurgilisest asendamisest (AVR), AS progresseerumisest tingitud kongestiivse südamepuudulikkusega (CHF), mittefataalse müokardiinfarktiga, koronaararteri šunteerimisega (CABG) ), perkutaanne koronaarne sekkumine (PCI), haiglaravi ebastabiilse stenokardia ja mittehemorraagilise insuldi tõttu. Peamised sekundaarsed tulemusnäitajad olid esmase tulemusnäitaja sündmuste kategooriate alamhulgad.
Võrreldes platseeboga ei vähendanud esetimiib / simvastatiin 10/40 mg MCE riski oluliselt. Esmane tulemus ilmnes 333 patsiendil (35,3%) esetimiibi / simvastatiini rühmas ja 355 patsiendil (38,2%) platseeborühmas (riskisuhe esetimiibi / simvastatiini rühmas 0,96; usaldusvahemik 95%, 0,83 ... 1,12). p = 0,59) Aordiklapi asendamine teostati 267 patsiendil (28,3%) esetimiibi / simvastatiini rühmas ja 278 patsiendil (29,9%) platseeborühmas (riskisuhe 1,00; 95%CI, 0,84 ... 1,18; p = 0,97) Esetimiibi / simvastatiini rühmas esines vähem isheemilisi kardiovaskulaarseid sündmusi (n = 148) võrreldes platseeborühmaga (n = 187) (riskisuhe, 0,78; 95% CI, 0,63 ... 0,97; p = 0,02), peamiselt väiksemale arvule patsientidele olid nad läbinud koronaararterite šunteerimise.
Vähk esines sagedamini esetimiibi / simvastatiini rühmas (105 versus 70, p = 0,01). Selle tähelepaneku kliiniline tähtsus on ebakindel, sest suuremas SHARP uuringus ei erinenud igat liiki vähijuhtumitega patsientide koguarv (esetimiibi / simvastatiini rühmas 438 versus 439 platseeborühmas) ja seetõttu oli SEAS uuringu tulemus erinev. ei ole erinev. kinnitas SHARP.
05.2 Farmakokineetilised omadused
Imendumine: Pärast suukaudset manustamist imendub esetimiib kiiresti ja konjugeeritakse ulatuslikult farmakoloogiliselt aktiivse fenoolglükuroniidiga (esetimiib-glükuroniid). Esetimiib-glükuroniidi keskmine plasmakontsentratsioon (Cmax) täheldatakse 1-2 tunni jooksul ja esetimiibi puhul 4 ... 12 tunni jooksul esetimiibi biosaadavust ei saa määrata, kuna ühend on süstimiseks sobivas vesikeskkonnas praktiliselt lahustumatu.
Samaaegne toidu manustamine (kõrge rasvasisaldusega või rasvata toidud) ei mõjutanud esetimiibi suukaudset biosaadavust, kui seda manustati ABSORCOL 10 mg tablettidena. ABSORCOL'i võib manustada koos toiduga või ilma.
Levitamine : Esetimiib ja esetimiib-glükuroniid seonduvad vastavalt 99,7% ja 88-92% inimese plasmavalkudega.
Biotransformatsioon: Esetimiib metaboliseerub peamiselt peensooles ja maksas glükuroniidkonjugatsiooni (II faasi reaktsioon) kaudu, seejärel eritub sapiga. Kõigil hinnatud liikidel täheldati minimaalset oksüdatiivset metabolismi (I faasi reaktsioon). Esetimiib ja esetimiib-glükuroniid on peamised ravimitest pärinevad ühendid, mida leidub plasmas, moodustades ligikaudu 10–20% ja 80–90% plasmas leiduvast ravimist vastavalt. Nii esetimiib kui ka esetimiib-glükuroniid eemaldatakse plasmast aeglaselt, näidates märkimisväärset enterohepaatilist tsüklit. Esetimiibi ja esetimiib-glükuroniidi poolväärtusaeg on ligikaudu 22 tundi.
Elimineerimine : Pärast 14C esetimiibi (20 mg) suukaudset manustamist inimestele moodustas esetimiib kokku ligikaudu 93% kogu plasma radioaktiivsusest. Ligikaudu 78% ja 11% manustatud radioaktiivsusest leiti väljaheites ja uriinis vastavalt 10-päevase proovivõtuperioodi jooksul. 48 tunni pärast ei leitud plasmas radioaktiivsust.
Spetsiaalsed populatsioonid :
Pediaatrilised patsiendid
Esetimiibi farmakokineetika on ≥ 6 -aastastel lastel ja täiskasvanutel sarnane. Farmakokineetilised andmed lastel
Eakad patsiendid
Esetimiibi üldkontsentratsioon plasmas on eakatel (≥ 65-aastased) ligikaudu kaks korda kõrgem kui noortel (18–45-aastased). LDL-kolesterooli taseme langus ja ohutusprofiil on võrreldavad eakate ja nooremate isikutega, keda ravitakse ABSORCOLiga. Seetõttu ei ole annuse kohandamine vajalik on vajalik eakatel.
Maksapuudulikkus
Pärast esetimiibi ühekordse 10 mg annuse manustamist suurenes esetimiibi keskmine AUC kerge maksakahjustusega patsientidel (Child Pugh skoor 5 või 6) ligikaudu 1,7 korda, võrreldes tervete isikutega. Mõõduka maksakahjustusega (Child Pugh skoor 7 ... 9) 14-päevase mitmekordse annuse (10 mg / päevas) uuringus suurenes esetimiibi keskmine AUC ligikaudu 4 korda päevas 1 ja 14. päeval võrreldes tervete isikutega. Kerge maksakahjustusega patsientidel ei ole annuse kohandamine vajalik. Kuna mõõduka või raske maksakahjustusega patsientidel (Child Pugh skoor> 9) on suurenenud esetimiibi ekspositsiooni tundmatu toime, ei soovitata neil patsientidel ABSORCOL'i kasutada (vt lõik 4.4).
Neerupuudulikkus
Pärast esetimiibi ühekordset 10 mg annust raske neeruhaigusega patsientidel (n = 8; keskmine CrCl ≤30 ml / min / 1,73 m2) suurenes kogu esetimiibi keskmine AUC ligikaudu 1,5 korda võrreldes tervete isikutega (n = 8 9). Seda tulemust ei peeta kliiniliselt oluliseks. Neerukahjustusega patsientidel ei ole annuse kohandamine vajalik.
Selle uuringu täiendaval patsiendil (neeru siirdamise järgselt ja mitme ravimiga, sealhulgas tsüklosporiiniga ravitud patsiendil) oli 12-kordne "kokkupuude" kogu esetimiibiga.
Seks
Esetimiibi üldkontsentratsioon plasmas on naistel veidi suurem (ligikaudu 20%) kui meestel. LDL-kolesterooli taseme langus ja ohutusprofiil on võrreldavad ABSORCOLiga ravitud meeste ja naiste vahel. Seetõttu ei ole annuse kohandamine vajalik soo alusel.
05.3 Prekliinilised ohutusandmed
Esetimiibi kroonilise toksilisuse uuringud loomadel ei tuvastanud sihtorganite toksilist toimet. Koertel, keda raviti neli nädalat esetimiibiga (≥0,03 mg / kg / päevas), suurenes kolesterooli kontsentratsioon tsüstilises sapis 2,5–3,5 korda. Üheaastases uuringus koertega, keda raviti annustega kuni 300 mg / kg päevas, ei täheldatud sapikivitõve ega muude maksa- ja sapiteede toimete esinemissageduse suurenemist. Nende andmete olulisus inimeste jaoks on teadmata. ABSORCOLi terapeutilise kasutamisega seotud litogeense toime riski ei saa välistada.
Esetimiibi ja statiinide samaaegse manustamise uuringutes olid toksilised toimed sisuliselt need, mis tavaliselt olid seotud statiinidega. Mõned toksilised toimed olid tugevamad kui need, mida täheldati ainult statiinravi korral. Selle põhjuseks on farmakokineetilised ja farmakodünaamilised koostoimed samaaegsel manustamisel. Selliseid koostoimeid kliinilistes uuringutes ei esinenud. Müopaatia episoode esines rottidel alles pärast kokkupuudet inimeste terapeutilistest annustest mitu korda suuremate annustega (ligikaudu 20 korda suurem statiinide AUC tasemest ja 500 kuni 2000 korda suurem aktiivsete metaboliitide AUC tasemest).
Esseede seerias in vivo ja in vitro Esetimiib, üksinda manustatuna või koos statiinidega, ei näidanud genotoksilist potentsiaali. Esetimiibi pikaajalised kartsinogeensuse testid olid negatiivsed.
Esetimiib ei mõjutanud isaste või emaste rottide viljakust, ei olnud teratogeenne rottidel ega küülikutel ega mõjutanud sünnieelset ega postnataalset arengut. Esetimiib ületas tiinetel rottidel ja ravitud küülikutel platsentaarbarjääri. Korduvate annustega 1000 mg / kg / päev. Esetimiibi ja statiinide samaaegne manustamine ei olnud rottidel teratogeenne. Tiinetel küülikutel täheldati väikest arvu skeleti deformatsioone (rinna- ja sabalülide sulandumine, sabalülide arvu vähenemine). Esetimiibi manustamisel koos lovastatiiniga on näidatud surmavat toimet embrüole.
06.0 FARMATSEUTILINE TEAVE
06.1 Abiained
Kroskarmelloosnaatrium
Laktoosmonohüdraat
Magneesiumstearaat
Mikrokristalne tselluloos
Povidoon (K29-32)
Naatriumlaurüülsulfaat
06.2 Sobimatus
Ei ole asjakohane.
06.3 Kehtivusaeg
3 aastat.
06.4 Säilitamise eritingimused
Hoida temperatuuril kuni 30 ° C.
Blistrid: Hoida originaalpakendis, et kaitsta ravimit niiskuse eest.
Pudelid: Hoida pudel tihedalt suletuna, et kaitsta ravimit niiskuse eest.
06.5 Vahetu pakendi olemus ja pakendi sisu
Üheannuseline läbipaistev blister polüklorotrifluoroetüleenist / PVC-st, keevitatud alumiinium- / paberi- / polüesterkatte külge, kasutades vinüülvaiku. Tablette saab ekstraheerida alumiinium- / paber- / polüesterfooliumi tõstmisega
Pakendis 7, 10, 14, 20, 28, 30, 50, 98, 100 või 300 tabletti.
Läbipaistev polüklorotrifluoroetüleen / PVC blister, mis on keevitatud alumiiniumkatte külge, kasutades vinüülvaiku. Tabletid saab välja tõmmata, vajutades kilekotti.
Pakendis 7, 10, 14, 20, 28, 30, 50, 84, 90, 98, 100 või 300 tabletti.
Läbipaistev üheannuseline blister polüklorotrifluoroetüleenist / PVC-st, kaetud alumiiniumiga. Tabletid saab välja tõmmata, vajutades kilekotti.
Pakendis 50, 100 või 300 tabletti.
HDPE pudel polüpropüleenist korgiga, mis sisaldab 100 tabletti.
Kõik pakendi suurused ei pruugi olla müügil.
06.6 Kasutamis- ja käsitsemisjuhised
Ei mingeid erijuhiseid.
07.0 MÜÜGILOA HOIDJA
ADDENDA PHARMA Srl, Via Shakespeare, 47
00144 Rooma
Müüa ainulaadne edasimüüja Itaalias:
SIGMA-TAU I.F.R. S.p.A. Pontina kaudu 30 400 km
00040 Pomezia (RM)
08.0 MÜÜGILOA NUMBER
7 tabletti üheannuselistes blisterpakendites PCTFE / PVC / AL / PAPER AIC nr 036018012
10 tabletti üheannuselistes blisterpakendites PCTFE / PVC / AL / PAPER AIC nr 036018024
14 tabletti üheannuselistes blisterpakendites PCTFE / PVC / AL / PAPER AIC nr 036018036
20 tabletti üheannuselistes blisterpakendites PCTFE / PVC / AL / PAPER AIC nr 036018253
28 tabletti üheannuselistes blisterpakendites PCTFE / PVC / AL / PAPER AIC nr 036018048
30 tabletti üheannuselistes blisterpakendites PCTFE / PVC / AL / PAPER AIC nr 036018051
50 tabletti üheannuselistes blisterpakendites PCTFE / PVC / AL / PAPER AIC nr 036018063
98 tabletti üheannuselistes blisterpakendites PCTFE / PVC / AL / PAPER AIC nr 036018075
100 tabletti üheannuselistes blisterpakendites PCTFE / PVC / AL / PAPER AIC nr 036018087
300 tabletti üheannuselistes blisterpakendites PCTFE / PVC / AL / PAPER AIC nr 036018099
7 tabletti PCTFE / PVC / AL AIC blistris nr 036018101
10 tabletti PCTFE / PVC / AL AIC blistris nr 036018113
14 tabletti PCTFE / PVC / AL AIC blistris nr 036018125
20 tabletti PCTFE / PVC / AL AIC blistris nr 036018265
28 tabletti PCTFE / PVC / AL AIC blistris nr 036018137
30 tabletti PCTFE / PVC / AL AIC blistris nr 036018149
50 tabletti PCTFE / PVC / AL AIC blistris nr 036018152
84 tabletti PCTFE / PVC / AL AIC blistris nr 036018238
90 tabletti PCTFE / PVC / AL AIC blistris nr 036018226
98 tabletti PCTFE / PVC / AL AIC blistris nr 036018164
100 tabletti PCTFE / PVC / AL AIC blistris nr 036018176
300 tabletti PCTFE / PVC / AL AIC blistris nr 036018188
50 tabletti üheannuselistes blisterpakendites PCTFE / PVC / AL AIC nr 036018190
100 tabletti üheannuselistes blisterpakendites PCTFE / PVC / AL AIC nr 036018202
300 tabletti üheannuselistes blisterpakendites PCTFE / PVC / AL AIC nr 036018214
100 tabletti HDPE pudelis AIC nr 036018240
09.0 MÜÜGILOA VÕI UUENDAMISE KUUPÄEV
Veebruar 2007