Toimeained: Montelukast
AIRING 4 mg närimistabletid
Pakendisuurused on saadaval pakendisuuruste jaoks:- AIRING 4 mg närimistabletid
- AIRING 5 mg närimistabletid
- AIRING 10 mg õhukese polümeerikattega tabletid
Näidustused Miks kasutatakse õhutamist? Milleks see mõeldud on?
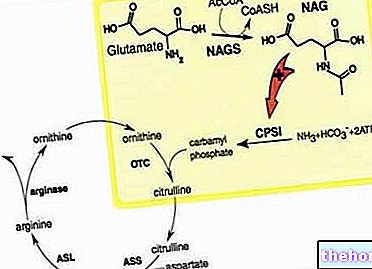
AIRING on leukotrieeni retseptori antagonist, mis blokeerib aineid, mida nimetatakse leukotrieenideks. Leukotrieenid põhjustavad kopsude hingamisteede ahenemist ja paisumist. Blokeerides leukotrieene, parandab AIRING astma sümptomeid ja aitab seda kontrollida.
Arst määras AIRINGi astma raviks, et vältida astma sümptomeid nii päeval kui öösel.
- AIRINGi kasutatakse patsientide raviks, kes ei saa oma ravimite abil piisavalt kontrolli ja vajavad täiendavaid ravimeid.
- AIRING -i võib kasutada ka inhaleeritavate kortikosteroidide alternatiivravina 2 ... 5 -aastastele patsientidele, kes ei ole hiljuti astma raviks suukaudseid kortikosteroide tarvitanud ja kellel on näidatud, et nad ei suuda astma korral sissehingamisel kortikosteroide kasutada.
- AIRING hoiab ära ka treeningust tingitud hingamisteede ahenemise 2-aastastel ja vanematel patsientidel.
Teie arst otsustab, kuidas AIRINGi kasutada, sõltuvalt teie lapse astma sümptomitest ja raskusastmest.
Mis on astma?
Astma on pikaajaline haigus.
Astma hõlmab:
- Hingamisraskused, mis on tingitud hingamisteede ahenemisest. Hingamisteede ahenemine halveneb ja paraneb vastuseks erinevatele tingimustele.
- Hingamisteed, mis reageerivad paljudele ärritavatele stiimulitele, nagu sigaretisuits, õietolm, külm õhk või treening.
- Hingamisteede turse (põletik).
Astma sümptomite hulka kuuluvad: köha, õhupuudus ja survetunne rinnus.
Vastunäidustused õhutamisel ei tohi kasutada
Ärge andke oma lapsele õhutamist, kui ta on allergiline (ülitundlik) montelukasti või AIRINGi mõne koostisosa suhtes (vt 6. LISAINFO).
Ettevaatusabinõud kasutamisel Mida on vaja teada enne õhu võtmist
Rääkige oma arstile kõigist praegustest või varasematest haigustest ja allergiatest.
Olge AIRINGuga eriti ettevaatlik
- kui teie astma või hingamine halveneb, võtke kohe ühendust oma arstiga.
- Suu kaudu õhutamist ei tohi kasutada ägedate astmahoogude raviks.Krampide tekkimisel järgige arsti juhiseid. Hoidke alati kaasas oma lapse erakorralisi inhaleeritavaid astmahoogude ravimeid.
- On oluline, et teie laps võtaks kõiki arsti poolt välja kirjutatud astmaravimeid. AIRINGi ei tohi kasutada teiste astmaravimite asemel, mille arst on teie lapsele määranud.
- Kui teie laps kasutab astmavastaseid ravimeid, peaksite olema teadlik, et kui tal esineb selliseid sümptomeid nagu gripilaadne sündroom, kipitus või puudutus kätes või jalgades, kopsusümptomite süvenemine ja / või punetus nahale, peaksid nad konsulteerima arstiga.
- Ärge võtke atsetüülsalitsüülhapet (aspiriini) ega põletikuvastaseid ravimeid (nimetatakse ka mittesteroidseteks põletikuvastasteks või mittesteroidseteks põletikuvastasteks ravimiteks), kui need halvendavad astmat.
Kasutamine lastel
2–5 -aastastele lastele on saadaval AIRING 4 mg närimistabletid.
6–14 -aastastele lastele on saadaval AIRING 5 mg närimistabletid.
Koostoimed Millised ravimid või toidud võivad muuta õhutamise toimet
Mõned ravimid võivad häirida AIRINGi toimimist või AIRING teiste ravimite toimet.
Rääkige oma arstile, kui teie laps kasutab või on hiljuti kasutanud mingeid muid ravimeid, isegi ilma retseptita.
Rääkige oma arstile, kui teie laps võtab enne AIRING -ravi alustamist järgmisi ravimeid:
- Fenobarbitaal (kasutatakse epilepsia raviks).
- Fenütoiin (kasutatakse epilepsia raviks).
- Rifampitsiin (kasutatakse tuberkuloosi ja mõnede teiste infektsioonide raviks).
AIRING kasutamine koos toidu ja joogiga
AIRING 4 mg närimistablette ei tohi võtta vahetult enne või pärast sööki. Seda tuleb võtta vähemalt 1 tund enne või 2 tundi pärast sööki.
Hoiatused Oluline on teada, et:
Rasedus ja imetamine
See jaotis ei kehti, sest AIRING 4 mg närimistablette tuleb kasutada lastel vanuses 2 kuni 5 aastat. Järgnev teave viitab siiski toimeainele montelukastile.
Kasutamine raseduse ajal
Kui olete rase või soovite rasestuda, peate enne AIRINGi kasutamist nõu pidama oma arstiga. Teie arst otsustab, kas saate sellistel asjaoludel AIRINGi võtta või mitte.
Kasutage rinnaga toitmise ajal
Ei ole teada, kas AIRING võib ilmneda rinnapiima. Kui te toidate last rinnaga või plaanite last rinnaga toita, peate enne AIRINGi kasutamist nõu pidama oma arstiga.
Autojuhtimine ja masinatega töötamine
Mõju autojuhtimise ja masinate käsitsemise võimele ei ole oodata.
Individuaalsed reaktsioonid ravimitele võivad siiski erineda. Mõned kõrvaltoimed (nagu pearinglus ja unisus), millest AIRINGi kasutamisel on teatatud väga harva, võivad mõjutada autojuhtimise ja masinate käsitsemise võimet.
Oluline teave mõningate AIRING koostisainete kohta
AIRING närimistabletid sisaldavad aspartaami, mis on fenüülalaniini allikas. Kui teie lapsel on fenüülketonuuria (harvaesinev pärilik ainevahetushäire), pange tähele, et 4 mg närimistablett sisaldab fenüülalaniini koguses, mis vastab 0,674 mg fenüülalaniinile tableti kohta.
Annustamine, manustamisviis ja aeg Kuidas õhutamist kasutada: Annustamine
- Seda ravimit tuleb lapsele anda täiskasvanu järelevalve all.
- Laps peaks võtma ainult ühe AIRING -tableti päevas, nagu arst on määranud.
- Tablett tuleb võtta ka siis, kui teie lapsel pole sümptomeid või tal on äge astmahoog.
- Võtke AIRING'i alati täpselt nii, nagu arst on teile rääkinud. Kahtluse korral peate konsulteerima oma arsti või apteekriga.
- Võtke tablett suu kaudu.
Lastele vanuses 2 kuni 5 aastat
Üks 4 mg närimistablett, mida tuleb võtta iga päev õhtul. AIRING 4 mg närimistablette ei tohi võtta vahetult enne või pärast sööki. Seda tuleb võtta vähemalt 1 tund enne või 2 tundi pärast sööki.
Kui teie laps kasutab AIRINGi, veenduge, et ta ei võtaks teisi sama toimeainet montelukasti sisaldavaid tooteid.
Kui unustate lapsele õhutamise
Proovige võtta AIRING nii, nagu see oli ette nähtud. Kui aga unustate tableti võtmata, jätkake ravimi võtmist tavalistes annustes. Ärge andke kahekordset annust, kui tablett jäi eelmisel korral võtmata.
Kui teie laps lõpetab AIRING -i võtmise
Ravi AIRINGiga võib astma vastu olla efektiivne ainult siis, kui teie laps jätkab selle võtmist. Oluline on jätkata AIRINGi võtmist seni, kuni arst on seda määranud. See aitab kontrollida teie beebi astmat.
Kui teil on lisaküsimusi AIRINGi kasutamise kohta, pidage nõu oma arsti või apteekriga.
Üleannustamine Mida teha, kui olete võtnud liiga palju õhku
Konsulteerige koheselt oma arstiga. Enamikul üleannustamise juhtudest ei esinenud kõrvaltoimeid. Üleannustamise korral täiskasvanutel ja lastel kõige sagedamini teatatud sümptomiteks on kõhuvalu, unisus, janu, peavalu, oksendamine ja hüperaktiivsus.
Kõrvaltoimed Millised on õhutamise kõrvaltoimed
Nagu kõik ravimid, võib ka AIRING põhjustada kõrvaltoimeid, kuigi kõigil neid ei teki.
Kliinilistes uuringutes montelukasti 4 mg närimistablettidega olid kõige sagedamini teatatud montelukastiga seotud kõrvaltoimed (esinenud vähemalt ühel patsiendil 100 -st ja vähem kui 1 -l 10 -st ravitud lapsest):
- kõhuvalu
- janu
Lisaks teatati kliinilistes uuringutes montelukasti 10 mg õhukese polümeerikattega tablettide ja 5 mg närimistablettidega järgmistest kõrvaltoimetest:
- peavalu
Need kõrvaltoimed olid tavaliselt kerged ja esinesid montelukastiga ravitud patsientidel sagedamini kui platseeboga (tablett, mis ei sisalda ravimit).
Allpool loetletud võimalike kõrvaltoimete esinemissagedus on määratletud järgmiselt:
- Väga sage (esineb vähemalt ühel kasutajal 10 -st)
- Sage (esineb 1 kuni 10 kasutajal 100 -st)
- Aeg -ajalt (esineb 1 kuni 10 kasutajal 1000 -st)
- Harv (esineb 1 kuni 10 kasutajal 10 000 -st)
- Väga harv (esineb vähem kui 1 kasutajal 10 000 -st)
Lisaks on ravimi kaubanduslikul kasutamisel teatatud järgmistest kõrvaltoimetest:
- ülemiste hingamisteede infektsioon (väga sage)
- suurenenud kalduvus veritseda (harv)
- allergilised reaktsioonid, sealhulgas nahalööve, näo, huulte, keele ja / või kõri turse, mis võib põhjustada hingamis- või neelamisraskusi (aeg -ajalt)
- muutused käitumises ja meeleolus [muutunud unenäod, sealhulgas õudusunenäod, unetus, unes kõndimine, ärrituvus, ärevus, rahutus, erutus, sealhulgas agressiivne käitumine või vaenulikkus, depressioon (aeg -ajalt); värin (harv); hallutsinatsioonid, mõtted ja tegevused enesetapp (väga harv) ]
- pearinglus, unisus, kipitus, krambid (aeg -ajalt)
- südamepekslemine (harv)
- ninaverejooks (aeg -ajalt)
- kõhulahtisus, iiveldus, oksendamine (sage); suukuivus, seedehäired (aeg -ajalt)
- hepatiit (maksapõletik) (väga harv)
- verevalumid, sügelus, urtikaaria (aeg -ajalt), nahaaluse koe punane valulik turse, mis paikneb kõige sagedamini jalgade esipinnal (nodoosne erüteem) (väga harv)
- liigese- või lihasvalu, lihaskrambid (aeg -ajalt)
- palavik (sage); väsimus, iiveldus, turse (aeg -ajalt)
Väga harvadel juhtudel on astmaatiliste patsientide Montelukast-ravi ajal teatatud sümptomite kompleksist, nagu gripilaadne vorm, käte või jalgade kipitus või tuimus, kopsusümptomite süvenemine ja / või nahalööve. Churg-Strauss) . Kui ilmneb üks või mitu neist sümptomitest, peab patsient lõpetama ravimi võtmise ja võtma kohe ühendust oma arstiga.
Lisateavet kõrvaltoimete kohta küsige oma arstilt või apteekrilt. Teatage oma arstile või apteekrile kõigist kõrvaltoimetest, mis ei ole ülalpool loetletud või kui sümptomid püsivad või süvenevad.
Kõrvaltoimetest teatamine
Kui teil tekib ükskõik milline kõrvaltoime, pidage nõu oma arsti või apteekriga, sealhulgas selles infolehes loetlemata. Kõrvaltoimetest võite ka ise teavitada riikliku teavitussüsteemi kaudu aadressil www.agenziafarmaco.it/it/responsabili Kõrvaltoimetest teatades saate aidata saada rohkem teavet selle ravimi ohutuse kohta.
Aegumine ja säilitamine
Hoida AIRING laste eest varjatud ja kättesaamatus kohas.
Ärge kasutage AIRINGi pärast kõlblikkusaega, mis on märgitud sildil kuue numbriga sõna EXP järel. Kaks esimest numbrit tähistavad kuud; viimased neli tähistavad aastat. Kõlblikkusaeg viitab kuu viimasele päevale.
Hoida temperatuuril kuni 25 ° C originaalpakendis, valguse ja niiskuse eest kaitstult.
Ravimeid ei tohi ära visata kanalisatsiooni kaudu ega koos majapidamisprügiga. Küsige oma apteekrilt, kuidas visata ära ravimeid, mida te enam ei kasuta. See aitab kaitsta keskkonda.
Muu info
Mida AIRING sisaldab
- Toimeaine on montelukast. Iga tablett sisaldab montelukasti naatriumi, mis vastab 4 mg montelukastile.
- Abiained on: mannitool (E421), mikrokristalne tselluloos, naatriumkroskarmelloos, punane raudoksiid (E172), hüdroksüpropüültselluloos, kirsimaitseaine (sisaldab ka glütserooltriatsetaati (E1518)), aspartaam (E951) ja magneesiumstearaat.
ÕHUTUSE välimuse ja pakendi sisu kirjeldus
Karbis 28 tabletti: 4 blistrit, igas 7 tabletti.
Allika pakendi infoleht: AIFA (Itaalia ravimiamet). Sisu avaldati jaanuaris 2016. Esitatud teave ei pruugi olla ajakohane.
Kõige ajakohasemale versioonile juurdepääsu saamiseks on soovitatav külastada AIFA (Itaalia ravimiamet) veebisaiti. Vastutusest loobumine ja kasulik teave.
01.0 RAVIMPREPARAADI NIMETUS
ÕHUTUS 4 MG
02.0 KVALITATIIVNE JA KVANTITATIIVNE KOOSTIS
Üks närimistablett sisaldab:
Toimeaine: montelukasti naatrium, mis vastab 4 mg montelukastile.
Abiaine: 1,2 mg aspartaami (E951) tableti kohta.
Abiainete täielik loetelu vt lõik "Abiainete loetelu".
03.0 RAVIMVORM
Närimistablett.
Roosa, ümar, kaksikkumer, läbimõõduga 8,5 mm, mille ühele küljele on pressitud "4".
04.0 KLIINILINE TEAVE
04.1 Näidustused
AIRING on näidustatud astma raviks täiendava ravina püsiva kerge / mõõduka astmaga patsientidel, kes ei ole inhaleeritavate kortikosteroididega piisavalt kontrolli all ja kelle lühitoimeline vajadus ei taga astma kliinilist kontrolli.
AIRING võib olla ka alternatiivne ravivõimalus väikeses annuses inhaleeritavatele kortikosteroididele 2 ... 5-aastastele kerge püsiva astmaga patsientidele, kellel pole hiljuti esinenud tõsiseid astmahooge, mis nõuavad suukaudsete kortikosteroidide kasutamist, ja kellel on näidatud, et ei saa kasutada inhaleeritavaid kortikosteroide (vt lõik "Annustamine ja manustamisviis").
AIRING on näidustatud ka astma profülaktikaks alates 2. eluaastast, kus domineerivaks komponendiks on füüsilisest koormusest tingitud bronhide ahenemine.
04.2 Annustamine ja manustamisviis
Seda ravimit tuleb lapsele anda täiskasvanu järelevalve all. Annustamine lastele vanuses 2 kuni 5 aastat on üks 4 mg närimistablett päevas, manustatuna õhtul. Kui AIRINGi võetakse koos toiduga, tuleb see võtta tund enne või kaks tundi pärast sööki. Selles vanuserühmas ei ole annuse kohandamine vajalik. 4 mg närimistablett ei ole soovitatav alla 2 -aastastele lastele.
Üldised soovitused. AIRINGi terapeutiline toime astma kontrolli parameetritele ilmneb ühe päeva jooksul. Soovitage patsiendil jätkata AIRINGi võtmist isegi siis, kui astma on kontrolli all, samuti astma ägenemise perioodidel.
Neerupuudulikkusega või kerge kuni mõõduka maksakahjustusega patsientidel ei ole annuse kohandamine vajalik. Puuduvad andmed raske maksakahjustusega patsientide kohta. Annustamine on mõlemast soost patsientidele sama.
ÕHUTUS püsiva kerge astma korral alternatiivse ravivõimalusena väikeses annuses inhaleeritavatele kortikosteroididele:
Montelukasti kasutamist ei soovitata monoteraapiana mõõduka püsiva astmaga patsientidel. Kerge püsiva astmaga lastele tuleks kaaluda montelukasti kasutamist alternatiivse ravivõimalusena väikeses annuses inhaleeritavate kortikosteroidide puhul. kellel on hiljuti esinenud tõsiseid astmahooge, mis nõuavad suukaudseid kortikosteroide, ja kellel on näidatud, et nad ei saa inhaleeritavaid kortikosteroide kasutada (vt „Näidustused”). Püsiva kerge astma all mõistetakse astma sümptomeid, mis esinevad rohkem kui üks kord nädalas, kuid vähem kui üks kord päevas, ja öiseid sümptomeid, mis esinevad rohkem kui kaks korda kuus, kuid harvem kui kord nädalas. Kopsude funktsioon episoodide vahel on normaalne. Kui jälgimise ajal (tavaliselt ühe kuu jooksul) ei saavutata rahuldavat astma kontrolli, tuleks astma järkjärgulisele ravile tuginedes kaaluda vajadust täiendava või erineva põletikuvastase ravi järele. Patsiente tuleb perioodiliselt kontrollida .
ÕHUTUS astma profülaktikaks 2–5-aastastel patsientidel, kus domineerivaks komponendiks on füüsilisest koormusest tingitud bronhide ahenemine :
2 ... 5-aastastel patsientidel võib füüsilisest koormusest tingitud bronhide ahenemine olla püsiva astma peamine ilming, mis nõuab ravi inhaleeritavate kortikosteroididega. Patsiente tuleb hinnata pärast 2 ... 4-nädalast ravi. Montelukastiga Kui rahuldavat ravivastust ei saavutata, või tuleks kaaluda teistsugust ravi.
ÕHUTUSravi võrreldes teiste astmaravidega:
Kui AIRING-ravi kasutatakse inhaleeritavate kortikosteroidide täiendava ravina, ei tohi AIRING-i järsult asendada inhaleeritavate kortikosteroididega (vt lõik "Hoiatused ja ettevaatusabinõud kasutamisel").
Täiskasvanutele ja 15-aastastele ja vanematele noorukitele on saadaval 10 mg õhukese polümeerikattega tabletid.
6–14 -aastastele patsientidele on saadaval 5 mg närimistabletid.
Manustamisviis
Tablett tuleb närida.
04.3 Vastunäidustused
Ülitundlikkus toimeaine või ravimi ükskõik millise abiaine suhtes.
04.4 Erihoiatused ja asjakohased ettevaatusabinõud kasutamisel
Soovitage patsiendil mitte kasutada suukaudset montelukasti ägedate astmahoogude raviks ja omama käepärast sobivaid erakorralisi ravimeid. Ägeda rünnaku korral tuleb kasutada inhaleeritavat a -adrenergilist agonisti. Juhul kui patsient vajab tavapärasest rohkem inhaleeritavaid agoniste? -Adrenergilisi aineid, peab ta võimalikult kiiresti pöörduma raviarsti poole.
Montelukasti ei tohi järsult asendada inhaleeritavate või suukaudsete kortikosteroididega.
Puuduvad andmed, mis näitaksid, et kortikosteroidide suukaudset annust on võimalik vähendada montelukasti samaaegsel manustamisel.
Harvadel juhtudel võivad astmavastaseid ravimeid, sealhulgas montelukasti, saavatel patsientidel tekkida süsteemne eosinofiilia, mis mõnikord avaldub vaskuliidi kliiniliste tunnustena, mis on sarnased Churg-Straussi sündroomiga, mis on sageli raviga ravitav süsteemne kortikosteroid. Neid juhtumeid on üldiselt, kuid mitte alati, seostatud suukaudse kortikosteroidravi vähendamise või katkestamisega.
Ei saa välistada ega tuvastada võimalust, et leukotrieeni retseptori antagoniste võib seostada Churg-Straussi sündroomi tekkimisega. Arstid peaksid patsiente jälgima eosinofiilia, vaskuliitilise lööbe, kopsu sümptomite süvenemise, südame tüsistuste ja / või neuropaatia suhtes. Neid sümptomeid tekitavaid patsiente tuleb hinnata ja nende raviskeeme uuesti läbi vaadata.
4 mg närimistablettide ohutust ja efektiivsust alla 2 -aastastel lastel ei ole kindlaks tehtud. Seetõttu ei soovitata neid kasutada alla 2 -aastastel lastel.
AIRING sisaldab aspartaami, mis on fenüülalaniini allikas. Fenüülketonuuriaga patsiendid peavad arvestama, et iga 4 mg närimistablett sisaldab fenüülalaniini koguses, mis vastab 0,674 mg annusele.
04.5 Koostoimed teiste ravimitega ja muud koostoimed
Montelukasti võib manustada koos teiste astma profülaktikas ja kroonilises ravis tavaliselt kasutatavate ravimitega. Ravimite koostoime uuringutes ei avaldanud montelukasti soovitatav kliiniline annus kliiniliselt olulist mõju järgmiste ravimite farmakokineetikale: teofülliin, prednisoon, prednisoloon, rasestumisvastased vahendid suukaudne (etinüülöstradiool / noretindroon 35/1), terfenadiin, digoksiin ja varfariin.
Patsientidel, keda manustati koos fenobarbitaaliga, vähenes montelukasti plasmakontsentratsiooni kõvera alune pindala (AUC) ligikaudu 40%. Kuna montelukasti metaboliseerib CYP 3A4, olge montelukasti manustamisel ettevaatlik, eriti lastel. 3A4, nagu fenütoiin, fenobarbitaal ja rifampitsiin.
In vitro uuringud on näidanud, et montelukast on tugev CYP2C8 inhibiitor. Siiski on kliinilise ravimite koostoimeuuringu andmed montelukasti ja rosiglitasooniga (substraat, mida kasutatakse peamiselt CYP2C8 kaudu metaboliseeritavate ravimite tüüpilise testina) näidanud, et montelukast ei inhibeeri CYP2C8 in vivo. Seetõttu ei tohiks montelukast oluliselt muuta selle ensüümi poolt metaboliseeritavate ravimite (nt paklitakseel, rosiglitasoon ja repagliniid) metabolismi.
04.6 Rasedus ja imetamine
Kasutamine raseduse ajal
Loomkatsed ei näita kahjulikku toimet rasedusele ega embrüo -loote arengule.
Raseduse andmebaasides saadaolevad piiratud andmed ei viita põhjusliku seose olemasolule AIRING-i ja väärarengute (jäsemete defektid) vahel, mida turustamisjärgses maailmas on harva teatatud.
AIRINGi võib raseduse ajal kasutada ainult siis, kui seda peetakse hädavajalikuks.
Kasutage rinnaga toitmise ajal
Uuringud rottidega on näidanud, et montelukast eritub rinnapiima (vt lõik "Prekliinilised ohutusandmed"). Ei ole teada, kas montelukast eritub imetavate naiste rinnapiima.
AIRINGi võib rinnaga toitmise ajal kasutada ainult siis, kui seda peetakse hädavajalikuks.
04.7 Mõju autojuhtimise ja masinate käsitsemise võimele
Arvatakse, et montelukast ei mõjuta autojuhtimise ega masinate käsitsemise võimet, kuid väga harvadel juhtudel on mõned inimesed teatanud unisusest või pearinglusest.
04.8 Kõrvaltoimed
Montelukasti on kliinilistes uuringutes hinnatud järgmiselt:
• 10 mg õhukese polümeerikattega tablette ligikaudu 4000 täiskasvanud patsiendile vanuses 15 aastat
• 5 mg närimistablette ligikaudu 1750 lapsel vanuses 6 kuni 14 aastat
• 4 mg närimistablette 851 lapsel vanuses 2 kuni 5 aastat.
Sageli teatati järgmistest ravimiga seotud kõrvaltoimetest (> 1/100, platseebo):
Kui kliinilistes uuringutes jätkati ravi piiratud arvul täiskasvanud patsientidel kuni 2 aastat ja lastel vanuses 6 kuni 14 aastat kuni 12 kuud, ei muutunud ohutusprofiil.
Kumulatiivselt raviti montelukastiga vähemalt 3 kuud 502 last vanuses 2 kuni 5 aastat, 338 patsienti 6 kuud või kauem ja 534 patsienti 12 kuud või kauem. Pikaajalise ravi korral ei muutunud ohutusprofiil isegi nendel patsientidel.
Turustamisjärgne kogemus
Turustamisjärgsest kasutamisest teatatud kõrvaltoimed on loetletud alljärgnevas tabelis, mis põhineb organsüsteemide klassil ja konkreetsete kõrvaltoimete terminoloogial. Esinemissageduse kategooriaid hinnati asjakohaste kliiniliste uuringute põhjal.
04.9 Üleannustamine
Spetsiifiline teave montelukasti üleannustamise ravi kohta puudub. Kroonilise astma uuringutes on montelukasti manustatud täiskasvanud patsientidele annustes kuni 200 mg päevas 22 nädala jooksul ja lühiajalistes uuringutes kuni 900 mg päevas ligikaudu ühe nädala jooksul, ilma kliiniliselt oluliste kõrvaltoimeta.
Turuletulekujärgselt ja montelukastiga läbi viidud kliinilistes uuringutes on teatatud ägedast üleannustamisest. Nende hulgas on teateid täiskasvanutest ja lastest kuni 1000 mg (ligikaudu 61 mg / kg 42-kuusel lapsel) annustes. Täheldatud laboratoorsed tulemused kooskõlas ohutusprofiiliga täiskasvanutel ja lastel. Enamikul üleannustamise juhtudest puudusid kõrvaltoimed. Kõige sagedamini täheldatud kõrvaltoimed olid kooskõlas montelukasti ohutusprofiiliga ja hõlmasid kõhuvalu, unisust, janu, peavalu, oksendamist ja psühhomotoorne hüperaktiivsus.
Ei ole teada, kas montelukast on dialüüsitav peritoneaaldialüüsi või hemodialüüsi teel.
05.0 FARMAKOLOOGILISED OMADUSED
05.1 Farmakodünaamilised omadused
Farmakoterapeutiline rühm: muud süsteemsed ravimid hingamisteede obstruktiivsete haiguste raviks. Leukotrieeni retseptori antagonistid.
ATC -kood: R03D C03.
Tsüsteinüülleukotrieenid (LTC4, LTD4, LTE4) on tugevad põletikulised eikosanoidid, mida vabastavad erinevad rakud, sealhulgas nuumrakud ja eosinofiilid. Need olulised astma vahendajad seonduvad inimestel hingamisteedes leiduvate tsüsteinüül-leukotrieeniretseptoritega (CysLT) ja põhjustavad hingamisteedele mitmesuguseid toimeid, sealhulgas bronhide ahenemist, limaskesta sekretsiooni, veresoonte läbilaskvust ja eosinofiilide värbamist.
Montelukast on suukaudselt aktiivne ühend, mis seondub suure afiinsuse ja selektiivsusega CysLT1 retseptoriga. Kliinilistes uuringutes pärsib montelukast väikestes annustes, näiteks 5 mg, LTD4 sissehingamisel põhjustatud bronhide ahenemist. Bronhide laienemist täheldati kahe tunni jooksul pärast suukaudset manustamist. Beeta-adrenergiliste agonistide põhjustatud bronhodilataatoriefekt lisandus sellele, mida montelukast. Ravi montelukastiga pärssis antigeeniga kokkupuutest tingitud bronhide ahenemise varajast ja hilist staadiumi. Võrreldes platseeboga vähendas montelukast perifeerse vere eosinofiilide arvu nii täiskasvanutel kui lastel. Eraldi uuringus vähendas ravi montelukastiga oluliselt hingamisteede eosinofiile (röga uurimise tulemusena). Täiskasvanutel ja lastel vanuses 2 kuni 14 aastat vähendas montelukast võrreldes platseeboga perifeerse vere eosinofiile, parandades samal ajal astma kliinilist kontrolli.
Täiskasvanutel ja platseeboga läbi viidud uuringutes näidati, et montelukast, 10 mg üks kord ööpäevas, parandab oluliselt FEV1 -d hommikul (muutused võrreldes algväärtusega 10,4% vs 2,7%), hommikust väljahingamise tippvoolu (PEFR) (muutused algväärtusest 24,5 l / min vs. 3,3 l / min) ja vähendab oluliselt a -adrenergiliste agonistide üldist kasutamist (muutused võrreldes algväärtusega -26,1% vs -4,6%). Patsientide poolt öösel ja päeval saadud sümptomite skoor oli oluliselt parem kui platseeborühmas.
Täiskasvanutega läbi viidud uuringutes on näidatud, et montelukastil on kliiniliselt täiendav toime inhaleeritava kortikosteroidi poolt indutseeritud toimele (protsentuaalsed muutused võrreldes inhaleeritava beklometasooni pluss montelukastiga võrreldes beklometasooniga FEV1 korral vastavalt: 5,43% vs 1 04% ja a -adrenergiliste agonistide kasutamine : -8,70% vs 2,64%). Esialgne ravivastus montelukastile osutus kiiremaks kui inhaleeritav beklometasoon (200 mikrogrammi kaks korda päevas, manustatuna vaheseadme kaudu), kuigi beklometasoon andis kogu kaheteistnädalase uuringuperioodi jooksul suurema keskmise toime (muutused FEEL1 -s vastavalt montelukasti ja beklometasooni vahel algväärtusest: 7,49% vs 13,3% ja a -adrenergiliste agonistide kasutamine: -28,28% vs -43,89%). Siiski saavutas "suur osa montelukastiga ravitud patsientidest kliinilise ravivastuse, mis oli sarnane beklometasooniga (nt 50% beklometasooniga ravitud patsientidest saavutas FEV1 paranemise ligikaudu 11% või rohkem kui algtasemel, samas kui ligikaudu 42% montelukastiga ravitud patsientidest saavutas sama ravivastuse).
12-nädalases platseebokontrollitud uuringus 2 ... 5-aastastel lastel parandas montelukast 4 mg üks kord ööpäevas astma kontrolli parameetreid võrreldes platseeboga, olenemata kontrollravi (inhaleeritavate / pihustatud kortikosteroidide või inhaleeritavate / pihustatud naatriumkromoglükaadi) samaaegsest kasutamisest. . Kuuskümmend protsenti patsientidest ei saanud ravi teiste kontrollravidega. Montelukast võrreldes platseeboga parandas päevaseid sümptomeid (sh köha, vilistav hingamine, hingamisraskused ja piiratud motoorne aktiivsus) ja öiseid sümptomeid. Montelukast vähendas platseeboga võrreldes ka "vastavalt vajadusele"? -Agonistide ja kiireloomuliste kortikosteroidide kasutamist astma ägenemise korral. Montelukastravi saanud patsiendid olid astmavabad rohkem kui päevi kui platseebot saanud patsiendid. Ravi andis efekti pärast esimest annust.
12-kuulises platseebokontrollitud uuringus kerge astma ja episoodiliste ägenemistega lastel vanuses 2 kuni 5 aastat vähendas montelukast 4 mg üks kord ööpäevas oluliselt (p <0,001) ägenemiste (EE) iga-aastast sagedust võrreldes platseeboga (1,60 EE vs Vastavalt 2,34 EE), [EE on määratletud kui ≥3 järjestikust päeva, mille päevased sümptomid nõuavad a -antagonistide või kortikosteroidide (suukaudsed või inhaleeritavad) või haiglaravi astma tõttu]. EE aastase määra vähenemine oli 31,9%, 95% CI 16,9, 44,1.
8-nädalases uuringus 6 ... 14-aastastel lastel parandas montelukast 5 mg üks kord ööpäevas võrreldes platseeboga oluliselt hingamisfunktsiooni (muutus FEV1 algväärtusest 8,71% vs 4,16%; muutus algväärtusest AM PEFR -is 27,9 l / min vs 17,8 l / min) ja vähendas vastavalt vajadusele "a -antagonistide kasutamist" (muutus algväärtusest -11,7% vs + 8,2%).
12-kuulises võrdlevas uuringus montelukasti ja inhaleeritava flutikasooni efektiivsuse kohta astma kontrolli all hoidmisel 6–14-aastastel lastel, kellel oli püsiv kerge astma, ei olnud montelukast flutikasoonist halvem, suurendades päevade protsentuaalset osa, ilma et oleks vaja päästeravi ( RFD), esmane tulemusnäitaja. RFD keskmine protsent 12-kuulise raviperioodi jooksul suurenes montelukasti rühmas 61,6-lt 84,0-le ja flutikasoonirühmal 60,9-lt 86,7-le. Erinevus rühmade vahel väikseimate ruutude (LS) keskmine RFD protsendi suurenemine oli statistiliselt oluline (-2,8 95% CI -4,7, -0,9), kuid vahemikus kliinilisest punktist ette nähtud mitte -halvemuse piires vaade.
Nii montelukast kui ka flutikasoon parandasid astma kontrolli ka 12-kuulise raviperioodi jooksul hinnatud sekundaarsete muutujate osas: VEF1 tõusis 1,83-lt 2,09-le montelukasti rühmas ja 1,85-lt 2,14-le. 14 l flutikasoonirühmas. FEV1 rühmade vahel oli -0,02 l, 95% CI -0,06, 0,02. FEV1 oodatava protsendi suurenemine algväärtusest oli montelukastiga ravitud rühmas 0,6% ja flutikasoonrühmas 2,7%. LS keskmiste erinevused FEV1 oodatava protsendi muutuse suhtes algtasemest olid -2,2%, 95% CI -3,6, -0,7. Β -agoniste kasutavate päevade protsent vähenes 38,0 -lt 15,4 -le montelukasti rühmas ja 38,5 -lt 12,8 -le flutikasooni rühmas. Päevade protsentide rühmadevaheline erinevus LS -i keskmistes β-agoniste kasutades oli 2,7, 95% CI 0,9, 4, 5.
Astmahooga patsientide protsent (määratletud kui astma süvenemise periood, mis nõuab ravi steroididega os, plaaniväline arstivisiit, erakorralise meditsiini osakonna visiit või haiglaravi) oli montelukasti rühmas 32,2 ja flutikasoonigrupis 25,6; koefitsient (95% CI) oli 1,38.
Patsientide protsent, kes kasutasid uuringu ajal süsteemseid (peamiselt suukaudseid) kortikosteroide, oli 17,8% montelukasti rühmas ja 10,5% flutikasooni rühmas. LS keskmiste erinevus rühmade vahel oli 7,3%, 95% CI 2,9, 11,7.
Täiskasvanutel läbi viidud 12-nädalases uuringus näidati treeningust tingitud bronhide ahenemise (BIE) olulist vähenemist (FEV1 maksimaalne vähenemine: montelukasti puhul 22,33% vs Platseebo puhul 32,40%; FEV1 taastumisaeg väärtuseni, mis ei erine algväärtusest rohkem kui 5%: 44,22 min vs 60,64 minutit)
See mõju kordus järjekindlalt kogu 12-nädalase uuringu jooksul. BIE vähenemist demonstreeriti ka lühiajalises uuringus 6 ... 14-aastastel lastel (FEV1 maksimaalne vähenemine: 18,27% vs 26,11%; FEV1 taastumisaeg väärtuseni, mis ei erine algväärtusest rohkem kui 5%: 17,76 min vs 27,98 min). Mõlemas uuringus ilmnes toime üks kord ööpäevas manustamisintervalli lõpus.
Aspiriinitundlikel astmahaigetel, kes said samaaegselt inhaleeritavaid ja / või suukaudseid kortikosteroide, parandas montelukastiravi platseeboga võrreldes oluliselt astma kontrolli (FEV1 protsentuaalsed muutused algväärtusest: 8,55% vs -1,74%; a -adrenergiliste agonistide üldkasutuse vähenemine võrreldes algtasemega: -27,78% vs 2,09%).
05.2 Farmakokineetilised omadused
Imendumine
Pärast suukaudset manustamist imendub montelukast kiiresti. 10 mg õhukese polümeerikattega tablettide puhul saavutatakse täiskasvanute maksimaalse plasmakontsentratsiooni (Cmax) keskmine väärtus 3 tundi (Tmax) pärast tühja kõhuga manustamist. Keskmine biosaadavus pärast suukaudset manustamist on 64%. Suukaudne biosaadavus ja Cmax ei mõjuta sööki standard. Ohutust ja efektiivsust on tõestatud kliinilistes uuringutes, kus 10 mg õhukese polümeerikattega tablette manustati sõltumata toiduainete võtmise ajast.
5 mg närimistablettide puhul saavutatakse täiskasvanu Cmax tühja kõhuga pärast 2 -tunnist manustamist. Keskmine biosaadavus pärast suukaudset manustamist on 73% ja väheneb söögi ajal 63% -ni. standard.
Pärast 4 mg närimistableti manustamist 2 ... 5 -aastastele lastele tühja kõhuga saavutatakse Cmax 2 tunniga. Keskmine C on suurem kui 66%, samas kui C min on väiksem kui täiskasvanutel, kes võtavad 10 mg tablette.
Levitamine
Üle 99% montelukastist seondub plasmavalkudega. Montelukasti jaotusruumala stabiilses olekus on keskmiselt 8–11 liitrit. Rottidel tehtud uuringud radiomärgistatud montelukastiga näitavad minimaalset jaotumist vere -aju barjääri vahel. Lisaks leiti, et 24 tundi pärast annuse manustamist on radioaktiivselt märgistatud aine kontsentratsioon kõigis teistes kudedes minimaalne.
Biotransformatsioon
Montelukast metaboliseerub ulatuslikult. Terapeutiliste annustega läbi viidud uuringutes ei leitud montelukasti metaboliitide plasmakontsentratsiooni püsikontsentratsioonis nii täiskasvanutel kui ka lastel.
Haridus in vitro Inimese maksa mikrosoomide kasutamine näitab, et tsütokroomid P450 3A4, 2A6 ja 2C9 osalevad montelukasti metabolismis. Edasiste leidude põhjal in vitro inimese maksa mikrosoomidel ei inhibeeri montelukast terapeutilises plasmakontsentratsioonis tsütokroomide P450 3A4, 2C9, 1A2, 2A6, 2C19 või 2D6 toimet. Metaboliitide panus montelukasti terapeutilisse toimesse on minimaalne.
Elimineerimine
Tervetel täiskasvanutel ,. kliirens montelukasti plasmakontsentratsioon on keskmiselt 45 ml / min. Pärast radiomärgistatud montelukasti annuse suukaudset manustamist tuvastati 86% radioaktiivsusest viiepäevase väljaheite testiga ja vähem kui 0,2% uriiniga. Need andmed koos montelukasti biosaadavusega seotud andmetega pärast suukaudset manustamist näitavad, et montelukast ja selle metaboliidid erituvad peaaegu ainult sapi kaudu.
Patsientide omadused
Eakatel või kerge kuni mõõduka maksakahjustusega patsientidel ei ole annuse kohandamine vajalik. Neerupuudulikkusega patsientidel ei ole uuringuid läbi viidud. Kuna montelukast ja selle metaboliidid erituvad peamiselt sapiteede kaudu, ei ole neerupuudulikkusega patsientidel annuse kohandamist oodata. Puuduvad farmakokineetilised andmed montelukasti kasutamise kohta raske maksakahjustusega patsientidel (Child-Pugh skoor> 9).
Suurte montelukasti annuste (20–60 korda suurem kui täiskasvanute soovitatav annus) kasutamisel täheldati teofülliini plasmakontsentratsiooni vähenemist, mida soovitatud annuse 10 mg üks kord päevas kasutamisel ei täheldatud.
05.3 Prekliinilised ohutusandmed
Loomkatsetes täheldati kergeid ja mööduvaid seerumi biokeemilisi muutusi SGPT (ALT), glükoosi, fosfori ja triglütseriidides. Toksilisuse tunnused loomadel olid: suurenenud süljevool, seedetrakti sümptomid, lahtised väljaheited ja elektrolüütide tasakaaluhäired. Need esinesid annuste korral, mis andsid> 17 -kordse süsteemse ekspositsiooni, mida täheldati kliinilise annuse korral. Loomkatsetes ei mõjutanud montelukast viljakust ja reproduktiivvõimet süsteemse ekspositsiooni korral, mis ületas kliinilise süsteemse ekspositsiooni rohkem kui 24 korda. Emaste rottide fertiilsusuuringus manustati annustes 200 mg / kg päevas (> 69 korda rohkem kui täheldati vastsündinute kehakaalu kerget vähenemist. Küülikute uuringutes täheldati "mittetäieliku luustumise suuremat esinemissagedust kui kontrollrühmas" süsteemse ekspositsiooni korral> 24 korda, mis täheldati kliinilise annustamise korral. Rottidel ei täheldatud kõrvalekaldeid. On tõestatud, et montelukast läbib platsentaarbarjääri ja eritub loomade rinnapiima.
Hiirtel ja rottidel ei esinenud surmajuhtumeid pärast ühekordset suukaudset annust kuni 5000 mg / kg, maksimaalset testitud annust (vastavalt 15 000 mg / m2 ja 30 000 mg / m2 hiirtel ja rottidel). Annus on 25 000 korda suurem kui soovitatud annus täiskasvanutele (täiskasvanud patsiendi kehakaalu järgi 50 kg).
Leiti, et montelukastil ei olnud hiirtel fototoksilisust UVA-, UVB- ega nähtava valgusspektri suhtes annustes kuni 500 mg / kg ööpäevas (ligikaudu 200 korda suurem kui kliinilises annuses täheldatud süsteemne ekspositsioon).
Montelukast ei olnud in vitro ja in vivo testides mutageenne ega närilistel onkogeenne.
06.0 FARMATSEUTILINE TEAVE
06.1 Abiained
Mannitool (E421), mikrokristalne tselluloos, kroskarmelloosnaatrium, punane raudoksiid (E172), hüdroksüpropüültselluloos, kirsimaitseaine (sisaldab ka glütserooltriatsetaati (E1518)), aspartaam (E951) ja magneesiumstearaat.
06.2 Sobimatus
Ei ole asjakohane.
06.3 Kehtivusaeg
2 aastat
06.4 Säilitamise eritingimused
Hoida temperatuuril kuni 25 ° C originaalpakendis, valguse ja niiskuse eest kaitstult.
06.5 Vahetu pakendi olemus ja pakendi sisu
Pappkarp ja PA / alumiinium / PVC // 28 tabletti sisaldavad alumiiniumblistrid.
06.6 Kasutamis- ja käsitsemisjuhised
Ei mingeid erijuhiseid.
07.0 MÜÜGILOA HOIDJA
RAHVUSVAHELINE KEEMIAASUTUS DR. GIUSEPPE RENDE S.r.l. - Via Salaria n. 1240 - 00138 Rooma
08.0 MÜÜGILOA NUMBER
AIC n. 041494016 - AIRING 4 mg närimistabletid - 28 tabletti
09.0 MÜÜGILOA VÕI UUENDAMISE KUUPÄEV
AIFA otsus 12.02.2013