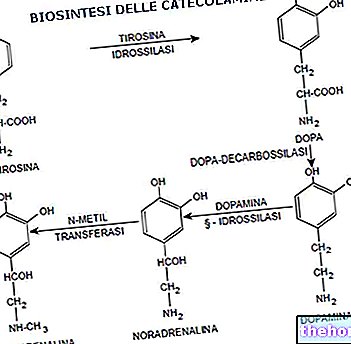
Struktuur ja funktsioonid
Hemoglobiin on metalloproteiin, mis sisaldub punastes verelibledes ja vastutab hapniku transportimise eest vereringesse. Tegelikult lahustub hapnik vees vaid mõõdukalt; seetõttu ei ole veres lahustunud kogused (alla 2% kogumahust) piisavad kudede metaboolsete vajaduste rahuldamiseks. Seetõttu on konkreetse vedaja vajadus ilmne.
Vereringes ei saa hapnik otseselt ja pöörduvalt valkudega seonduda, nagu see esineb metallide, näiteks vase ja raua puhul. Pole üllatav, et iga proteiini alaühiku keskmes, mis on ümbritsetud valgukestaga, leiame nn proteesi rühm EME, metallilise südamega, mida kujutab Fe2 + oksüdeerimisolekus (redutseeritud olekus) olev rauaatom, mis seob hapniku pöörduvalt.
Vereanalüüs
- Normaalsed hemoglobiini väärtused veres: 13-17 g / 100 ml
Naistel on väärtused keskmiselt 5-10% madalamad kui meestel.
Kõrge hemoglobiini põhjused
- Polütsüteemia
- Pikem viibimine kõrgel pinnal
- Kroonilised kopsuhaigused
- Südamehaigus
- Vere doping (erütropoetiini ja nende toimet jäljendavate derivaatide või ainete kasutamine)
Madala hemoglobiini põhjused
- Aneemia
- Rauapuudus (rauapuudus)
- Rikkalik verejooks
- Kartsinoomid
- Rasedus
- Thalassemia
- Põletab
Hapnikusisalduse veres annab seetõttu plasmas lahustunud väikese koguse liitmine fraktsiooniga, mis on seotud raua hemoglobiiniga.
Üle 98% veres sisalduvast hapnikust on seotud hemoglobiiniga, mis omakorda ringleb punavereliblede eraldatud vereringes. Ilma hemoglobiinita ei saaks erütrotsüüdid täita oma ülesannet vere hapniku transportijatena.
Arvestades selle metalli keskset rolli, nõuab hemoglobiini süntees piisavat raua tarbimist toidus. Ligikaudu 70% kehas leiduvast rauast sisaldub tegelikult hemoglobiini heemirühmades.
Hemoglobiin koosneb 4 alaühikust, mis on struktuurilt väga sarnased müoglobiiniga *.
* Kui hemoglobiin transpordib hapnikku kopsudest kudedesse, siis müoglobiin kannab hemoglobiini poolt vabanenud hapniku erinevatesse rakulistesse organellidesse, mis seda kasutavad (nt mitokondrid).

Hemoglobiin on suur ja keeruline metalloproteiin, mida iseloomustab neli kerakujulist valguahelat, mis on vastavalt ümbritsetud Fe2 +sisaldava heemirühmaga.
Seetõttu leiame iga hemoglobiini molekuli kohta neli heemirühma, mis on pakitud suhtelisse globaalsesse valguahelasse. Kuna igas hemoglobiinimolekulis on neli raua aatomit, võib iga hemoglobiinimolekul siduda endaga neli hapniku aatomit vastavalt pöörduvale reaktsioonile:
Hb + 4O2 ← → Hb (O2) 4
Nagu enamikule teada, on hemoglobiini ülesanne võtta kopsudesse hapnik, vabastada see rakkudele, kes seda vajavad, võtta neilt süsinikdioksiid ja vabastada see kopsudesse, kus tšilo uuesti algab.
Vere läbimisel kopsu alveoolide kapillaarides seob hemoglobiin endaga hapniku, mis seejärel vabaneb perifeerse vereringe kudedesse. See vahetus toimub seetõttu, et hapniku sidemed EME rühma rauaga on labiilsed ja tundlikud paljude tegurite suhtes, millest olulisim on hapniku pinge või osarõhk.
Hapniku sidumine hemoglobiiniga ja Bohri efekt
Kopsudes suureneb plasma hapniku pinge gaasi difusiooni tõttu alveoolidest verre (↑ PO2); see tõus põhjustab hemoglobiini innukat sidumist hapnikuga; vastupidine toimub perifeersetes kudedes, kus lahustunud hapniku kontsentratsioon veres väheneb (↓ PO2) ja süsinikdioksiidi osarõhk suureneb (↑ CO2); see põhjustab hemoglobiini hapniku vabanemist ja süsinikdioksiidi laengut. Kontseptsiooni võimalikult lihtsustamine, mida rohkem süsinikdioksiidi veres on, seda vähem jääb hapnikku hemoglobiiniga seotuks.
Kuigi veres füüsiliselt lahustunud hapniku kogus on väga väike, mängib see seetõttu olulist rolli. Tegelikult mõjutab see kogus tugevalt hapniku ja hemoglobiini vahelist sideme tugevust (samuti kujutab endast "olulist kontrollväärtust kopsuventilatsiooni reguleerimisel").
Kui kõike graafikuga kokku võtta, kasvab hemoglobiiniga seotud hapniku hulk pO2 suhtes sigmoidkõvera järgi:

Asjaolu, et platoo piirkond on nii suur, annab olulise ohutusvaru hemoglobiini maksimaalse küllastumise korral kopsudesse sisenemise ajal. Kuigi pO2 alveolaarsel tasemel on tavaliselt 100 mm Hg, jälgides joonist, märkame tegelikult, kuidas isegi kui hapniku osarõhk on 70 mmHg (mõne haiguse tüüpiline esinemine või kõrgel kõrgusel viibimine), jääb küllastunud hemoglobiini protsent 100%lähedale.
Maksimaalse kalde piirkonnas langeb hapniku osaline pinge alla 40 mmHg, langeb hemoglobiini võime hapnikku siduda järsult.
Puhketingimustes on rakusiseste vedelike PO2 ligikaudu 40 mmHg; selles kohas hajub gaaside seaduste tõttu plasmas lahustunud hapnik O2 kehvemate kudede poole, ületades kapillaarmembraani. Järelikult langeb O2 plasmapinge veelgi ja see soodustab hapniku vabanemist hemoglobiinist. . Seevastu intensiivse füüsilise koormuse korral langeb kudedes hapniku pinge 15 mmHg või alla selle, mille tagajärjel verest hapnik väheneb.
Nagu öeldud, puhkeolekus väljub kudedest oluline kogus hapnikuga rikastatud hemoglobiini, mis jääb vajaduse korral kättesaadavaks (näiteks mõnede rakkude ainevahetuse järsu kiirenemise korral).
Ülaltoodud pildil näidatud pidevat joont nimetatakse hemoglobiini dissotsiatsioonikõveraks; see määratakse tavaliselt in vitro pH 7,4 juures ja temperatuuril 37 ° C.
Bohri efekt mõjutab nii O2 tarbimist kopsutasandil kui ka selle vabanemist kudede tasandil.
Kui vesinikkarbonaadi kujul on rohkem lahustunud süsinikdioksiidi, eraldab hemoglobiin kergemini hapnikku ja laeb süsinikdioksiidi (vesinikkarbonaadi kujul).

Sama efekt saavutatakse vere hapestamisel: mida rohkem vere pH langeb ja seda vähem jääb hapnik hemoglobiiniga seotuks; pole üllatav, et süsinikdioksiid lahustub veres peamiselt süsinikhappe kujul, mis dissotsieerub.



Avastaja auks on pH või süsinikdioksiidi mõju hapniku dissotsiatsioonile tuntud kui Bohri efekt.
Nagu oodatud, vabastab hemoglobiin happelises keskkonnas kergemini hapnikku, samas kui aluselises keskkonnas on side hapnikuga tugevam.

Teised tegurid, mis võivad muuta hemoglobiini afiinsust hapniku suhtes, hõlmavad temperatuuri. Eelkõige väheneb hemoglobiini afiinsus hapniku suhtes kehatemperatuuri tõustes. See on eriti kasulik talve- ja kevadkuudel, kuna kopsuvere temperatuur (kokkupuutel väliskeskkonna õhk) on madalam kui kudedes, kus hapniku vabanemine on seega hõlbustatud.

2.3 Difosfoglütseraat on glükolüüsi vaheühend, mis mõjutab hemoglobiini afiinsust hapniku suhtes. Kui selle kontsentratsioon vere punalibledes suureneb, väheneb hemoglobiini afiinsus hapniku suhtes, hõlbustades seega hapniku vabanemist kudedesse. Pole üllatav, et erütrotsüütide kontsentratsioon 2,3 difosfoglütseraadi sisaldus suureneb näiteks aneemia, südame-kopsu puudulikkuse ja kõrgel kõrgusel viibimise ajal.
Üldiselt on 2,3 bisfosfoglütseraadi toime suhteliselt aeglane, eriti kui võrrelda kiiret reageerimist süsinikdioksiidi pH, temperatuuri ja osarõhu muutustele.

Bohri efekt on intensiivse lihastöö ajal väga oluline; sellistes tingimustes tõuseb tegelikult stressiga kõige enam kokku puutuvates kudedes kohalik süsinikdioksiidi temperatuuri ja rõhu tõus, seega vere happesus. Nagu eespool selgitatud, soodustab see kõik hapniku vabanemist kudedesse, nihutades hemoglobiini dissotsiatsioonikõverat paremale.