Toimeained: fluoksetiin
AZUR 20 mg kõvakapslid Fluoksetiin
Miks Azurit kasutatakse? Milleks see mõeldud on?
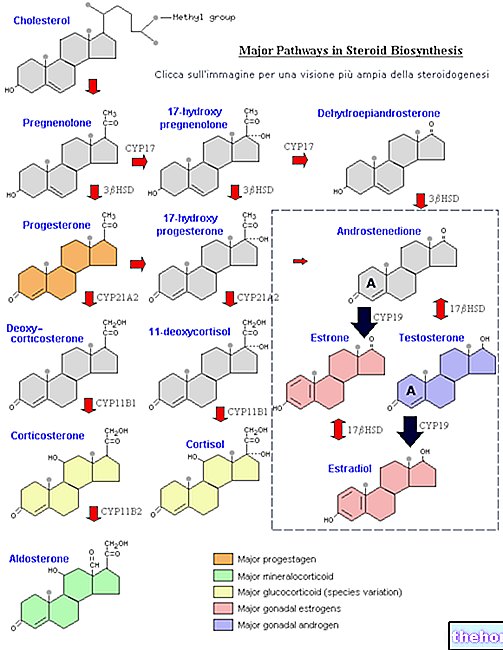
FARMAKOTERAPEUTILINE KATEGOORIA
Antidepressandid. Selektiivsed serotoniini tagasihaarde inhibiitorid.
RAVI NÄIDUSTUSED
AZUR on näidustatud depressiooni, obsessiiv -kompulsiivse häire ja buliimia raviks.
Vastunäidustused Kui Azurit ei tohi kasutada
Harvadel juhtudel on seoses fluoksetiinraviga teatatud serotoniinisündroomi või pahaloomulise neuroleptilise sündroomi sarnaste sündmuste tekkest, eriti kui fluoksetiini manustatakse koos teiste serotoniinergiliste ravimitega (muuhulgas L-trüptofaan) ja / või neuroleptikumidega. Kuna need sündroomid võivad tekitada patsiendile potentsiaalselt eluohtlikke seisundeid, võivad selliste sündmuste ilmnemisel tekkida (neid iseloomustavad sümptomite rühmad nagu hüpertermia, jäikus, müokloonus, autonoomse närvisüsteemi ebastabiilsus koos võimalike kiirete elutähtsate kõikumistega, segasus, ärrituvus ja äärmine erutus kuni deliiriumi ja koomani) ravi fluoksetiiniga tuleb katkestada ja alustada sümptomaatilist toetavat ravi.
Ettevaatusabinõud kasutamisel Mida on vaja teada enne Azuri võtmist
Kasutamiseks lastele ja alla 18 -aastastele noorukitele
Enesetappudega seotud käitumist (enesetapukatse ja enesetapumõtted) ja vaenulikku suhtumist (eriti agressiivne, opositsiooniline ja vihakäitumine) täheldati kliinilistes uuringutes sagedamini antidepressantidega ravitud lastel ja noorukitel kui platseebot saanud patsientidel. Azur on ette nähtud kasutamiseks lastel ja noorukitel vanuses 8 kuni 18 aastat ainult mõõduka kuni raske depressiooni episoodide raviks ja seda ei tohi kasutada muude näidustuste korral. Kui meditsiinilise vajaduse põhjal tehakse otsus ravi kohta, tuleb patsienti hoolikalt jälgida enesetapumõjude ilmnemise suhtes. Lisaks on laste ja noorukite kohta pikaajalise mõju kohta ohutusele, sealhulgas mõjule kasvule, seksuaalsele küpsemisele ning kognitiivsele, emotsionaalsele ja käitumuslikule arengule, saadaval ainult piiratud andmed.
19 nädalat kestnud kliinilises uuringus täheldati fluoksetiiniga ravitud lastel ja noorukitel pikkuse ja kehakaalu langust (vt lõik Kõrvaltoimed). Ei ole kindlaks tehtud, kas sellel on mõju normaalse pikkuse saavutamisele täiskasvanu ". Ei saa välistada puberteedi hilinemise võimalust (vt lõik Kõrvaltoimed). Seetõttu tuleb fluoksetiinravi ajal ja pärast seda jälgida puberteedi kasvu ja arengut (pikkus, kaal ja TANNERi staadium). Kui mõlemad on aeglustunud, tuleb nõuda pediaatrilist hindamist.
Laste kliinilistes uuringutes teatati sageli maaniast ja hüpomaaniast (vt lõik „Kõrvaltoimed“). Seetõttu on soovitatav regulaarselt jälgida maania / hüpomaania tekkimist. Maniakaalsesse faasi siseneva patsiendi puhul tuleb fluoksetiinravi katkestada.
On oluline, et arst arutaks hoolikalt lapse ja noore ja / või nende vanematega ravi riske ja kasu.
Lööve ja allergilised reaktsioonid: On teatatud lööbest, anafülaktoidsetest sündmustest ja progresseeruvatest süsteemsetest sündmustest, mõnikord tõsistest (naha, neerude, maksa või kopsude puhul). Nahalööbe või muude allergiliste nähtude ilmnemisel, mille puhul ei ole võimalik kindlaks teha erinevat etioloogiat, tuleb fluoksetiini manustamine lõpetada.
Ettevaatusabinõud
Krambid: Krambid kujutavad endast potentsiaalset riski antidepressantide kasutamisel. Seetõttu, nagu ka teiste antidepressantide puhul, tuleb fluoksetiini manustada ettevaatusega patsientidele, kellel on esinenud krampe. Ravi tuleb katkestada kõigil patsientidel, kellel esinevad krambid või kellel on täheldatud krampide esinemissageduse suurenemist. Ebastabiilsete krambihoogude / epilepsiaga patsientidel tuleb fluoksetiini manustamist vältida ja kontrollitud epilepsiaga patsiente tuleb hoolikalt jälgida.
Mania: antidepressante tuleb mania / hüpomaania anamneesiga patsientidel kasutada ettevaatusega. Nagu kõik antidepressandid, tuleb fluoksetiini kasutamine maniakaalsesse faasi sattunud patsientidel katkestada.
Maksa- / neerufunktsioon: Fluoksetiin metaboliseerub ulatuslikult maksas ja eritub neerude kaudu. Olulise maksafunktsiooni häirega patsientidel on soovitatav kasutada väiksemat annust 20 mg ööpäevas, nt. alternatiivne päevane annus. Kui fluoksetiini 20 mg ööpäevas manustati 2 kuu jooksul, ei näidanud dialüüsi vajavate raske neerukahjustusega (GFR <10 ml / min) patsientidel erinevusi fluoksetiini ega norfluoksetiini plasmatasemes võrreldes normaalse neerufunktsiooniga kontrollidega.
Südamehaigus: 312 patsiendil, kes said topeltpimedates kliinilistes uuringutes fluoksetiini, ei täheldatud EKG-s ühtegi juhtivuse muutust, mis põhjustas südame seiskumist. Kuid ägeda südamehaiguse kliiniline kogemus on piiratud, seega on soovitatav olla ettevaatlik.
Kehakaalu langus: Fluoksetiini võtvatel patsientidel võib esineda kehakaalu langust, kuid see on tavaliselt proportsionaalne algkaaluga.
Diabeet: diabeediga patsientidel võib SSRI -ravi muuta glükeemilist kontrolli. Hüpoglükeemia tekkis fluoksetiinravi ajal, samas kui hüperglükeemia tekkis pärast ravimi kasutamise lõpetamist. Vajalikuks võib osutuda insuliini ja / või suukaudse hüpoglükeemilise aine annuse kohandamine.
Enesetapp / enesetapumõtted või kliiniline halvenemine: Depressioon on seotud enesetapumõtete, enesevigastamise ja enesetapu (suitsiidiga seotud sündmused) suurenenud riskiga. See oht püsib kuni haiguse märkimisväärse remissioonini. Kuna paranemine ei pruugi ilmneda esimestel või järgnevatel ravinädalatel, tuleb patsiente tähelepanelikult jälgida kuni paranemiseni. Üldine kliiniline kogemus näitab, et enesetapurisk võib paranemisprotsessi alguses suureneda.
Teised psühhiaatrilised seisundid, mille puhul Azur on välja kirjutatud, võivad olla seotud ka enesetapuga seotud sündmuste suurenenud riskiga. Lisaks võivad need seisundid kaasneda depressiooniga. Seetõttu tuleb rakendada samu ettevaatusabinõusid, mida järgitakse raske depressiooniga patsientide ravimisel ka teiste psühhiaatriliste häiretega patsientide ravimisel.
Patsientide seas, kellel on anamneesis suitsiidiga seotud juhtumeid, on patsientidel, kellel oli enne ravi alustamist märkimisväärne enesetapumõte, suurenenud risk enesetapumõteteks ja enesetapukatseteks ning neid tuleb ravi ajal hoolikalt jälgida. Kliiniliste uuringute metaanalüüs antidepressantidega võrreldes platseeboga psühhiaatriliste häirete ravis näitasid suitsidaalse käitumise riski suurenemist alla 25 -aastastel patsientidel, kes said antidepressante, võrreldes platseeboga.
Patsientide ja eriti kõrge riskiga patsientide hoolikas jälgimine peaks kaasnema ravimitega, eriti ravi algfaasis ja pärast annuse muutmist. Patsiente (või nende hooldajaid) tuleb teavitada vajadusest jälgida ja viivitamatult raviarstile teatada kliinilise pildi halvenemisest, enesetapukäitumise või -mõtete ilmnemisest või ebatavalistest muutustest käitumises, kui need sümptomid ilmnevad.
Akatiisia / psühhomotoorne rahutus: Fluoksetiini kasutamist on seostatud akatiisia tekkega, mida iseloomustab "subjektiivselt ebameeldiv või murettekitav rahutus ja vajadus sageli liikuda, millega kaasneb" võimetus paigal istuda või seista. See on tõenäolisem. Patsientidel, kellel tekivad need sümptomid, võib annuse suurendamine olla kahjulik.
Katkestamissümptomid, mida täheldati SSRI -ravi katkestamisel: katkestamise sümptomid on ravi lõpetamisel tavalised, eriti kui ravi lõpetatakse järsult (vt lõik "Kõrvaltoimed"). Kliinilistes uuringutes esines ravi järsul katkestamisel täheldatud kõrvaltoimeid ligikaudu 60% -l patsientidest nii fluoksetiini kui ka platseeborühmas. Nendest kõrvaltoimetest olid 17% fluoksetiinirühmas ja 12% fluoksetiinigrupis platseebot saanud patsientidel tõsised. looduses.
Võõrutusnähtude risk võib sõltuda mitmest tegurist, sealhulgas ravi kestusest ja annusest ning annuse vähendamise kiirusest. Kõige sagedamini teatatud reaktsioonid on pearinglus, sensoorsed häired (sh paresteesia), unehäired (sh unetus ja intensiivsed unenäod), asteenia, erutus või ärevus, iiveldus ja / või oksendamine, värisemine ja peavalu. Üldiselt on need sümptomid kerged kuni mõõdukad, kuid mõnedel patsientidel võivad need olla tugevad. Need sümptomid tekivad tavaliselt esimestel päevadel pärast ravi lõpetamist. Üldjuhul on need sümptomid iseenesest mööduvad ja taanduvad tavaliselt 2 nädala jooksul, kuigi mõnel inimesel võivad need pikeneda (2-3 kuud või kauem). Seetõttu soovitame Azur-ravi järk-järgult väheneb vähemalt 1-2 nädala jooksul enne ravi lõpetamist vastavalt patsiendi vajadusele (vt lõik "Azur-ravi katkestamisel täheldatud võõrutusnähud", annus, manustamisviis ja aeg).
Verejooks: SSRI -de kasutamisel on teatatud nahaverejooksu ilmingutest, nagu ekhümoos ja purpur. Harva on teatatud muudest hemorraagilistest ilmingutest (nt günekoloogilised verejooksud, seedetrakti verejooks ja muu naha või limaskesta verejooks).
SSRI -sid kasutavatel patsientidel tuleb olla ettevaatlik, eriti samaaegsel kasutamisel suukaudsete antikoagulantidega, ravimitega, mis teadaolevalt mõjutavad trombotsüütide funktsiooni (nt ebatüüpilised antipsühhootikumid nagu klosapiin, fenotiasiinid, enamik tritsüklilisi antidepressante, aspiriin, MSPVA -d) või muud ravimid, mis võivad suurendada verejooksu riski , samuti patsientidel, kellel on esinenud verejooksu häireid.
Elektrokonvulsiivne ravi (ECT): fluoksetiiniga ravitud patsientidel, kes saavad EKT-ravi, on harva teatatud pikaajalistest krampidest, seega on soovitatav olla ettevaatlik.
Naistepuna: Selektiivsete setononiini tagasihaarde inhibiitorite ja naistepuna (Hypericum perforatum) sisaldavate taimsete preparaatide samaaegsel kasutamisel võivad tekkida tugevamad serotoniinergilised toimed, näiteks serotoniinisündroom.
Koostoimed Millised ravimid või toidud võivad Azuri toimet muuta
Rääkige oma arstile või apteekrile, kui olete hiljuti kasutanud mingeid ravimeid, isegi ilma retseptita
Koostoimeuuringuid on läbi viidud ainult täiskasvanutel.
Poolväärtusaeg: kui arvestada farmakodünaamilisi või farmakokineetilisi koostoimeid (nt fluoksetiinilt teistele antidepressantidele üleminekul), tuleb arvestada nii fluoksetiini kui ka norfluoksetiini pika eliminatsiooni poolväärtusajaga.
Monoamiini oksüdaasi inhibiitorid: (vt lõik "Vastunäidustused").
Ei ole soovitatav kasutada kombinatsioone: MAOI-tüüp A (vt lõik "Vastunäidustused").
Ühendused, mis nõuavad nende kasutamisel ettevaatusabinõusid:
MAOI-tüüp B (selegiliin): serotoniinisündroomi oht. Soovitatav on kliiniline jälgimine.
Fenütoiin: Fluoksetiiniga kombineerituna on täheldatud muutusi veres. Mõnel juhul on esinenud toksilisuse ilminguid. Seetõttu on soovitatav manustada fenütoiini vastavalt konservatiivsetele raviskeemidele ja hoolikalt jälgida patsiendi kliinilisi seisundeid.
Kesknärvisüsteemi ravimid: fluoksetiini manustamine võib põhjustada karbamasepiini, haloperidooli, klosapiini, alprasolaami, imipramiini ja desipramiini taseme tõusu veres; mõnel juhul täheldati toksilisuse kliinilisi ilminguid. Seetõttu on soovitatav manustada samaaegselt kasutatavaid ravimeid vastavalt kaalutletud raviskeemidele ja järgida patsiendi kliinilisi seisundeid.
Diasepaam: selle ravimi toime võib pikeneda.
Serotoniinergilised ravimid: samaaegne manustamine serotoniinergiliste ravimitega (nt tramadool, triptaanid) võib suurendada serotoniinisündroomi tekke riski. Seos triptaanidega lisab täiendavat riski pärgarterite vasokonstriktsiooni ja arteriaalse hüpertensiooni tekkeks.
Liitium ja trüptofaan: kui SSRI -sid on manustatud kombinatsioonis liitiumi või trüptofaaniga, on teatatud serotoniinisündroomist ja seetõttu tuleb fluoksetiini samaaegsel kasutamisel nende ravimitega kasutada ettevaatusega. Kui fluoksetiini manustatakse koos liitiumiga, on vajalik sihipärasem ja sagedasem kliiniline jälgimine.
CYP2D6 isoensüüm: Kuna fluoksetiini metabolism (nagu tritsükliliste antidepressantide ja teiste selektiivsete antidepressantide puhul serotoniini puhul) mõjutab tsütokroom CYP2D6 isoensümaatilist süsteemi maksas, võib samaaegne ravi sama ensüümsüsteemi poolt metaboliseeritavate ravimitega põhjustada ravimite koostoimeid. Samaaegne ravi ravimitega, mida peamiselt metaboliseerib see isoensüüm ja mille terapeutiline indeks on piiratud (nt flekainiid, enkainiid, karbamasepiin ja tritsüklilised antidepressandid), tuleb alustada või kohandada väikseimast efektiivsest annusest. Seda tuleb teha isegi siis, kui fluoksetiini on võetud viimase 5 nädala jooksul.
Suukaudsed antikoagulandid: Fluoksetiini ja suukaudsete antikoagulantide samaaegsel manustamisel on harva täheldatud muutunud antikoagulantide toimet (laboratoorsed andmed ja / või kliinilised sümptomid ja tunnused), mis ei sobi homogeensesse kategooriasse, kuid hõlmavad suurenenud verejooksu. Kui fluoksetiinravi alustatakse või lõpetatakse varfariini saavatel patsientidel, tuleb hoolikalt jälgida hüübimist (vt lõik "Ettevaatusabinõud kasutamisel", Verejooks).
Elektrokonvulsioonravi (ECT): fluoksetiiniga ravitud patsientidel, kes saavad EKT-ravi, on harva teatatud krampide pikenemisest, seega on soovitatav olla ettevaatlik.
Alkohol: rutiinsetes testides ei põhjusta fluoksetiin vere alkoholisisalduse tõusu ega tugevda alkoholi toimet. SSRI ja alkoholravi kombinatsioon ei ole siiski soovitatav.
Naistepuna: võib esineda farmakodünaamilisi koostoimeid fluoksetiini ja naistepuna (Hypericum perforatum) sisaldava taimse preparaadi vahel, mis võib põhjustada serotonergiliste toimete suurenemist ja kõrvaltoimete suurenemist.
Hoiatused Oluline on teada, et:
Rasedus, imetamine
Enne mis tahes ravimi kasutamist pidage nõu oma arsti või apteekriga. Rääkige oma arstile niipea kui võimalik, kui olete rase, arvate end olevat rase või kavatsete rasestuda.
Rasedatel ja imetavatel naistel peab arst Azur -ravi hoolikalt hindama ja ravimit kasutama ainult juhul, kui oodatav kasu õigustab võimalikku ohtu lootele.
Vastsündinute kohta, kelle emad võtsid Azuri esimestel raseduskuudel, on olemas andmed, mis näitavad suurenenud sünnidefektide riski, eriti südame puhul. Üldpopulatsioonis sünnib südamepuudulikkusega umbes 1 laps 1000 -st. See suhe suureneb Azuri võtnud emade puhul umbes 2 -le 1000 -st beebist. Koos oma arstiga saate otsustada, kas on asjakohasem raseduse ajal Azuri tarbimist järk -järgult vähendada.Sõltuvalt asjaoludest võib arst soovitada teil Azur'i kasutamist jätkata või mitte.
Veenduge, et teie ämmaemand ja / või arst teaksid, et teid ravitakse Azuriga. Raseduse ajal, eriti raseduse viimase 3 kuu jooksul, võivad sellised ravimid nagu Azur suurendada vastsündinu tõsise lastehaiguse, mida nimetatakse püsivaks pulmonaalseks hüpertensiooniks (IPPN), riski, millega kaasneb vastsündinu kiire hingamine ja välimus. värvus, sinakas. Tavaliselt ilmnevad need sümptomid esimese 24 tunni jooksul pärast lapse sündi. Kui teie lapsel tekivad need sümptomid, rääkige sellest kohe oma ämmaemandale ja / või arstile.
Ettevaatust tuleb kasutada fluoksetiini kasutamisel raseduse ajal, eriti raseduse lõpus või vahetult enne sünnituse algust, sest vastsündinutel on teatatud järgmistest toimetest: ärrituvus, värisemine, hüpotoonia, pidev nutmine, imemis- või magamisraskused. Need sümptomid võivad näitavad nii serotonergilist toimet kui ka võõrutussündroomi.
Imetamine: Fluoksetiin ja selle aktiivne metaboliit norfluoksetiin erituvad teadaolevalt rinnapiima. Imetavatel imikutel on teatatud kõrvaltoimetest. Kui ravi fluoksetiiniga peetakse vajalikuks, tuleb kaaluda rinnaga toitmise katkestamist, kuid kui rinnaga toitmist jätkatakse, tuleb määrata madalaim efektiivne fluoksetiini annus.
Meeste viljakus: Loomkatsetes on fluoksetiin vähendanud sperma kvaliteeti. Teoreetiliselt võib see mõjutada viljakust, kuid mõju inimese viljakusele ei ole veel täheldatud.
Autojuhtimine ja masinatega töötamine
Kuigi on tõestatud, et fluoksetiin ei häiri tervetel vabatahtlikel psühhomotoorset jõudlust, võib iga psühhoaktiivne ravim kahjustada otsustusvõimet või kutseoskusi. Patsiente tuleb soovitada vältida sõiduki juhtimist või ohtlike masinatega töötamist.
Annustamine ja kasutusviis Kuidas Azuri kasutada: Annustamine
Suukaudseks manustamiseks.
Peamised depressiooni episoodid
Täiskasvanud ja eakad:
Soovitatav annus on 20 mg päevas. Vajadusel tuleb annus 3-4 nädala jooksul pärast ravi alustamist üle vaadata ja seda korrigeerida ning seejärel kliiniliselt sobivaks hinnata. Kuigi suuremate annuste korral võib esineda kõrvaltoimete sagenemise võimalus, võib mõnel patsiendil, kelle ravivastus ei ole 20 mg , võib annust järk -järgult suurendada kuni maksimaalse 60 mg -ni. Iga patsiendi annust tuleb kohandada hoolikalt, et hoida patsienti väikseima efektiivse annusena.
Depressiooniga patsiente tuleb ravida piisavalt kaua, vähemalt 6 kuud, et veenduda sümptomite puudumises.
Obsessiiv-kompulsiivne häire
Täiskasvanud ja eakad: soovitatav annus on 20 mg ööpäevas. Kuigi suuremate kui 20 mg ööpäevaste annuste korral võib mõnedel patsientidel kõrvaltoimete esinemissagedus suureneda, võib annust järk -järgult suurendada kuni maksimaalse 60 mg -ni, kui kahe nädala pärast ei saavutata 20 mg -le piisavat ravivastust.
Kui 10 nädala jooksul paranemist ei täheldata, tuleb fluoksetiinravi uuesti kaaluda. Kui on saavutatud hea ravivastus, võib ravi jätkata individuaalselt kohandatud annusega. Kuigi puuduvad süstemaatilised uuringud fluoksetiinravi jätkamise kestuse kindlakstegemiseks, on OCD krooniline haigus ja ravile alluvatel patsientidel on mõistlik kaaluda ravi pikendamist üle 10 nädala. Annust tuleb iga patsiendi puhul hoolikalt muuta, et patsient saaks väikseima efektiivse annuse. Ravi vajadust tuleb perioodiliselt uuesti hinnata. Patsientidel, kes on farmakoteraapiale hästi reageerinud, peavad mõned arstid kasulikuks samaaegset käitumuslikku psühhoteraapiat.
Pikaajalist efektiivsust (üle 24 nädala) ei ole OCD puhul tõestatud.
Buliimia
Täiskasvanud ja eakad: soovitatav annus on 60 mg ööpäevas. Pikaajalist (üle 3 kuu) efektiivsust ei ole tõestatud bulimia nervosa korral.
Täiskasvanud
Kõigi näidustuste korral: soovitatud annust võib suurendada või vähendada. Üle 80 mg ööpäevaseid annuseid ei ole süstemaatiliselt hinnatud.
Fluoksetiini võib manustada ühe või mitme annusena, koos toiduga või ilma.
Kui annustamine lõpetatakse, püsivad farmakoloogiliselt aktiivsed ained kehas nädalaid, seda tuleb ravi alustamisel või lõpetamisel meeles pidada.
8 -aastased ja vanemad lapsed ja noorukid (Mõõdukas kuni raske raske depressiooni episood)
Azur on ette nähtud kasutamiseks lastel ja noorukitel vanuses 8 kuni 18 aastat ainult mõõduka kuni raske depressiooni episoodide raviks ja seda ei tohi kasutada muude näidustuste korral.
Ravi tuleb alustada ja jälgida spetsialisti järelevalve all. Algannus on 10 mg ööpäevas. Annust tuleb kohandada hoolikalt, individuaalselt, et hoida patsient väikseima efektiivse annusena.
Ühe kuni kahe nädala pärast võib annust suurendada 20 mg -ni päevas. Kliiniline kogemus üle 20 mg ööpäevaste annuste kasutamisel on minimaalne. Üle 9 nädala kestnud ravi kohta on andmed piiratud.
Madala kehakaaluga lapsed
Kuna madalama kehakaaluga lastel saavutatakse kõrgem plasmakontsentratsioon, saab terapeutilise toime saavutada väiksemate annustega.
Lastel, kes reageerivad ravile, tuleb uuesti hinnata vajadust ravi jätkata 6 kuu pärast. Kui 9 nädala jooksul ei ole kliinilist kasu saavutatud, tuleb ravi uuesti läbi vaadata.
Eakad: annuse suurendamisel on soovitatav olla ettevaatlik ja ööpäevane annus ei tohi üldiselt ületada 40 mg. Maksimaalne soovitatav annus on 60 mg päevas.
Maksapuudulikkusega patsientidel või patsientidel, kellel on võimalik koostoime Azuri ja kombineeritud ravimite vahel, tuleb kaaluda väiksemat või harvemat annust (nt 20 mg igal teisel päeval).
Azur -ravi katkestamisel täheldatud võõrutusnähud:
Järsku ravi katkestamist tuleks vältida. Azur-ravi lõpetamisel tuleb annust järk-järgult vähendada vähemalt 1-2 nädala jooksul, et vähendada võõrutusreaktsioonide riski (vt lõik "Ettevaatusabinõud kasutamisel" ja lõik "Kõrvaltoimed"). "). Kui pärast annuse vähendamist või ravi katkestamist tekivad talumatud sümptomid, võib kaaluda eelnevalt määratud annuse jätkamist. Seejärel võib arst jätkata annuse vähendamist, kuid järk -järgult.
Üleannustamine Mida teha, kui olete Azur'i võtnud liiga palju?
Juhuslikul Azur'i liiga suure annuse allaneelamisel / võtmisel teavitage sellest kohe oma arsti või minge lähimasse haiglasse
Ainuüksi fluoksetiini põhjustatud üleannustamise juhtumid on tavaliselt kerged. Üleannustamise sümptomiteks on iiveldus, oksendamine, krambid, kardiovaskulaarne düsfunktsioon, alates asümptomaatilisest arütmiast kuni südame seiskumiseni, kopsufunktsiooni häire ja muutused kesknärvisüsteemi seisundis, alates põnevusest kuni koomani. Surmav tulemus, mis on tingitud ainult fluoksetiini üleannustamisest, on olnud äärmiselt haruldane. südamefunktsiooni ja eluliste näitajate jälgimiseks, samuti üldised sümptomaatilised ja toetavad meetmed Spetsiifilisi antidoote pole teada.
Sunnitud diurees, dialüüs, hemoperfusioon ja asendusülekanne tõenäoliselt kasu ei too. Aktiivsüsi, mida saab kasutada koos sorbitooliga, võib olla isegi tõhusam ravi kui oksendamine või maoloputus. Üleannustamise ravimisel kaaluge mitmete ravimite kaasamise võimalust. Patsientidel, kes on võtnud liiga palju tritsüklilist antidepressanti, võib olla vajalik pikem ajavahemik hoolikaks meditsiiniliseks jälgimiseks, kui nad võtavad või on hiljuti kasutanud fluoksetiini.
Kui kahtlete Azuri kasutamises, pidage nõu oma arsti või apteekriga.
VÄLJASTATUD HALDUS (TAGASISÜNDROOM).
Juhuslikul ühe või mitme annuse võtmata jätmisel on võõrutussündroomi tekkimise oht minimaalne.
Kõrvaltoimed Millised on Azuri kõrvaltoimed
Nagu kõik ravimid, võib ka Azur põhjustada kõrvaltoimeid, kuigi kõigil neid ei teki.Kõrvaltoimete intensiivsus ja esinemissagedus võivad ravi jätkamisel väheneda ega põhjusta tavaliselt ravi katkestamist.
Nagu teiste SSRI -de puhul, on täheldatud järgmisi kõrvaltoimeid:
Keha tervikuna: ülitundlikkuse ilmingud (nt sügelus, lööve, urtikaaria, anafülaktoidne reaktsioon, vaskuliit, seerumhaigust meenutav reaktsioon, angioödeem) (vt lõik "Vastunäidustused" ja lõik "Ettevaatusabinõud kasutamisel"), värinad, serotoniinisündroom, valgustundlikkus ja väga harva multiformne erüteem, mis võib areneda kuni Stevensi-Johnsoni sündroomi või toksilise epidermaalse nekrolüüsi (Lyelli sündroom) alguseni.
Kardiovaskulaarsüsteem: stenokardia, arütmia, 1. astme atrioventrikulaarne blokaad, hüpotensioon, hüpertensioon.
Seedesüsteem: seedetrakti häired (nt kõhulahtisus, iiveldus, oksendamine, düspepsia, düsfaagia, muutunud maitse), suukuivus. Harva on teatatud ebanormaalsetest maksafunktsiooni testidest. Väga harvad idiosünkraatilise hepatiidi juhtumid.
Närvisüsteem: peavalu, unehäired (nt ebanormaalsed unenäod, unetus, unisus), pearinglus, anoreksia, väsimus, unisus (nt unisus), eufooria, mööduvad ebanormaalsed liigutused (nt närvipuud, ataksia, värin, müokloonus), krambid ja harva psühhomotoorne rahutus / akatiisia (vt lõik "Ettevaatusabinõud kasutamisel") Väga harva serotoniinisündroom.
Psühhiaatrilised häired: hallutsinatsioonid, maniakaalsed reaktsioonid, segasus, erutus, ärevus ja sellega seotud sümptomid (nt närvilisus), keskendumis- ja kognitiivsete protsesside halvenemine (nt depersonalisatsioon), paanikahood, enesetapukäitumine ja -mõtted (need sümptomid võivad olla tingitud mõnest haigusest).
Fluoksetiinravi ajal või varsti pärast ravi lõpetamist on teatatud enesetapumõtete ja suitsidaalse käitumise juhtudest (vt lõik "Ettevaatusabinõud kasutamisel").
Urogenitaalsüsteem: kusepeetus ja urineerimissageduse muutus.
Reproduktiivse süsteemi häired: seksuaalne düsfunktsioon (ejakulatsiooni hilinemine või puudumine, anorgasmia), priapism, galaktorröa, hüperprolaktineemia.
Mitmesugused: alopeetsia, haigutamine, nägemishäired (nt hägune nägemine, müdriaas), higistamine, vasodilatatsioon, artralgia, müalgia, posturaalne hüpotensioon, ekhümoos, hüpoglükeemia, hüpokaleemia. Harva on teatatud muudest hemorraagilistest ilmingutest (nt günekoloogilised verejooksud, seedetrakti verejooks ja muu naha või limaskesta verejooks) (vt lõik "Ettevaatusabinõud kasutamisel", Verejooks).
Hüponatreemia: harva on teatatud hüponatreemiast (sh naatriumisisaldus alla 110 mmol / l) ja see oli pöörduv pärast fluoksetiini kasutamise lõpetamist. Mõned juhtumid olid tõenäoliselt tingitud antidiureetilise hormooni sobimatu sekretsiooni sündroomist. Enamik teateid leiti eakatel patsientidel ja patsientidel. diureetikumidega või muul põhjusel vähenenud veremahuga.
Hingamissüsteem: neelupõletik, düspnoe. Harva on teatatud kopsusündmustest (sealhulgas erineva histopatoloogiaga põletikulised protsessid ja / või fibroos). Hingeldus võib olla ainus hoiatav sümptom.
Luumurrud: seda tüüpi ravimeid kasutavatel patsientidel on täheldatud suurenenud luumurdude riski.
Võõrutusnähud, mida täheldati fluoksetiinravi katkestamisel: Fluoksetiinravi katkestamine põhjustab tavaliselt võõrutusnähte. Kõige sagedamini teatatud reaktsioonid on pearinglus, sensoorsed häired (sh paresteesia), unehäired (sh unetus ja intensiivsed unenäod), asteenia, erutus või ärevus, iiveldus ja / või oksendamine, värisemine ja peavalu. Üldiselt on need sümptomid kerge kuni mõõduka intensiivsusega ja iseenesest mööduvad, kuid mõnedel patsientidel võivad need olla rasked ja / või pikaajalised (vt lõik "Ettevaatusabinõud kasutamisel"). Seetõttu on soovitatav "ravi katkestada" järk-järgult, vähendades järk-järgult annust, kui ravi Azuriga ei ole enam vajalik (vt lõik "Annus, manustamisviis ja -aeg" ja lõik "Ettevaatusabinõud kasutamisel").
Lapsed ja noorukid (vt lõik "Ettevaatusabinõud kasutamisel"):
Laste kliinilistes uuringutes täheldati antidepressantidega ravitud lastel ja noorukitel enesetapuga seotud käitumist (enesetapukatse ja enesetapumõtted) ja vaenulikku suhtumist sagedamini kui platseebot saanud patsientidel.
Fluoksetiini ohutust ei ole süstemaatiliselt hinnatud kroonilise ravi korral, mis kestab kauem kui 19 nädalat.
Pediaatrilistes kliinilistes uuringutes teatati maniakaalsetest reaktsioonidest, sealhulgas maaniast ja hüpomaaniast (2,6% fluoksetiiniga ravitud patsientidel ja 0% platseebokontrolliga patsientidel), mis põhjustas enamikul juhtudel ravi katkestamise. Nendel patsientidel ei olnud varasemaid hüpomaania / maania episoode.
Pärast 19 -nädalast ravi teatasid kliinilises uuringus fluoksetiiniga ravitud pediaatrilised patsiendid keskmiselt 1,1 cm väiksema pikkusega (p = 0,004) ja 1,1 kg väiksema kaaluga (p = 0,008) kui platseebot saanud patsiendid.
Kliinilises kasutuses on teatatud ka üksikutest kasvupeetuse juhtudest. Kliinilisel kasutamisel lastel on teatatud üksikutest kõrvaltoimetest, mis võivad viidata seksuaalse küpsemise hilinemisele või seksuaalsele düsfunktsioonile.
Laste kliinilistes uuringutes seostati fluoksetiinravi leeliselise fosfataasi taseme langusega veres.
Kui ükskõik milline kõrvaltoimetest muutub tõsiseks või kui te märkate mõnda kõrvaltoimet, mida selles infolehes ei ole nimetatud, palun rääkige sellest oma arstile või apteekrile.
Pakendi infolehel olevate juhiste järgimine vähendab kõrvaltoimete riski. Oluline on teavitada arsti või apteekrit kõigist kõrvaltoimetest, isegi kui neid pole pakendi infolehel kirjeldatud.
Aegumine ja säilitamine
Vaadake pakendile trükitud aegumiskuupäeva.
Kõlblikkusaeg viitab puutumata pakendis olevale tootele, mis on õigesti hoitud.
Hoiatus: ärge kasutage ravimit pärast kõlblikkusaega, mis on märgitud pakendil. Hoida temperatuuril kuni 30 ° C.
Ravimeid ei tohi ära visata kanalisatsiooni kaudu ega koos majapidamisprügiga. Küsige oma apteekrilt, kuidas visata ära ravimeid, mida te enam ei kasuta. See aitab kaitsta keskkonda.
HOIDA RAVIMPREPARAAT LASTE EEST KÄTTESAAMATUS KOHAS
Koostis ja ravimvorm
KOOSTIS
Iga kapsel sisaldab:
toimeaine: 22,36 mg fluoksetiinvesinikkloriidi
vastab 20 mg fluoksetiinile
abiained: maisitärklis, dimetikoon, želatiin, titaandioksiid.
RAVIMVORM JA SISU
20 mg kõvakapslid. Karp 28 kapsliga
Allika pakendi infoleht: AIFA (Itaalia ravimiamet). Sisu avaldati jaanuaris 2016. Esitatud teave ei pruugi olla ajakohane.
Kõige ajakohasemale versioonile juurdepääsu saamiseks on soovitatav külastada AIFA (Itaalia ravimiamet) veebisaiti. Vastutusest loobumine ja kasulik teave.
01.0 RAVIMPREPARAADI NIMETUS
AZUR 20 MG KÕVAD KAPSLID
02.0 KVALITATIIVNE JA KVANTITATIIVNE KOOSTIS
Iga kapsel sisaldab:
Aktiivne põhimõte:
Fluoksetiinvesinikkloriid 22,36 mg
võrdub 20 mg fluoksetiiniga
Abiainete täielik loetelu vt lõik 6.1
03.0 RAVIMVORM
Kõvad kapslid
04.0 KLIINILINE TEAVE
04.1 Näidustused
AZUR on näidustatud depressiooni, obsessiiv -kompulsiivse häire ja buliimia raviks.
04.2 Annustamine ja manustamisviis
Suukaudseks manustamiseks.
Peamised depressiooni episoodid
Täiskasvanud ja eakad:
Soovitatav annus on 20 mg päevas. Vajadusel tuleb annus uuesti läbi vaadata ja korrigeerida 3-4 nädala jooksul pärast ravi alustamist ning seejärel hinnata, kas see on kliiniliselt sobiv. Kuigi suuremate annuste korral võib kõrvaltoimete esinemissagedus suureneda, võib mõnedel patsientidel ebapiisav ravivastus 20 mg, võib annust järk -järgult suurendada kuni maksimaalse 60 mg -ni (vt lõik 5.1 "Farmakodünaamilised omadused"). Annust tuleb individuaalselt kohandada, et hoida patsient väikseima efektiivse annusena.
Depressiooniga patsiente tuleb ravida piisavalt kaua, vähemalt 6 kuud, et veenduda sümptomite puudumises.
Obsessiiv-kompulsiivne häire
Täiskasvanud ja eakad: soovitatav annus on 20 mg ööpäevas. Kuigi suuremate kui 20 mg ööpäevaste annuste korral võib mõnedel patsientidel kõrvaltoimete esinemissagedus suureneda, võib annust järk -järgult suurendada kuni maksimaalse 60 mg -ni, kui kahe nädala pärast ei saavutata 20 mg -le piisavat ravivastust.
Kui 10 nädala jooksul paranemist ei täheldata, tuleb fluoksetiinravi uuesti kaaluda. Kui on saavutatud hea ravivastus, võib ravi jätkata individuaalselt kohandatud annusega. Kuigi puuduvad süstemaatilised uuringud fluoksetiinravi jätkamise kestuse kindlakstegemiseks, on OCD krooniline haigus ja ravile alluvatel patsientidel on mõistlik kaaluda ravi pikendamist üle 10 nädala. Annust tuleb iga patsiendi puhul hoolikalt muuta, et patsient saaks väikseima efektiivse annuse. Ravi vajadust tuleb perioodiliselt uuesti hinnata. Patsientidel, kes on farmakoteraapiale hästi reageerinud, peavad mõned arstid kasulikuks samaaegset käitumuslikku psühhoteraapiat.
Pikaajalist efektiivsust (üle 24 nädala) ei ole OCD puhul tõestatud.
Buliimia
Täiskasvanud ja eakad: soovitatav annus on 60 mg ööpäevas. Pikaajalist (üle 3 kuu) efektiivsust ei ole tõestatud bulimia nervosa korral.
Täiskasvanud
Kõigi näidustuste korral: Soovitatavat annust võib suurendada või vähendada. Üle 80 mg ööpäevaseid annuseid ei ole süstemaatiliselt hinnatud.
Fluoksetiini võib manustada ühe või mitme annusena, koos toiduga või ilma.
Kui annustamine lõpetatakse, püsivad farmakoloogiliselt aktiivsed ained kehas nädalaid, seda tuleb ravi alustamisel või lõpetamisel meeles pidada.
8 -aastased ja vanemad lapsed ja noorukid (Mõõdukas kuni raske raske depressiooni episood)
Ravi tuleb alustada ja jälgida spetsialisti järelevalve all. Algannus on 10 mg ööpäevas. Annust tuleb kohandada hoolikalt, individuaalselt, et hoida patsient väikseima efektiivse annusena.
Ühe kuni kahe nädala pärast võib annust suurendada 20 mg -ni päevas. Kliiniline kogemus üle 20 mg ööpäevaste annuste kasutamisel on minimaalne. Üle 9 nädala kestnud ravi kohta on andmed piiratud.
Madala kehakaaluga lapsed
Kuna madalama kehakaaluga lastel saavutatakse kõrgem plasmakontsentratsioon, saab terapeutilise toime saavutada väiksemate annustega (vt lõik 5.2).
Lastel, kes reageerivad ravile, tuleb uuesti hinnata vajadust ravi jätkata 6 kuu pärast. Kui 9 nädala jooksul ei ole kliinilist kasu saavutatud, tuleb ravi uuesti läbi vaadata.
Eakad: annuse suurendamisel on soovitatav olla ettevaatlik ja ööpäevane annus ei tohi üldiselt ületada 40 mg. Maksimaalne soovitatav annus on 60 mg päevas.
Maksakahjustusega patsientidel (vt lõik 5.2 Farmakokineetilised omadused) või patsientidel, kellel on Azur. (vt lõik 4.5 Koostoimed teiste ravimitega ja muud koostoimed).
Azur -ravi lõpetamisel täheldati võõrutusnähte:
Järsku ravi katkestamist tuleks vältida. Azur-ravi katkestamisel tuleb annust järk-järgult vähendada vähemalt 1-2 nädala jooksul, et vähendada võõrutusreaktsioonide riski (vt lõik 4.4 „Hoiatused ja ettevaatusabinõud kasutamisel“ ja lõik 4.8 "Kõrvaltoimed"). Kui pärast annuse vähendamist või ravi katkestamist tekivad talumatud sümptomid, võib kaaluda varem määratud annuse jätkamist. Seejärel võib arst jätkata annuse vähendamist, kuid järk -järgult.
04.3 Vastunäidustused
Ülitundlikkus toote komponentide või muude keemiliselt lähedaste ainete suhtes.
Fluoksetiini ei tohi võtta samaaegselt MAO inhibiitoritega (vt lõik 4.4 "Hoiatused ja ettevaatusabinõud kasutamisel" ja lõik 4.5 "Koostoimed teiste ravimitega ja muud koostoimed").
Üldiselt vastunäidustatud raseduse ajal (vt lõik 4.6 "Rasedus ja imetamine").
Ülitundlikkus fluoksetiini või ravimi ükskõik millise abiaine suhtes.
Monoamiini oksüdaasi inhibiitorid: Raskeid ja mõnikord surmaga lõppevaid reaktsioone on kirjeldatud patsientidel, kes kasutasid SSRI -sid kombinatsioonis monoamiini oksüdaasi inhibiitoriga (MAOI), ja patsientidel, kes olid hiljuti lõpetanud ravi SSRI -ga ja alustanud seda MAOI -ga. Ravi fluoksetiiniga tuleb alustada alles 2 nädalat pärast pöördumatu MAOI-ravi lõpetamist ja üks päev pärast pöörduva MAO-A lõpetamist.
Mõnel juhul on esinenud serotoniinisündroomile sarnaseid tunnuseid (mis võivad sarnaneda pahaloomulise neuroleptilise sündroomiga ja seda diagnoosida). Tsüproheptadiinist või dantroleenist võib selliste reaktsioonidega patsientidele kasu olla. Ravimi koostoime sümptomid MAOI -ga on järgmised: hüpertermia, jäikus, müokloonus, autonoomse närvisüsteemi ebastabiilsus koos võimalike kiirete elutähtsate kõikumistega, vaimse seisundi muutused, sealhulgas segasus, ärrituvus ja äärmine erutus, mis põhjustab deliiriumi ja kooma.
Seetõttu on fluoksetiin koos mitteselektiivse MAOI-ga vastunäidustatud. Samamoodi peaks pärast fluoksetiinravi katkestamist mööduma vähemalt 5 nädalat enne ravi alustamist MAOI -ga. Kui fluoksetiini määratakse pikaajaliselt ja / või suurtes annustes, tuleb kaaluda pikemat ajavahemikku.
Fluoksetiini ja pöörduva MAOI (nt moklobemiid) kombinatsiooni ei soovitata .. Fluoksetiinravi võib alustada järgmisel päeval pärast ravi lõpetamist pöörduva MAOI -ga.
04.4 Erihoiatused ja asjakohased ettevaatusabinõud kasutamisel
Erihoiatused ja ettevaatusabinõud kasutamisel
Hoiatused
Kasutamiseks lastele ja alla 18 -aastastele noorukitele
Enesetappudega seotud käitumist (enesetapukatse ja enesetapumõtted) ja vaenulikku suhtumist (eriti agressiivne, opositsiooniline ja vihakäitumine) täheldati sagedamini antidepressantidega ravitud laste ja noorukite kliinilistes uuringutes kui platseebot saanud patsientidel. Azur on ette nähtud kasutamiseks lastel ja noorukitel vanuses 8 kuni 18 aastat ainult mõõduka kuni raske depressiooni episoodide raviks ja seda ei tohi kasutada muude näidustuste korral. Kui meditsiinilise vajaduse põhjal tehakse otsus ravi kohta, tuleb patsienti hoolikalt jälgida enesetapumõjude ilmnemise suhtes. Lisaks on laste ja noorukite kohta pikaajalise mõju kohta ohutusele, sealhulgas mõju kasvule, seksuaalsele küpsemisele ja kognitiivsele, emotsionaalsele ja käitumuslikule arengule, saadaval ainult piiratud andmed (vt lõik 5.3).
19-nädalases kliinilises uuringus täheldati fluoksetiiniga ravitud lastel ja noorukitel pikkuse ja kehakaalu langust (vt lõik 4.8). Ei ole kindlaks tehtud, kas sellel on mõju täiskasvanu normaalsele pikkusele. Ei saa välistada puberteedi hilinemise võimalust (vt lõigud 5.3 ja 4.8). Seetõttu tuleb fluoksetiinravi ajal ja pärast seda jälgida puberteedi kasvu ja arengut (pikkus, kaal ja toimeetapid vastavalt TANNERile).Kui mõlemad on aeglustunud, tuleb nõuda pediaatrilist hindamist.
Laste kliinilistes uuringutes teatati sageli maaniast ja hüpomaaniast (vt lõik 4.8). Seetõttu on soovitatav regulaarselt jälgida maania / hüpomaania tekkimist. Maniakaalsesse faasi siseneva patsiendi puhul tuleb fluoksetiinravi katkestada.
On oluline, et arst arutaks hoolikalt lapse ja noore ja / või nende vanematega ravi riske ja kasu.
Nahalööve ja allergilised reaktsioonid: On teatatud lööbest, anafülaktoidsetest sündmustest ja progresseeruvatest süsteemsetest sündmustest, mõnikord tõsistest (naha, neerude, maksa või kopsude puhul). Nahalööbe või muude allergiliste nähtude ilmnemisel, mille puhul ei ole võimalik kindlaks teha erinevat etioloogiat, tuleb fluoksetiini manustamine lõpetada.
Ettevaatusabinõud
Krambid: krambid kujutavad endast potentsiaalset riski antidepressantide kasutamisel. Seetõttu, nagu ka teiste antidepressantide puhul, tuleb fluoksetiini manustada ettevaatusega patsientidele, kellel on esinenud krampe. Ravi tuleb katkestada kõigil patsientidel, kellel esinevad krambid või kellel on täheldatud krampide esinemissageduse suurenemist. Ebastabiilsete krambihoogude / epilepsiaga patsientidel tuleb fluoksetiini manustamist vältida ja kontrollitud epilepsiaga patsiente tuleb hoolikalt jälgida.
Mania: Antidepressante tuleb mania / hüpomaania anamneesiga patsientidel kasutada ettevaatusega. Nagu kõik antidepressandid, tuleb fluoksetiini kasutamine maniakaalsesse faasi sattunud patsientidel katkestada.
Maksa- / neerufunktsioonFluoksetiin metaboliseerub ulatuslikult maksas ja eritub neerude kaudu. Olulise maksafunktsiooni häirega patsientidel on soovitatav kasutada väiksemat annust 20 mg ööpäevas, nt. alternatiivne päevane annus. Kui 2 kuu jooksul manustati 20 mg fluoksetiini ööpäevas, olid raske neerukahjustusega patsiendid (GFR -dialüüs ei näidanud erinevusi fluoksetiini ega norfluoksetiini plasmatasemes võrreldes normaalse neerufunktsiooniga kontrollrühmaga).
Südamehaigus: 312 patsiendil, kes said topeltpimedate kliiniliste uuringute ajal fluoksetiini, ei täheldatud EKG-s ühtegi juhtivuse muutust, mis põhjustas südame seiskumist.
Siiski on ägeda südamehaiguse kliiniline kogemus piiratud ja soovitatav olla ettevaatlik.
KaalukaotusFluoksetiini võtvatel patsientidel võib tekkida kehakaalu langus, kuid see on tavaliselt proportsionaalne algkaaluga.
Diabeet: Diabeediga patsientidel võib SSRI -ravi halvendada glükeemilist kontrolli. Hüpoglükeemia tekkis fluoksetiinravi ajal, samas kui hüperglükeemia tekkis pärast ravimi kasutamise lõpetamist. Vajalikuks võib osutuda insuliini ja / või suukaudse hüpoglükeemilise aine annuse kohandamine.
Enesetapp / enesetapumõtted või kliiniline halvenemine: Depressioon on seotud enesetapumõtete, enesevigastamise ja enesetapu (suitsiidiga seotud sündmused) suurenenud riskiga. See oht püsib kuni haiguse märkimisväärse remissioonini. Kuna paranemine ei pruugi ilmneda esimestel või järgnevatel ravinädalatel, tuleb patsiente tähelepanelikult jälgida kuni paranemiseni. Üldine kliiniline kogemus näitab, et enesetapurisk võib paranemisprotsessi alguses suureneda.
Teised psühhiaatrilised seisundid, mille puhul Azur on välja kirjutatud, võivad olla seotud ka enesetapuga seotud sündmuste suurenenud riskiga. Lisaks võivad need seisundid kaasneda depressiooniga. Seetõttu tuleb rakendada samu ettevaatusabinõusid, mida järgitakse raske depressiooniga patsientide ravimisel ka teiste psühhiaatriliste häiretega patsientide ravimisel.
Patsientide seas, kellel on anamneesis suitsiidiga seotud juhtumeid, on patsientidel, kellel oli enne ravi alustamist märkimisväärne enesetapumõte, suurenenud risk enesetapumõteteks ja enesetapukatseteks ning neid tuleb ravi ajal hoolikalt jälgida. Kliiniliste uuringute metaanalüüs antidepressantidega võrreldes platseeboga psühhiaatriliste häirete ravis näitasid suitsidaalse käitumise riski suurenemist alla 25 -aastastel patsientidel, kes said antidepressante, võrreldes platseeboga.
Patsientide ja eriti kõrge riskiga patsientide hoolikas jälgimine peaks kaasnema ravimitega, eriti ravi algfaasis ja pärast annuse muutmist. Patsiente (või nende hooldajaid) tuleb teavitada vajadusest jälgida ja viivitamatult raviarstile teatada kliinilise pildi halvenemisest, enesetapukäitumise või -mõtete ilmnemisest või ebatavalistest muutustest käitumises, kui need sümptomid ilmnevad.
Akatisia / psühhomotoorne rahutus: Fluoksetiini kasutamist on seostatud akatiisia tekkega, mida iseloomustab "subjektiivselt ebameeldiv või murettekitav rahutus ja vajadus sageli liikuda, millega kaasneb" võimetus paigal istuda või seista. See esineb tõenäolisemalt esimestel ravinädalatel. Patsientidel, kellel tekivad need sümptomid, võib annuse suurendamine olla kahjulik.
SSRI -ravi katkestamisel täheldati võõrutusnähteRavi lõpetamisel on katkestamise sümptomid sagedased, eriti kui ravi lõpetatakse järsult (vt lõik 4.8 "Kõrvaltoimed"). Kliinilistes uuringutes esines ravi järsul katkestamisel täheldatud kõrvaltoimeid ligikaudu 60% -l patsientidest nii fluoksetiini kui ka platseeborühmas . Nendest kõrvaltoimetest olid 17% fluoksetiini rühmas ja 12% platseeborühmas tõsised.
Võõrutusnähtude risk võib sõltuda mitmest tegurist, sealhulgas ravi kestusest ja annusest ning annuse vähendamise kiirusest. Kõige sagedamini teatatud reaktsioonid on pearinglus, sensoorsed häired (sh paresteesia), unehäired (sh unetus ja intensiivsed unenäod), asteenia, erutus või ärevus, iiveldus ja / või oksendamine, värisemine ja peavalu. Üldiselt on need sümptomid kerged kuni mõõdukad, kuid mõnedel patsientidel võivad need olla tugevad. Need sümptomid tekivad tavaliselt esimestel päevadel pärast ravi lõpetamist. Üldiselt on need sümptomid iseenesest mööduvad ja taanduvad tavaliselt 2 nädala jooksul, kuigi mõnel inimesel võivad need pikeneda (2-3 kuud või kauem). Seetõttu soovitame Azuri väheneb vähemalt 1-2 nädala jooksul enne ravi katkestamist vastavalt patsiendi vajadusele (vt „Võõrutusnähud, mida on täheldatud Azur-ravi katkestamisel”, lõik 4.2 Annustamine ja manustamisviis).
VerejooksSSRI -de kasutamisel on teatatud nahaverejooksu ilmingutest, nagu ekhümoos ja purpur, Fluoksetiinravi ajal on harva esinenud ekhümoosi. Harva on teatatud muudest hemorraagilistest ilmingutest (nt günekoloogilised verejooksud, seedetrakti verejooks ja muu naha või limaskesta verejooks).
SSRI -sid kasutavatel patsientidel tuleb olla ettevaatlik, eriti samaaegsel kasutamisel suukaudsete antikoagulantidega, ravimitega, mis teadaolevalt mõjutavad trombotsüütide funktsiooni (nt ebatüüpilised antipsühhootikumid nagu klosapiin, fenotiasiinid, enamik tritsüklilisi antidepressante, aspiriin, MSPVA -d) või muud ravimid, mis võivad suurendada verejooksu riski , samuti patsientidel, kellel on esinenud verejooksu häireid.
Elektrokonvulsioonravi (ECT): Fluoksetiiniga ravitud patsientidel, kes saavad ECT-ravi, on harva teatatud krampide pikenemisest, seega on soovitatav olla ettevaatlik.
Naistepuna: Kui selektiivsed serotoniini tagasihaarde inhibiitorid ja naistepuna sisaldavad taimsed preparaadid (Hypericum perforatum) Kui neid kasutatakse koos, võib esineda suurenenud serotoniinergilist toimet, näiteks serotoniinisündroom.
Harvadel juhtudel on seoses fluoksetiinraviga teatatud serotoniinisündroomi või pahaloomulise neuroleptilise sündroomi sarnaste sündmuste tekkest, eriti kui fluoksetiini manustatakse koos teiste serotoniinergiliste ravimitega (muuhulgas L-trüptofaan) ja / või neuroleptikumidega. Kuna need sündroomid võivad tekitada patsiendile potentsiaalselt eluohtlikke seisundeid, võivad selliste sündmuste ilmnemisel tekkida (neid iseloomustavad sümptomite rühmad nagu hüpertermia, jäikus, müokloonus, autonoomse närvisüsteemi ebastabiilsus koos võimalike kiirete elutähtsate kõikumistega, segasus, ärrituvus ja äärmine erutus kuni deliiriumi ja koomani) ravi fluoksetiiniga tuleb katkestada ja alustada sümptomaatilist toetavat ravi.
04.5 Koostoimed teiste ravimitega ja muud koostoimed
Koostoimeuuringuid on läbi viidud ainult täiskasvanutel.
Pool elu: Farmakodünaamiliste või farmakokineetiliste koostoimete (nt fluoksetiinilt teisele üleminekul) kaalumisel tuleb arvestada nii fluoksetiini kui norfluoksetiini pika eliminatsiooni poolväärtusajaga (vt lõik 5.2 "Farmakokineetilised omadused").
Monoamiini oksüdaasi inhibiitorid: (vt lõik 4.3 "Vastunäidustused").
Kombinatsioone ei soovitata: MAOI-tüüp A (vt lõik 4.3).
Ühendused, mis nõuavad nende kasutamisel ettevaatusabinõusid:
MAOI-tüüp B (selegiliin): serotoniinisündroomi oht.Soovitatav on kliiniline jälgimine.
FenütoiinFluoksetiiniga kombineerimisel on täheldatud muutusi veres. Mõnel juhul on esinenud toksilisuse ilminguid. Seetõttu on soovitatav manustada fenütoiini vastavalt konservatiivsetele raviskeemidele ja hoolikalt jälgida patsiendi kliinilisi seisundeid.
Kesknärvisüsteemi ravimid: Fluoksetiini manustamine võib põhjustada karbamasepiini, haloperidooli, klosapiini, alprasolaami, imipramiini ja desipramiini taseme tõusu veres; mõnel juhul täheldati toksilisuse kliinilisi ilminguid. Seetõttu on soovitatav manustada samaaegselt kasutatavaid ravimeid vastavalt kaalutletud raviskeemidele ja järgida patsiendi kliinilisi seisundeid.
Diasepaam: Selle ravimi toime võib pikeneda.
Serotoniinergilised ravimid: Samaaegne manustamine serotoniinergiliste ravimitega (nt tramadool, triptaanid) võib suurendada serotoniinisündroomi tekke riski. Seos triptaanidega lisab täiendavat riski pärgarterite vasokonstriktsiooni ja arteriaalse hüpertensiooni tekkeks.
Liitium ja trüptofaan: On teatatud serotoniinisündroomist, kui SSRI -sid on manustatud kombinatsioonis liitiumi või trüptofaaniga ning seetõttu tuleb fluoksetiini samaaegsel kasutamisel nende ravimitega kasutada ettevaatusega. Kui fluoksetiini manustatakse koos liitiumiga, on vajalik sihipärasem ja sagedasem kliiniline jälgimine.
CYP2D6 isoensüümKuna fluoksetiini metabolism (nagu tritsükliliste antidepressantide ja teiste selektiivsete antidepressantide puhul serotoniini puhul) mõjutab maksa isoensümaatilist CYP2D6 süsteemi, võib samaaegne ravi sama ensüümsüsteemi kaudu metaboliseeritavate ravimitega põhjustada ravimite koostoimeid. Samaaegne ravi ravimitega, mida peamiselt metaboliseerib see isoensüüm ja mille terapeutiline indeks on piiratud (nt flekainiid, enkainiid, karbamasepiin ja tritsüklilised antidepressandid), tuleb alustada või kohandada väikseimast efektiivsest annusest. Seda tuleb teha isegi siis, kui fluoksetiini on võetud viimase 5 nädala jooksul.
Suukaudsed antikoagulandidPärast fluoksetiini ja suukaudsete antikoagulantide samaaegset manustamist on harva täheldatud muutunud antikoagulantide toimet (laboratoorsed andmed ja / või kliinilised sümptomid ja tunnused), mis ei sobi homogeensesse kategooriasse, kuid hõlmavad suurenenud verejooksu. Kui fluoksetiinravi alustatakse või lõpetatakse varfariini saavatel patsientidel, tuleb hoolikalt jälgida hüübimist (vt lõik 4.4 „Hoiatused ja ettevaatusabinõud kasutamisel“). Verejooks).
Elektrokonvulsioonravi (ECT): Fluoksetiiniga ravitud patsientidel, kes saavad ECT-ravi, on harva teatatud krampide pikenemisest, seega on soovitatav olla ettevaatlik.
Alkohol: Tavapäraste testide käigus ei põhjusta fluoksetiin vere alkoholisisalduse tõusu ega tugevda alkoholi toimet. SSRI ja alkoholravi kombinatsioon ei ole siiski soovitatav.
Naistepuna: Fluoksetiini ja naistepuna sisaldava taimse preparaadi vahel võivad tekkida farmakodünaamilised koostoimed (Hypericum perforatum), mis võib põhjustada serotoniinergiliste toimete suurenemist ja kõrvaltoimete suurenemist.
04.6 Rasedus ja imetamine
Rasedus:
Rasedatel ja imetavatel naistel peab arst Azur -ravi hoolikalt hindama ja ravimit kasutama ainult juhul, kui oodatav kasu õigustab võimalikku ohtu lootele.
Epidemioloogilised andmed näitavad suurenenud kardiovaskulaarsete defektide riski, mis on seotud fluoksetiini kasutamisega raseduse esimesel trimestril. Mehhanism on teadmata. Üldiselt näitavad andmed, et pärast ema fluoksetiiniga kokkupuudet on kardiovaskulaarsete defektidega lapse saamise oht suurusjärgus 2% võrreldes eeldatava samade defektide määraga üldpopulatsioonis umbes 1%.
Epidemioloogilised andmed näitavad, et SSRI-de kasutamine raseduse ajal, eriti raseduse lõpus, võib suurendada vastsündinu püsiva pulmonaalse hüpertensiooni (PPHN) riski. Täheldatud risk oli ligikaudu 5 rasedust 1000-st. Üldpopulatsioonis on 1- 2 püsiva pulmonaalse hüpertensiooni juhtu vastsündinutel iga 1000 lapseootel naise kohta.
Lisaks, kuigi fluoksetiini võib raseduse ajal kasutada, tuleb olla ettevaatlik, eriti raseduse hilises staadiumis või vahetult enne sünnituse algust, sest vastsündinutel on täheldatud järgmisi toimeid: ärrituvus, värisemine, hüpotoonia, püsiv nutt, imemisraskused või Need sümptomid võivad viidata nii serotonergilistele toimetele kui ka võõrutussündroomile. Nende sümptomite ilmnemise aeg ja kestus võivad olla seotud fluoksetiini ja selle aktiivse metaboliidi norfluoksetiini pika poolväärtusajaga (4–6 päeva). päeva).
ToitmisaegFluoksetiin ja selle aktiivne metaboliit norfluoksetiin erituvad teadaolevalt rinnapiima. Imetavatel imikutel on teatatud kõrvaltoimetest. Kui ravi fluoksetiiniga peetakse vajalikuks, tuleb kaaluda rinnaga toitmise katkestamist, kuid kui rinnaga toitmist jätkatakse, tuleb määrata madalaim efektiivne fluoksetiini annus.
04.7 Mõju autojuhtimise ja masinate käsitsemise võimele
Kuigi on tõestatud, et fluoksetiin ei häiri tervetel vabatahtlikel psühhomotoorset jõudlust, võib iga psühhoaktiivne ravim kahjustada otsustusvõimet või kutseoskusi. Patsiente tuleb soovitada vältida sõiduki juhtimist või ohtlike masinatega töötamist.
04.8 Kõrvaltoimed
Kõrvaltoimete intensiivsus ja esinemissagedus võivad ravi jätkamisel väheneda ega põhjusta tavaliselt ravi katkestamist.
Nagu teiste SSRI -de puhul, on täheldatud järgmisi kõrvaltoimeid:
Keha tervikuna: Ülitundlikkuse ilmingud (nt sügelus, lööve, urtikaaria, anafülaktoidne reaktsioon, vaskuliit, seerumitaoline reaktsioon, angioödeem) (vt lõik 4.3 "Vastunäidustused" ja lõik 4.4 "Hoiatused ja ettevaatusabinõud kasutamisel"), värinad, serotoniini sündroom, valgustundlikkus ja väga harva multiformne erüteem, mis võib areneda kuni Stevensi-Johnsoni sündroomi või toksilise epidermaalse nekrolüüsi (Lyelli sündroom) alguseni.
Seedeelundkond: Seedetrakti häired (nt kõhulahtisus, iiveldus, oksendamine, düspepsia, düsfaagia, muutunud maitse), suukuivus. Harva on teatatud ebanormaalsetest maksafunktsiooni testidest. Väga harvad idiosünkraatilise hepatiidi juhtumid.
Närvisüsteem: Peavalu, unehäired (nt ebanormaalsed unenäod, unetus, unisus), pearinglus, anoreksia, väsimus, unisus (nt unisus), eufooria, mööduvad ebanormaalsed liigutused (nt närvipuud, ataksia, värin, müokloonus), krambid ja harva psühhomotoorne rahutus / akatiisia (vt lõik 4.4 "Hoiatused ja ettevaatusabinõud kasutamisel"). Väga harva serotoniini sündroom.
Kardiovaskulaarne süsteem: Stenokardia, arütmia, 1. astme atrioventrikulaarne blokaad, hüpotensioon, hüpertensioon.
Psühhiaatrilised häired: Hallutsinatsioonid, maniakaalne reaktsioon, segasus, erutus, ärevus ja sellega seotud sümptomid (nt närvilisus), keskendumis- ja kognitiivsete protsesside halvenemine (nt depersonalisatsioon), paanikahood, enesetapukäitumine ja -mõtted (need sümptomid võivad olla tingitud mõnest haigusest).
Fluoksetiinravi ajal või varsti pärast ravi lõpetamist on teatatud enesetapumõtete ja suitsidaalse käitumise juhtudest (vt lõik 4.4).
Urogenitaalsüsteem: Uriinipeetus ja muutunud urineerimissagedus.
Reproduktiivse süsteemi häired: seksuaalne düsfunktsioon (ejakulatsiooni hilinemine või puudumine, anorgasmia), priapism, galaktorröa, hüperprolaktineemia.
Mitmesugused: Alopeetsia, haigutamine, nägemishäired (nt ähmane nägemine, müdriaas), higistamine, vasodilatatsioon, artralgia, müalgia, posturaalne hüpotensioon, ekhümoos, hüpoglükeemia, hüpokaleemia. Harva on teatatud muudest hemorraagilistest ilmingutest (nt günekoloogilised verejooksud, seedetrakti verejooks ja muu naha või limaskesta verejooks) (vt lõik 4.4 „Hoiatused ja ettevaatusabinõud kasutamisel“). Verejooks).
HüponatreemiaHarva on teatatud hüponatreemiast (sh naatriumisisaldus alla 110 mmol / l) ja see oli pöörduv fluoksetiini kasutamise lõpetamisel. Mõned juhtumid olid tõenäoliselt tingitud antidiureetilise hormooni sobimatu sekretsiooni sündroomist.Enamik teateid leiti eakatel patsientidel ja patsientidel, keda raviti diureetikumidega või kellel oli muul põhjusel vähenenud veremaht.
Hingamissüsteem: Farüngiit, düspnoe. Harva on teatatud kopsusündmustest (sealhulgas erineva histopatoloogiaga põletikulised protsessid ja / või fibroos). Hingeldus võib olla ainus hoiatav sümptom.
Luumurrud: Epidemioloogilised uuringud, mis viidi läbi peamiselt 50 -aastastel ja vanematel patsientidel, näitavad SSRI -de ja tritsükliliste antidepressantidega (TCA) ravitud patsientidel luumurdude riski suurenemist. Selle riski tekitamise mehhanism ei ole teada.
Fluoksetiinravi katkestamisel täheldati võõrutusnähte: Fluoksetiinravi katkestamine põhjustab tavaliselt võõrutusnähte. Kõige sagedamini teatatud reaktsioonid on pearinglus, sensoorsed häired (sh paresteesia), unehäired (sh unetus ja intensiivsed unenäod), asteenia, erutus või ärevus, iiveldus ja / või oksendamine, värisemine ja peavalu. Üldiselt on need sümptomid kerged kuni mõõdukad ja iseenesest piiravad, kuid mõnedel patsientidel võivad need olla rasked ja / või pikaajalised (vt lõik 4.4 „Hoiatused ja ettevaatusabinõud kasutamisel“). seetõttu on soovitatav annust vähendada, kui ravi Azuriga ei ole enam vajalik (vt lõik 4.2 "Annustamine ja manustamisviis" ja lõik 4.4 "Hoiatused ja ettevaatusabinõud kasutamisel").
Lapsed ja noorukid (vt lõik 4.4):
Laste kliinilistes uuringutes täheldati antidepressantidega ravitud lastel ja noorukitel enesetapuga seotud käitumist (enesetapukatse ja enesetapumõtted) ja vaenulikku suhtumist sagedamini kui platseebot saanud patsientidel.
Fluoksetiini ohutust ei ole süstemaatiliselt hinnatud kroonilise ravi korral, mis kestab kauem kui 19 nädalat.
Pediaatrilistes kliinilistes uuringutes teatati maniakaalsetest reaktsioonidest, sealhulgas maaniast ja hüpomaaniast (2,6% fluoksetiiniga ravitud patsientidel ja 0% platseebokontrolliga patsientidel), mis põhjustas enamikul juhtudel ravi katkestamise. Nendel patsientidel ei olnud varasemaid hüpomaania / maania episoode.
Pärast 19 -nädalast ravi teatasid kliinilises uuringus fluoksetiiniga ravitud pediaatrilised patsiendid keskmiselt 1,1 cm väiksema pikkusega (p = 0,004) ja 1,1 kg kaaluga (p = 0,008) võrreldes platseebot saanud patsientidega. Kliinilises kasutuses on teatatud ka üksikutest kasvupeetuse juhtudest.
Laste kliinilises kasutamises on teatatud üksikutest kõrvaltoimete juhtudest, mis võivad viidata seksuaalse küpsemise hilinemisele või seksuaalsele düsfunktsioonile (vt ka lõik 5.3).
Laste kliinilistes uuringutes seostati fluoksetiinravi leeliselise fosfataasi taseme langusega veres.
04.9 Üleannustamine
Ainuüksi fluoksetiini põhjustatud üleannustamise juhtumid on tavaliselt kerged. Üleannustamise sümptomiteks on iiveldus, oksendamine, krambid, kardiovaskulaarne düsfunktsioon, alates asümptomaatilisest arütmiast kuni südame seiskumiseni, kopsufunktsiooni häire ja muutused kesknärvisüsteemi seisundis, alates põnevusest kuni koomani. Surmav tulemus, mis on tingitud ainult fluoksetiini üleannustamisest, on olnud äärmiselt haruldane. südamefunktsiooni ja eluliste näitajate jälgimiseks, samuti üldised sümptomaatilised ja toetavad meetmed Spetsiifilisi antidoote pole teada.
Sunnitud diurees, dialüüs, hemoperfusioon ja asendusülekanne tõenäoliselt kasu ei too. Aktiivsüsi, mida saab kasutada koos sorbitooliga, võib olla isegi tõhusam ravi kui oksendamine või maoloputus. Üleannustamise ravimisel kaaluge mitmete ravimite kaasamise võimalust. Patsientidel, kes on võtnud liiga palju tritsüklilist antidepressanti, võib olla vajalik pikem ajavahemik hoolikaks meditsiiniliseks jälgimiseks, kui nad võtavad või on hiljuti kasutanud fluoksetiini.
05.0 FARMAKOLOOGILISED OMADUSED
05.1 Farmakodünaamilised omadused
ATC -kood: N06AB03
Fluoksetiin (INN) on selektiivne serotoniini tagasihaarde inhibiitor.
Fluoksetiin on mittetritsüklilise struktuuriga (±) -N-metüül-3-fenüül-3-[(a, a, a, -trifluoro-p-tolüül) -oksü] -propüülamiinvesinikkloriid, mille antidepressantide toime on eeldatavasti seotud serotoniini omastamise pärssimine keskneuronites Inimese trombotsüütide uuringutes on näidatud, et fluoksetiin blokeerib serotoniini omastamist trombotsüütidesse.
Loomkatsed näitavad ka, et fluoksetiinil on palju tugevam pärssiv toime serotoniini omastamisele kui teiste monoamiinide omastamisele.
On oletatud, et klassikaliste tritsükliliste antidepressantide erinevate antikolinergiliste ja kardiovaskulaarsete toimete eest vastutab "antagonistlik toime muskariin-, histamiini- ja alfa1-adrenergilistele retseptoritele. Fluoksetiin seondub nende ja teiste membraaniretseptoritega palju vähem kui tritsüklilised ravimid.
05.2 Farmakokineetilised omadused
Imendumine pärast suukaudset manustamist on kiire ja täielik.Inimestel täheldatakse pärast 40 mg ühekordset annust 6 ... 8 tunni pärast fluoksetiini plasmakontsentratsioone vahemikus 15 kuni 55 ng / ml.
Fluoksetiini preparaadid kapslites, lahustuvates tablettides ja suukaudseks manustamiseks mõeldud lahuses on bioekvivalentsed.
Fluoksetiini võib manustada koos toiduga või ilma, sest toit ei muuda süsteemset biosaadavust, kuigi võib imendumist veidi aeglustada.
Fluoksetiin metaboliseerub maksas peamiselt norfluoksetiiniks ja teisteks mitteaktiivseteks metaboliitideks, mis seejärel erituvad neerude kaudu.
Fluoksetiin on organismis laialt levinud ja seondub ulatuslikult plasmavalkudega.
Fluoksetiini eliminatsiooni poolväärtusaeg on 4-6 päeva, samas kui selle aktiivsel metaboliidil on 4-16 päeva (need väärtused võivad P450IID6 ensüümsüsteemi puudulikkusega patsientidel veelgi pikeneda). Selle tulemuseks on märkimisväärne kumulatsioon neist kroonilise kasutusega aktiivsed tooted. Tasakaalukontsentratsioon plasmas saavutatakse alles pärast nädalast ravi.
Järgnev tabel võtab kokku kõige olulisemad farmakokineetilised omadused.
* Neid väärtusi võib veelgi pikendada patsientidel, kellel on ensüümsüsteemi P450IID6 puudulikkus.
Maksapuudulikkuse esinemine võib takistada fluoksetiini eliminatsiooni.
Raske neerupuudulikkusega patsientidel võib fluoksetiin või selle metaboliidid veelgi kuhjuda.
05.3 Prekliinilised ohutusandmed
Nii fluoksetiin kui ka selle aktiivne metaboliit norfluoksetiin näitasid erinevates loomaliikides, sealhulgas primaatides, ühe- ja korduvannuse, alaägeda ja kroonilise toksilisuse testides kõrget taluvust.
Ägeda manustamise korral olid LD50 (mg / kg) järgmised:
Mürgiseid nähtusi põhjustavad ägedad annused on mitu korda suuremad kui inimeste terapeutilised annused (0,3–1,0 mg / kg päevas). Kroonilise toksilisuse testides leitud mis tahes toksilist toimet (anoreksia, kehakaalu langus, fosfolipidoos mõnedel loomaliikidel) on ravi katkestamisel on pöörduv.
Reproduktsiooniuuringud: Fluoksetiin ei mõjuta testitud annustes fertiilsust ja reproduktiivvõimet.
Teratogeensed uuringud: Fluoksetiin ei mõjuta negatiivselt sünnieelset arengut ega loote kaalu ning olulisi teratogeenseid toimeid ei ole täheldatud.
Mutageensuse uuringud: Fluoksetiin ja norfluoksetiin ei sisalda mutageenseid toimeid nii in vitro kui ka in vivo.
Kantserogeensusuuringud: keskmiste annuste puhul, mis olid ligikaudu 10 korda suuremad kui inimese kavandatud ööpäevane annus 2 aasta jooksul, ei täheldatud rottidel ja hiirtel kantserogeenset toimet.
06.0 FARMATSEUTILINE TEAVE
06.1 Abiained
Maisitärklis, dimetikoon, želatiin, titaandioksiid.
06.2 Sobimatus
Ärge teatage.
06.3 Kehtivusaeg
2 aastat.
06.4 Säilitamise eritingimused
Hoida temperatuuril kuni 30 ° C.
06.5 Vahetu pakendi iseloomustus ja pakendi sisu
Litograafiline pappkarp 28 kapsliga, mis sisaldab 1 pakendi infolehte.
06.6 Kasutamis- ja käsitsemisjuhised
Ei mingeid erijuhiseid
07.0 MÜÜGILOA HOIDJA
BIORES ITALIA S.r.l. "Via Vittorio Grassi n. 13." 00155 Rooma
08.0 MÜÜGILOA NUMBER
AZUR 20 mg kapslid. "28 kapslit A.I.C. nr: 034375030
09.0 MÜÜGILOA VÕI UUENDAMISE KUUPÄEV
22.11.2000
10.0 TEKSTI LÄBIVAATAMISE KUUPÄEV
Mai 2011