Toimeained: emtritsitabiin, rilpiviriin, tenofoviirdisoproksiil
Eviplera 200 mg / 25 mg / 245 mg õhukese polümeerikattega tabletid
Miks Eviplerat kasutatakse? Milleks see mõeldud on?
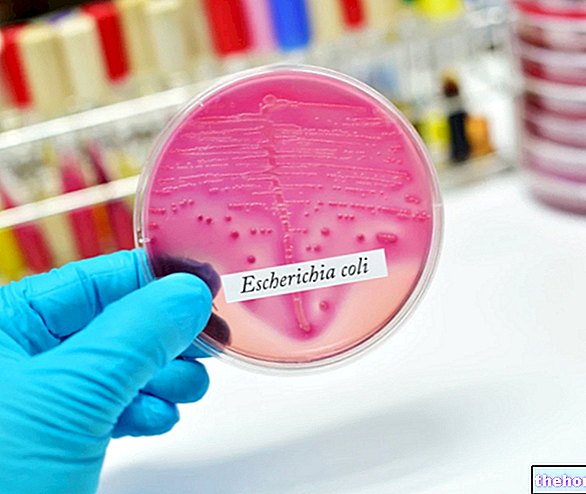
Eviplera sisaldab kolme toimeainet, mida kasutatakse inimese immuunpuudulikkuse viiruse (HIV) infektsiooni raviks:
- emtritsitabiin, nukleosiidi pöördtranskriptaasi inhibiitor (NRTI).
- rilpiviriin, mitte-nukleosiidne pöördtranskriptaasi inhibiitor (NNRTI).
- tenofoviirdisoproksiil, nukleotiidne pöördtranskriptaasi inhibiitor (NtRTI).
Kõik need toimeained, mida tuntakse ka retroviirusevastaste ravimitena, mõjutavad ensüümi (valku, mida nimetatakse pöördtranskriptaasiks), mis on viiruse paljunemiseks hädavajalik.
Eviplera vähendab HIV-i kogust organismis. Sel viisil parandab see immuunsüsteemi ja vähendab HIV-iga seotud haiguste tekkimise riski.
Eviplera on inimese immuunpuudulikkuse viiruse (HIV) infektsiooni ravi täiskasvanutel vanuses 18 aastat ja rohkem.
Vastunäidustused Kui Eviplerat ei tohi kasutada
Ärge võtke Eviplerat
- Kui olete emtritsitabiini, rilpiviriini, tenofoviirdisoproksiili või selle ravimi mis tahes koostisosade (loetletud lõigus 6) suhtes allergiline.
Kui see kehtib teie kohta, rääkige sellest kohe oma arstile.
- Kui te võtate praegu mõnda neist ravimitest:
- karbamasepiin, okskarbasepiin, fenobarbitaal ja fenütoiin (ravimid, mida kasutatakse epilepsia raviks ja krampide ennetamiseks)
- rifampitsiin ja rifapentiin (kasutatakse teatud bakteriaalsete infektsioonide, näiteks tuberkuloosi raviks)
- omeprasool, lansoprasool, rabeprasool, pantoprasool ja esomeprasool (prootonpumba inhibiitorid, mida kasutatakse maohaavandite, kõrvetiste ja happe refluksi ennetamiseks ja raviks)
- deksametasoon (kortikosteroid, mida kasutatakse põletiku raviks ja immuunsüsteemi pärssimiseks) suu kaudu või süstituna (välja arvatud ühekordse annuse korral)
- naistepuna (Hypericum perforatum) sisaldavad ravimid (taimne ravim, mida kasutatakse depressiooni ja ärevuse korral)
Ettevaatusabinõud kasutamisel Mida on vaja teada enne Eviplera võtmist
Eviplera võtmise ajal peab arst teid jätkuvalt jälgima.
- Selle ravimi võtmise ajal saate HIV -i edasi anda, kuigi retroviirusevastase ravi mõju vähendab riski. Arutage oma arstiga vajalikke ettevaatusabinõusid, et vältida nakkuse edasikandumist teistele inimestele.See ravim ei ravi HIV -nakkust. Eviplera võtmise ajal võivad teil endiselt tekkida infektsioonid või muud HIV -nakkusega seotud haigused.
- Rääkige oma arstile, kui teil on olnud neeruhaigus või kui testid on näidanud neeruprobleeme. Eviplera võib mõjutada neere. Enne ravi alustamist ja ravi ajal võib arst tellida neerufunktsiooni mõõtmiseks vereanalüüse. Eviplerat ei soovitata kasutada, kui teil on mõõdukas kuni raske neeruhaigus.
Eviplerat ei tohi võtta koos teiste ravimitega, mis võivad kahjustada neere (vt Muud ravimid ja Eviplera). Kui see on vältimatu, jälgib arst kord nädalas teie neerufunktsiooni.
- Rääkige oma arstile, kui teil on anamneesis maksahaigus, sealhulgas hepatiit. HIV-nakkusega patsientidel, kellel on maksahaigus (sh krooniline B- või C-hepatiit) ja keda ravitakse retroviirusevastaste ravimitega, on suurem oht tõsisteks tüsistusteks ja potentsiaalselt surmavaks maksale. Kui teil on B -hepatiit, kaalub teie arst hoolikalt, milline raviskeem teile kõige paremini sobib. Kaks Eviplera toimeainet (tenofoviirdisoproksiil ja emtritsitabiin) näitavad teatud toimet B -hepatiidi viiruse, maksa või kroonilise B -hepatiidi infektsiooni vastu. arst võib määrata maksafunktsiooni jälgimiseks vereanalüüse.
Kui teil on B -hepatiit, võivad maksaprobleemid pärast Eviplera kasutamise lõpetamist süveneda. Oluline on mitte lõpetada Eviplera võtmine ilma arstiga nõu pidamata: vt lõik 3, Ärge lõpetage Eviplera võtmist.
- Rääkige kohe oma arstile ja lõpetage Eviplera võtmine, kui teil tekivad lööbed koos järgmiste sümptomitega: palavik, villid, punased silmad ja näo, suu või keha turse. See reaktsioon võib muutuda tõsiseks või potentsiaalselt eluohtlikuks. Rääkige oma arstile, kui teil tekib olete üle 65 -aastane. Eviplerat ei ole uuritud piisavalt üle 65 -aastastel patsientidel. Kui te olete üle 65 -aastane ja teile on määratud Eviplera, jälgib teie arst teid hoolikalt.
Eviplera võtmise ajal
Kui alustate Eviplera võtmist, olge ettevaatlik:
- mis tahes põletiku või infektsiooni tunnused
- luuprobleemid
Kui märkate mõnda neist sümptomitest, rääkige sellest kohe oma arstile.
Lapsed ja noorukid
Ärge andke seda ravimit lastele ja alla 18 -aastastele noorukitele.
Koostoimed Millised ravimid või toidud võivad muuta Eviplera toimet
Teatage oma arstile või apteekrile, kui te kasutate, olete hiljuti kasutanud või kavatsete kasutada mis tahes muid ravimeid, kaasa arvatud ilma retseptita ostetud ravimeid ja taimseid ravimeid.
Öelge oma arstile, kui te võtate mõnda järgmistest ravimitest:
- Muud ravimid, mis sisaldavad:
- emtritsitabiin
- rilpiviriin
- tenofoviirdisoproksiil
- tenofoviir -alafenamiid
- mis tahes muud viirusevastased ravimid, mis sisaldavad lamivudiini või adefoviirdipivoksiili
Eviplera võib suhelda teiste ravimitega. Seetõttu võib Eviplera või teiste ravimite kogus veres muutuda. See võib takistada ravimite nõuetekohast toimimist või halvendada nende kõrvaltoimeid. Mõnel juhul võib arst vajada teie annuse kohandamist või vere taseme kontrollimist.
- Ravimid, mis võivad kahjustada neere, näiteks:
- aminoglükosiidid (nt streptomütsiin, neomütsiin ja gentamütsiin), vankomütsiin (bakteriaalsete infektsioonide korral)
- foskarnet, gantsükloviir, tsidofoviir (viirusnakkuste korral)
- amfoteritsiin B, pentamidiin (seeninfektsioonide raviks)
- interleukiin-2, mida nimetatakse ka aldesleukiiniks (vähi raviks)
- mittesteroidsed põletikuvastased ravimid (MSPVA-d, kasutatakse luu- või lihasvalu leevendamiseks)
- Didanosiini sisaldavad ravimid (HIV -nakkuse korral): Eviplera võtmine koos teiste didanosiini sisaldavate viirusevastaste ravimitega võib suurendada didanosiini taset veres ja vähendada CD4 -rakkude arvu. Kui tenofoviirdisoproksiilfumaraati ja didanosiini sisaldavaid ravimeid on koos võetud, on harvad teated kõhunäärmepõletikust ja piimhappe atsidoosist (piimhappe liig veres), mis mõnikord lõppes surmaga. Arst peab väga ettevaatlikult kaaluma, kas ravida teid teiste nakkuse raviks kasutatavate ravimitega (vt lõik HIV -nakkuse ravimid).
- Muud HIV-nakkuse ravimid: mittenukleosiidsed pöördtranskriptaasi inhibiitorid (NNRTI-d). Eviplera sisaldab NNRTI-d (rilpiviriini) ja seetõttu ei tohi seda kombineerida teiste seda tüüpi ravimitega. Arst hindab teistsuguse ravimi kasutamist. vajalik.
- Rifabutiin, ravim, mida kasutatakse teatud bakteriaalsete infektsioonide raviks. See ravim võib vähendada rilpiviriini (Eviplera koostisosa) sisaldust veres. Teie arst võib HIV -nakkuse raviks anda teile täiendava annuse rilpiviriini (vt lõik 3 Kuidas Eviplerat võtta)
- Bakteriaalsete infektsioonide, sealhulgas tuberkuloosi raviks kasutatavad antibiootikumid, mis sisaldavad:
- klaritromütsiin
- erütromütsiin Need ravimid võivad suurendada rilpiviriini (Eviplera koostisosa) sisaldust veres. Arst võib muuta teie antibiootikumi annust või määrata teile teise antibiootikumi.
- Ravimid maohaavandite, kõrvetiste või happe refluksi vastu, näiteks:
- antatsiidid (alumiinium / magneesiumhüdroksiid või kaltsiumkarbonaat)
- H2 antagonistid (famotidiin, tsimetidiin, nisatidiin või ranitidiin) Need ravimid võivad vähendada rilpiviriini (Eviplera koostisosa) sisaldust veres. Kui te võtate mõnda neist ravimitest, määrab arst teile teistsuguse ravimi maohaavandite, kõrvetiste või happe refluksi vastu või annab nõu, kuidas ja millal seda ravimit võtta.
- Kui te võtate antatsiidi (nt magneesiumi või kaaliumi sisaldavad ravimid), võtke see vähemalt 2 tundi enne või vähemalt 4 tundi pärast Eviplera kasutamist (vt lõik 3 Kuidas Eviplera't võtta).
- Kui te võtate H2 antagonisti (kasutatakse ka maohappe või reflukshaiguse raviks), võtke see vähemalt 12 tundi enne või vähemalt 4 tundi pärast Eviplera kasutamist. H2 antagoniste võib võtta ainult üks kord päevas koos Eviplera H2 antagonistidega ei tohi võtta kaks korda päevas Rääkige oma arstiga alternatiivse annustamisskeemi kohta (vt lõik 3 Kuidas Eviplera't võtta).
- Metadoon, ravim, mida kasutatakse opiaadisõltuvuse raviks, kuna arst võib vajada metadooni annuse muutmist.
- Dabigatraaneteksilaat, ravim, mida kasutatakse südameprobleemide raviks, kuna arstil võib tekkida vajadus jälgida selle ravimi taset veres.
Rääkige oma arstile, kui te võtate mõnda neist ravimitest. Ärge lõpetage ravi ilma arstiga ühendust võtmata.
Hoiatused Oluline on teada, et:
Rasedus ja imetamine
Enne mis tahes ravimi kasutamist pidage nõu oma arsti või apteekriga.
- Naised ei tohi Eviplera võtmise ajal rase olla.
- Kasutage Eviplera võtmise ajal tõhusaid rasestumisvastaseid vahendeid.
- Rääkige oma arstile kohe, kui olete rase. Rasedad naised ei tohi Eviplerat võtta, välja arvatud juhul, kui arst otsustab koos nendega, et see on hädavajalik. Arst arutab teiega Eviplera võtmise võimalikku kasu ja riske teile ja teie lapsele.
- Kui te olete juba raseduse ajal Eviplera't võtnud, võib arst regulaarselt nõuda vereanalüüse ja muid diagnostilisi teste, et jälgida lapse arengut. Lastel, kelle emad võtsid raseduse ajal NRTI -sid, kaalus HIV -kaitse kasu üles kõrvaltoimete riski.
Ärge imetage Eviplera võtmise ajal:
- Põhjus on selles, et selle ravimi toimeaine eritub rinnapiima.
- Kui olete HIV-nakkusega naine, soovitatakse last rinnaga mitte toita, et vältida HIV-viiruse kandumist lapsele piima kaudu.
Autojuhtimine ja masinatega töötamine
Ärge juhtige autot ega töötage masinatega, kui olete pärast ravimi võtmist väsinud, unine või uimane. Eviplera sisaldab laktoosi ja kollakasoranži alumiiniumlaki (E110)
- Rääkige oma arstile, kui teil on "laktoosi või muude suhkrute talumatus. Eviplera sisaldab laktoosmonohüdraati. Kui teil on laktoositalumatus või kui arst on teile öelnud, et te ei talu teisi suhkruid, võtke enne selle ravimi kasutamist ühendust oma arstiga.
- Öelge oma arstile, kui teil on allergia kollase oranži alumiiniumlaki (E110) suhtes. Eviplera sisaldab kollakasoranži alumiiniumlakki, mida nimetatakse ka "E110" ja mis võib põhjustada allergilisi reaktsioone.
Annus, manustamisviis ja aeg Kuidas Eviplerat kasutada: Annustamine
Võtke seda ravimit alati täpselt nii, nagu arst on teile rääkinud. Kahtluse korral pidage nõu oma arsti või apteekriga.
Tavaline annus on üks tablett päevas suu kaudu. Tablett tuleb võtta koos toiduga. See on oluline toimeaine õige taseme saavutamiseks kehas.
Toitumisjook üksi ei asenda toitu.
Neelake tablett alla tervelt koos vähese veega.
Ärge närige, purustage ega purustage tabletti, vastasel juhul mõjutab see seda, kuidas ravim teie kehasse vabaneb.
Kui teie arst otsustab Eviplera mõne komponendi katkestada või Eviplera annust muuta, võidakse teile eraldi manustada emtritsitabiini, rilpiviriini ja / või tenofoviirdisoproksiili või koos teiste HIV -infektsiooni ravimitega.
Kui te võtate antatsiidi, näiteks magneesiumi või kaaliumi sisaldavaid ravimeid. Võtke seda vähemalt 2 tundi enne või vähemalt 4 tundi pärast Eviplera võtmist.
Kui te võtate H2 antagonisti, näiteks famotidiini, tsimetidiini, nisatidiini või ranitidiini. Võtke seda vähemalt 12 tundi enne või vähemalt 4 tundi pärast Eviplera võtmist. H2 antagoniste võib võtta koos Evipleraga ainult üks kord päevas. H2 antagoniste ei tohi võtta kaks korda päevas. Rääkige oma arstiga alternatiivse annustamisskeemi kohta.
Kui te võtate rifabutiini. Arst võib teile anda täiendava annuse rilpiviriini. Võtke rilpiviriini tablett samaaegselt Eviplera võtmisega. Kahtluse korral pidage nõu oma arsti või apteekriga.
Kui te unustate Eviplera't võtta
On oluline, et te ei jätaks Eviplera annust vahele.
Kui te unustate annuse:
- Kui märkate seda 12 tunni jooksul pärast Eviplera tavapärast võtmise aega, peate tableti võtma niipea kui võimalik. Võtke tablett alati koos toiduga. Seejärel võtke järgmine annus nagu tavaliselt.
- Kui märkate seda 12 tunni või rohkem pärast Eviplera tavapärast võtmist, ärge võtke vahelejäänud annust. Oodake ja võtke järgmine annus koos toiduga tavalisel ajal.
Kui 4 tunni jooksul pärast Eviplera võtmist tekib oksendamine, võtke teine tablett koos toiduga. Kui te oksendate rohkem kui 4 tundi pärast Eviplera võtmist, siis ärge võtke uut tabletti enne järgmist regulaarselt planeeritud tabletti. Ärge lõpetage Eviplera võtmist.
Ärge lõpetage Eviplera võtmist ilma arstiga nõu pidamata.
Eviplera -ravi lõpetamine võib tõsiselt mõjutada teie reaktsiooni järgnevale ravile. Kui teie Eviplera -ravi mingil põhjusel katkestatakse, pidage enne Eviplera tablettide taasalustamist nõu oma arstiga. Arst võib teile anda Eviplera koostisosi. Kui teil on probleeme või annust kohandada.
Kui Eviplera varud hakkavad otsa saama, hankige oma arstilt või apteekrilt rohkem. See on väga oluline, sest viiruse hulk võib hakata kasvama, kui ravim peatatakse isegi lühiajaliselt. Viiruse ravi võib muutuda raskemaks.
Kui teil on nii HIV kui ka B -hepatiidi infektsioon, on eriti oluline mitte lõpetada ravi Evipleraga, ilma et oleksite eelnevalt oma arstiga ühendust võtnud. Mõnedel patsientidel on hepatiit süvenenud, millele viitavad sümptomid või vereanalüüsid pärast emtritsitabiini või tenofoviirdisoproksiilfumaraadi (kaks Eviplera kolmest toimeainest) kasutamise lõpetamist. Kui Eviplera kasutamine lõpetatakse, võib arst soovitada teil jätkata B -hepatiidi ravi. Võimalik, et maksafunktsiooni kontrollimiseks tuleb 4 kuu jooksul pärast ravi lõpetamist teha vereanalüüse. Mõnel kaugelearenenud maksahaiguse või tsirroosiga patsiendil ei ole soovitatav ravi katkestada, kuna see võib põhjustada hepatiidi ägenemist, mis võib olla eluohtlik.
Teatage kohe oma arstile kõigist uutest või ebatavalistest sümptomitest, mida on täheldatud pärast ravi lõpetamist, eriti sümptomitest, mis on tavaliselt seotud B -hepatiidi infektsiooniga.
Kui teil on lisaküsimusi selle ravimi kasutamise kohta, pidage nõu oma arsti või apteekriga.
Üleannustamine Mida teha, kui olete võtnud liiga palju Eviplera’t
Kui te võtate kogemata rohkem kui soovitatav Eviplera annus, võib teil olla suurem risk selle ravimi võimalike kõrvaltoimete tekkeks (vt lõik 4, Võimalikud kõrvaltoimed).
Võtke kohe ühendust oma arstiga või lähima hädaabikeskusega. Võtke pudel tablette kaasa, et saaksite hõlpsalt kirjeldada, mida olete võtnud.
Kõrvaltoimed Millised on Eviplera kõrvaltoimed
Nagu kõik ravimid, võib ka see ravim põhjustada kõrvaltoimeid, kuigi kõigil neid ei teki.
Võimalikud kõrvaltoimed: Rääkige sellest kohe oma arstile
- Laktatsidoos (piimhappe liig veres) on mõnede HIV-ravimite haruldane, kuid potentsiaalselt eluohtlik kõrvaltoime. Laktatsidoosi esineb sagedamini naistel, eriti kui nad on ülekaalulised, ja maksahaigusega inimestel. Järgmised võivad olla laktatsidoosi tunnused:
- sügav, kiire hingamine
- väsimus või unisus
- iiveldus, oksendamine
- kõhuvalu
Kui arvate, et teil võib olla laktatsidoos, rääkige sellest kohe oma arstile.
Põletiku või infektsiooni tunnused. Mõnel kaugelearenenud HIV-nakkusega (AIDS) patsiendil, kellel on esinenud oportunistlikke infektsioone (nõrga immuunsüsteemiga inimestel esinevad infektsioonid), võivad infektsioonipõletiku nähud ja sümptomid ilmneda peagi pärast HIV-vastase ravi alustamist. arvatavasti on see tingitud organismi immuunvastuse paranemisest, mis võimaldab tal võidelda infektsioonidega, mis võivad esineda ilma ilmsete sümptomiteta.
Lisaks oportunistlikele infektsioonidele võivad autoimmuunhäired (seisund, mis tekib siis, kui immuunsüsteem ründab tervet kehakude) tekkida ka pärast seda, kui hakkate kasutama HIV -nakkuse raviks mõeldud ravimeid. Autoimmuunhaigused võivad tekkida ka mitu kuud pärast ravi alustamist. Kui märkate infektsiooni sümptomeid või muid sümptomeid, nagu lihasnõrkus, esmane nõrkus kätes ja jalgades, mis liiguvad pagasiruumi, südamepekslemine, värisemine või hüperaktiivsus, rääkige sellest kohe oma arstile, et otsida vajalikku ravi.
Kui märkate põletiku või infektsiooni sümptomeid, rääkige sellest kohe oma arstile.
Väga sageli esinevad kõrvaltoimed (kõrvaltoimed esinevad rohkem kui ühel patsiendil 10 -st)
- kõhulahtisus, oksendamine, iiveldus
- unehäired (unetus)
- pearinglus, peavalu
- lööve
- nõrkuse tunne
Analüüsid võivad näidata ka järgmist:
- vere fosfaatide taseme langus
- kreatiinkinaasi taseme tõus veres, mis võib põhjustada lihasvalu ja nõrkust
- suurenenud kolesterooli ja / või pankrease amülaasi sisaldus veres
- maksaensüümide taseme tõus veres
- Kui mõni neist kõrvaltoimetest muutub tõsiseks, rääkige sellest oma arstile.
Sageli esinevad kõrvaltoimed (kõrvaltoimed esinevad vähem kui 1 patsiendil 10 -st)
- vähenenud söögiisu
- depressioon ja depressiivne meeleolu
- väsimus, unisus
- unisus
- kõhuvalu, valu või ebamugavustunne, puhitus, suukuivus
- ebanormaalsed unenäod, unehäired
- seedimisprobleemid pärast halba enesetunnet pärast sööki, gaasid (gaasid)
- nahalööbed (sh punased laigud või pustulid, millega mõnikord kaasneb villide teke ja naha turse), mis võivad olla allergilised reaktsioonid, sügelus, nahavärvi muutus tumedate laikude tekkimisel
- muud allergilised reaktsioonid, nagu vilistav hingamine, puhitus või peapööritus
Analüüsid võivad näidata ka järgmist:
- valgete vereliblede arvu vähenemine (see võib muuta teid nakkustele vastuvõtlikumaks)
- trombotsüütide arvu vähenemine (teatud tüüpi vererakud, mis osalevad vere hüübimises)
- hemoglobiini vähenemine veres (madal punaste vereliblede arv)
- suurenenud rasvhapete (triglütseriidide), bilirubiini või veresuhkru sisaldus
- kõhunäärme probleemid
Kui mõni neist kõrvaltoimetest muutub tõsiseks, rääkige sellest oma arstile.
Aeg -ajalt esinevad kõrvaltoimed (kõrvaltoimed esinevad vähem kui ühel patsiendil 100 -st)
- aneemia (madal punaste vereliblede arv)
- kõhuvalu, mis on põhjustatud kõhunäärmepõletikust
- lihaste lagunemine, lihasvalu või lihasnõrkus
- näo, huulte, keele või kõri turse
- põletiku või infektsiooni nähud või sümptomid
- rasked nahareaktsioonid, sealhulgas lööve, millega kaasneb palavik, turse ja maksaprobleemid
- neerutorukeste rakkude kahjustus
Analüüsid võivad näidata ka järgmist:
- kaaliumi sisalduse vähenemine veres
- kreatiniini taseme tõus veres
- muutused uriinis
- Kui mõni neist kõrvaltoimetest muutub tõsiseks, rääkige sellest oma arstile.
Harva esinevad kõrvaltoimed (need toimed esinevad vähem kui ühel patsiendil 1000 -st)
- laktatsidoos (vt Võimalikud kõrvaltoimed; rääkige sellest kohe arstile)
- seljavalu, mis on põhjustatud neeruprobleemidest, sealhulgas neerupuudulikkusest. Teie arst võib tellida vereanalüüse, et näha, kas teie neerud töötavad korralikult
- rasvmaks
- naha ja silmade kollasus, sügelus või kõhuvalu, mis on põhjustatud maksapõletikust
- neerupõletik, raske uriin ja janu
- luude pehmenemine (koos luuvalu ja mõnikord luumurdudega)
- Neerude torukujuliste rakkude kahjustuse tõttu võivad tekkida lihaste lagunemine, luude pehmenemine (koos luuvalu ja mõnikord luumurdudega), lihasvalu, lihasnõrkus ja kaaliumi või fosfaadi sisalduse vähenemine veres.
Kui mõni neist kõrvaltoimetest muutub tõsiseks, rääkige sellest oma arstile.
Muud mõjud, mis võivad tekkida HIV -ravi ajal
Järgmiste kõrvaltoimete esinemissagedus ei ole teada (esinemissagedust ei saa hinnata olemasolevate andmete alusel).
- Probleemid luudega. Mõnedel kombineeritud retroviirusevastaseid ravimeid, näiteks Eviplera võtvatel patsientidel võib tekkida luuhaigus, mida nimetatakse osteonekroosiks (luukoe surm, mis on tingitud luu verevarustuse vähenemisest). Seda tüüpi ravimite pikaajaline kasutamine, kortikosteroidide võtmine, alkoholi joomine, nõrk immuunsüsteem ja ülekaalulisus võivad olla mõned selle haiguse tekkimise riskifaktoritest. Osteonekroosi sümptomid on järgmised:
- liigeste jäikus
- liigesevalud (eriti puusades, põlvedes ja õlgades)
- liikumisraskused
Kui märkate mõnda neist sümptomitest, rääkige sellest palun oma arstile.
HIV -ravi ajal võib esineda kehakaalu ning vere lipiidide ja glükoosisisalduse suurenemist, mis on osaliselt seotud tervise ja elustiili taastumisega ning vere lipiidide puhul mõnikord samade HIV -vastaste ravimitega. Arst kontrollib neid muutusi.
Kõrvaltoimetest teatamine
Kui teil tekib ükskõik milline kõrvaltoime, pidage nõu oma arsti või apteekriga, sealhulgas selles infolehes loetlemata. Kõrvaltoimetest võite ka ise teavitada riikliku teavitussüsteemi kaudu, mis on loetletud lisas V. Kõrvaltoimetest teatades saate aidata saada rohkem teavet selle ravimi ohutuse kohta.
Aegumine ja säilitamine
Hoidke seda ravimit laste eest varjatud ja kättesaamatus kohas.
Ärge kasutage seda ravimit pärast kõlblikkusaega, mis on märgitud pudelil ja karbil pärast {EXP}. Kõlblikkusaeg viitab selle kuu viimasele päevale.
Hoida originaalpakendis, niiskuse eest kaitstult.
Ärge visake ravimeid kanalisatsiooni ega olmejäätmete hulka. Küsige oma apteekrilt, kuidas visata ära ravimeid, mida te enam ei kasuta. See aitab kaitsta keskkonda.
Tähtaeg "> Muu teave
Mida Eviplera sisaldab
- Toimeained on emtritsitabiin, rilpiviriin ja tenofoviirdisoproksiil. Iga Eviplera õhukese polümeerikattega tablett sisaldab 200 mg emtritsitabiini, 25 mg rilpiviriini (vesinikkloriidina) ja 245 mg tenofoviirdisoproksiili (fumaraadina).
- Teised koostisosad on:
- Tableti sisu: mikrokristalne tselluloos, laktoosmonohüdraat, povidoon -eelgeelistatud maisitärklis, polüsorbaat 20, naatriumkroskarmelloos ja magneesiumstearaat.
- Kilekate: hüpromelloos, indigokarmiin-alumiiniumlakk, laktoosmonohüdraat, polüetüleenglükool, punane raudoksiid, kollakasoranž alumiiniumlakk (E110), titaandioksiid ja triatsetiin.
Kuidas Eviplera välja näeb ja pakendi sisu
Eviplera õhukese polümeerikattega tabletid on lillakasroosad, kapslikujulised, ühele küljele on trükitud "GSI" ja teisele küljele sile.
Eviplera on saadaval 30 tabletiga pudelites ja pakendites, mis sisaldavad 3 pudelit, millest igaüks sisaldab 30 tabletti.
Iga pudel sisaldab kuivatusainena silikageeli, mida tuleb tablettide kaitsmiseks pudelis hoida.
Silikageel on eraldi kotikeses või purgis ja seda ei tohi alla neelata.
Kõik pakendi suurused ei pruugi olla müügil.
Allika pakendi infoleht: AIFA (Itaalia ravimiamet). Sisu avaldati jaanuaris 2016. Esitatud teave ei pruugi olla ajakohane.
Kõige ajakohasemale versioonile juurdepääsu saamiseks on soovitatav külastada AIFA (Itaalia ravimiamet) veebisaiti. Vastutusest loobumine ja kasulik teave.
01.0 RAVIMPREPARAADI NIMETUS -
EVIPLERA 200 MG / 25 MG / 245 MG Kilega kaetud tabletid
02.0 KVALITATIIVNE JA KVANTITATIIVNE KOOSTIS -
Üks õhukese polümeerikattega tablett sisaldab 200 mg emtritsitabiini, 25 mg rilpiviriini (vesinikkloriidina) ja 245 mg tenofoviirdisoproksiili (fumaraadina).
Teadaolevat toimet omavad abiained
Üks õhukese polümeerikattega tablett sisaldab 277 mg laktoosmonohüdraati ja 4 mikrogrammi kollakasoranži alumiiniumlaki (E110).
Abiainete täielik loetelu vt lõik 6.1.
03.0 RAVIMVORM -
Õhukese polümeerikattega tablett.
Lillakas-roosa, kapslikujuline õhukese polümeerikattega tablett, suurusega 19 mm x 8,5 mm, mille ühel küljel on märgistus „GSI” ja teine külg on sile.
04.0 KLIINILINE TEAVE -
04.1 Näidustused -
Eviplera on näidustatud 1. tüüpi inimese immuunpuudulikkuse viirusega (HIV-1) nakatunud täiskasvanute raviks, kellel ei ole teadaolevaid resistentsusmutatsioone, mis on seotud mitte-nukleosiidse pöördtranskriptaasi inhibiitori (NNRTI) klassi, tenofoviiri või emtritsitrabiiniga ja viiruse koormusega ≤ 100 000 HIV-1 RNA-d koopiaid / ml (vt lõigud 4.2, 4.4 ja 5.1).
Eviplera kasutamisel tuleb lähtuda resistentsuse ja / või resistentsuse genotüübilisest analüüsist (vt lõigud 4.4 ja 5.1).
04.2 Annustamine ja manustamisviis
Ravi peab alustama HIV -nakkuse valdkonnas kogenud arst.
Annustamine
Täiskasvanud
Eviplera soovitatav annus on üks tablett suu kaudu üks kord päevas. Eviplerat tuleb võtta koos toiduga (vt lõik 5.2).
Kui on näidustatud ravi katkestamine ühe Eviplera komponendiga või annust tuleb kohandada, on saadaval eraldi emtritsitabiini, rilpiviriinvesinikkloriidi ja tenofoviirdisoproksiilfumaraadi preparaadid. Palun vaadake nende ravimite ravimi omaduste kokkuvõtet.
Kui patsient jätab Eviplera annuse võtmata 12 tunni jooksul pärast tavapärast võtmise aega, peab ta võtma Eviplera niipea kui võimalik koos toiduga ja jätkama tavapärase annustamisskeemiga. Kui patsient jätab Eviplera annuse võtmata rohkem kui 12 Ärge võtke vahelejäänud annust ja jätkake tavapärase annustamisskeemiga.
Kui patsient oksendab 4 tunni jooksul pärast Eviplera võtmist, peab ta koos toiduga võtma veel ühe Eviplera tableti. Kui patsient oksendab rohkem kui 4 tundi pärast Eviplera võtmist, ei pea ta uut Eviplera annust võtma enne järgmist tavapäraselt määratud annust.
Annuse kohandamine
Kui Eviplerat manustatakse koos rifabutiiniga, on soovitatav rifabutiini samaaegse manustamise ajal võtta koos Evipleraga täiendavalt 25 mg rilpiviriini tabletti päevas (vt lõik 4.5).
Spetsiaalsed populatsioonid
Eakad kodanikud
Eviplerat ei ole uuritud üle 65 -aastastel patsientidel. Eviplerat tuleb eakatele patsientidele manustada ettevaatusega (vt lõigud 4.4 ja 5.2).
Neerukahjustus
Ravi Evipleraga põhjustas seerumi keskmise kreatiniinisisalduse varase väikese tõusu, mis püsis aja jooksul stabiilsena ja mida peeti kliiniliselt ebaoluliseks (vt lõik 4.8).
Kliiniliste uuringute piiratud andmed toetavad Eviplera annustamist üks kord ööpäevas kerge neerukahjustusega patsientidel (kreatiniini kliirens 50 ... 80 ml / min). Siiski ei ole hinnatud Eviplera emtritsitabiini ja tenofoviirdisoproksiilfumaraadi komponentide pikaajalisi ohutusandmeid kerge neerukahjustusega patsientidel. Seetõttu tuleb kerge neerukahjustusega patsientidel kasutada Eviplerat ainult juhul, kui ravist saadav kasu kaalub üles võimalikud riskid (vt lõigud 4.4 ja 5.2).
Eviplerat ei soovitata mõõduka või raske neerukahjustusega (kreatiniini kliirens) patsientidele
Maksakahjustus
Eviplera kasutamise kohta kerge või mõõduka maksakahjustusega (Child-Pugh-Turcotte (CPT) aste A või B) patsientidel on piiratud teave. Kerge või mõõduka maksakahjustusega patsientidel ei ole Eviplera annust vaja kohandada. mõõduka maksakahjustusega patsientidel. Eviplerat ei ole uuritud raske maksakahjustusega (CPT aste C) patsientidel. Seetõttu ei ole Eviplerat raske maksakahjustusega patsientidele soovitatav kasutada (vt lõigud 4.4 ja 5.2).
Kui ravi Evipleraga katkestatakse patsientidel, kes on samaaegselt nakatunud HIV-i ja B-hepatiidi viirusega (HBV), tuleb neid patsiente hoolikalt jälgida hepatiidi ägenemiste suhtes (vt lõik 4.4).
Lapsed
Eviplera ohutus ja efektiivsus alla 18 -aastastel lastel ei ole tõestatud. Praegu kättesaadavad andmed on kirjeldatud lõigus 5.2, kuid soovitusi annustamise kohta ei saa anda.
Manustamisviis
Eviplerat tuleb võtta suu kaudu üks kord päevas koos toiduga (vt lõik 5.2). Eviplera on soovitatav alla neelata tervelt koos vähese veega. Õhukese polümeerikattega tabletti ei tohi närida, purustada ega poolitada, kuna see võib mõjutada Eviplera imendumist.
04.3 Vastunäidustused -
Ülitundlikkus toimeainete või lõigus 6.1 loetletud mis tahes abiainete suhtes.
Eviplerat ei tohi manustada koos järgmiste ravimitega, kuna rilpiviriini plasmakontsentratsioon võib oluliselt väheneda (CYP3A ensüümide indutseerimise või mao pH suurenemise tõttu), mis võib viia Eviplera terapeutilise toime kadumiseni:
• krambivastased ained karbamasepiin, okskarbasepiin, fenobarbitaal, fenütoiin;
• antimikroobsed ained rifampitsiin, rifapentiin;
• prootonpumba inhibiitorid, nagu omeprasool, esomeprasool, lansoprasool, pantoprasool, rabeprasool;
• süsteemne glükokortikoid deksametasoon, välja arvatud ühekordse annusena;
• naistepuna / hüperikum (Hypericum perforatum).
04.4 Erihoiatused ja ettevaatusabinõud kasutamisel -
Kuigi on tõestatud, et retroviirusevastase raviga tõhus viiruse pärssimine vähendab oluliselt sugulisel teel levimise ohtu, ei saa välistada jääkuriski. Tuleb võtta ettevaatusabinõusid, et vältida levikut vastavalt riiklikele juhistele.
Viroloogiline ebaõnnestumine ja resistentsuse teke
Eviplerat ei ole uuritud patsientidel, kellel on varem esinenud muu retroviirusevastase ravi viroloogiline ebaõnnestumine. Eviplera kasutamisel tuleb lähtuda resistentsuse analüüsist ja / või anamneesis resistentsusest (vt lõik 5.1).
Kahe III faasi kliinilise uuringu (C209 [ECHO] ja C215 [THRIVE]) 96. nädala koondatud efektiivsusanalüüsis said emtritsitabiini / tenofoviirdisoproksiilfumaraadi + rilpiviriiniga ravitud patsiendid viiruse algtasemega> 100 000 koopiat HIV-1 RNA / ml-l oli suurem viroloogilise ebaõnnestumise risk (17,6% rilpiviriini ja 7,6% efavirensi kasutamisel) kui patsientidel, kelle viiruse algtaseme väärtus oli ≤ 100 000 HIV-1 RNA koopiat / ml (5,9% rilpiviriini ja 2,4% efavirensi kasutamisel). Viroloogilise ebaõnnestumise määr emtritsitabiini / tenofoviirdisoproksiilfumaraadi + rilpiviriiniga ravitud patsientidel oli 48. nädalal ja 96. nädalal vastavalt 9,5% ja 11,5%, samal ajal kui emtritsitabiini / tenofoviiri rühmas. Disoproksiilfumaraat + efavirens vastavalt 4,2% ja 5,1% Rilpiviriini ja efavirensi vaheline erinevus uute viroloogiliste ebaõnnestumiste esinemissageduses, mida täheldati 48. kuni 96. nädala analüüsides, ei olnud statistiliselt oluline. Patsientidel, kelle viiruskoormus oli algtasemel> 100 000 HIV-1 RNA koopiat / ml ja kellel esines viroloogiline ebaõnnestumine, oli suurem raviga tekkiv resistentsus NNRTI klassi suhtes. Rohkem patsientidel, kellel esines virpoloogiline ebaõnnestumine rilpiviriiniga, tekkis lamivudiini / emtritsitabiiniga seotud resistentsus kui neil, kes said seda efavirensi kasutamisel (vt lõik 5.1).
Kardiovaskulaarsed mõjud
Ravi ületavate annuste (75 mg ja 300 mg üks kord ööpäevas) kasutamisel on rilpiviriini seostatud elektrokardiogrammi (EKG) QTc -intervalli pikenemisega (vt lõigud 4.5, 4.8 ja 5.2). Rilpiviriin soovitatud annuses 25 mg üks kord ööpäevas ei ole seotud kliiniliselt olulise toimega QTc -le. Eviplerat tuleb kasutada ettevaatusega, kui seda manustatakse koos ravimitega, millel on teadaolev Torsade de Pointes'i oht.
Koosmanustamine teiste ravimitega
Eviplerat ei tohi manustada koos teiste ravimitega, mis sisaldavad emtritsitabiini, tenofoviirdisoproksiilfumaraati, tenofoviirialafenamiidi või muid tsütidiini analooge, nagu lamivudiin (vt lõik 4.5). Eviplerat ei tohi manustada koos rilpiviriinvesinikkloriidiga, välja arvatud juhul, kui see on vajalik rifabutiini manustamisel annuse kohandamiseks (vt lõigud 4.2 ja 4.5). Eviplerat ei tohi manustada koos adefoviirdipivoksiiliga (vt lõik 4.5).
Eviplera ja didanosiini samaaegset manustamist ei soovitata, kuna kokkupuude didanosiiniga suureneb oluliselt pärast samaaegset manustamist tenofoviirdisoproksiilfumaraadiga, suurendades didanosiiniga seotud kõrvaltoimete riski (vt lõik 4.5). Harva esineb pankreatiit ja laktatsidoos, mõnikord surmaga teatatud.
Neerukahjustus
Eviplerat ei soovitata mõõduka või raske neerukahjustusega (kreatiniini kliirens) patsientidele
Pärast mitmete või suurte annuste mittesteroidsete põletikuvastaste ravimite (MSPVA-de) alustamist on tenofoviirdisoproksiilfumaraadiga ravitud patsientidel, kellel esines neerufunktsiooni häire riskitegureid, teatatud ägeda neerupuudulikkuse juhtudest. Kui Eviplerat manustatakse koos MSPVA -sid, neerufunktsiooni tuleb piisavalt jälgida.
Tenofoviirdisoproksiilfumaraadi kasutamisel kliinilises praktikas on teatatud neerupuudulikkuse, neerukahjustuse, kreatiniini taseme tõusu, hüpofosfateemia ja proksimaalse tubulopaatia juhtudest (sh Fanconi sündroom) (vt lõik 4.8).
Enne Eviplera -ravi alustamist on kõigil patsientidel soovitatav mõõta kreatiniini kliirensit ja neerufunktsiooni (kreatiniini kliirens ja seerumi fosfaat) tuleb jälgida pärast kahe kuni nelja ravinädalat, pärast kolmekuulist ravi ja seejärel iga kolme kuni kuue kuu järel patsiendid, kellel puuduvad neerude riskifaktorid. Neerukahjustuse riskiga patsientidel on vajalik neerufunktsiooni sagedasem jälgimine.
Kui seerumi fosfaat on vere glükoosisisaldus ning kaalium ja glükoos uriinis (vt lõik 4.8, proksimaalne tubulopaatia). Kuna Eviplera on kombineeritud ravim ja üksikute komponentide annustamisintervalli ei saa muuta, tuleb ravi Evipleraga katkestada patsientidel, kelle kreatiniini kliirens on kinnitatud alla 50 ml / min või kui seerumi fosfaatisisaldus on vähenenud.
Mõju luudele
Alamuuring, mis viiakse läbi kahe energiaga röntgenkiirte absorptiomeetria abil (kahe energiaga röntgenkiirte absorptiomeetria, DEXA) mõlema III faasi uuringu (C209 ja C215) puhul hinnati rilpiviriini mõju tihedusele, võrreldes üldise ja algse raviskeemiga.
luu mineraal (luude mineraalne tihedus, Luu tihedus) ja luude mineraalide sisaldus (luude mineraalide sisaldus(BMC) kogu organismis 48. ja 96. nädalal. DEXA alauuringud näitasid, et kogu organismi KMT ja KMK vähene, kuid statistiliselt oluline vähenemine võrreldes algtasemega oli rilpiviriini ja kontrolli puhul 48. ja 96. nädalal sarnane. rilpiviriini kogu keha BMD ja BMC muutustes võrreldes algtasemega võrreldes kontrolliga kogu populatsioonis ja patsientidel, keda raviti taustraviga, sealhulgas tenofoviirdisoproksiilfumaraadiga.
144 nädalat kestnud kontrollitud uuringus, milles anti-retroviirusevastaste ravimitega patsientide puhul võrreldi tenofoviirdisoproksiilfumaraati stavudiiniga kombinatsioonis lamivudiini ja efavirensiga, täheldati mõlemas puusaliigese ja lülisamba BMD vähest langust. Rühmad. luu biomarkerite algväärtus oli tenofoviirdisoproksiilfumaraadi rühmas 144. nädalal oluliselt suurem. Puusaluu BMD vähenemine oli selles rühmas oluliselt suurem kuni 96. nädalani. Pärast 144 ravinädalat ei suurenenud luumurdude oht ega ilmnenud olulised luu kõrvalekalded.
Teistes uuringutes (prospektiivsed ja ristlõikega) täheldati KMT kõige märgatavamat vähenemist patsientidel, keda raviti tenofoviirdisoproksiilfumaraadiga osana raviskeemist, mis sisaldas võimendatud proteaasi inhibiitorit. Osteoporoosiga patsientidel, kellel on suur luumurdude oht, tuleb kaaluda alternatiivseid ravirežiime.
Luuhäired (harva luumurrud) võivad olla seotud proksimaalse neeru tubulopaatiaga (vt lõik 4.8). Kui kahtlustatakse luude kõrvalekaldeid, tuleb otsida asjakohast konsultatsiooni.
HIV-patsiendid, kes on samaaegselt nakatunud B- või C-hepatiidi viirusega
Kroonilise B- või C-hepatiidiga patsientidel, keda ravitakse retroviirusevastase raviga, on suurenenud tõsiste ja eluohtlike maksapõhiste kõrvaltoimete risk.
Arstid peaksid järgima kehtivaid ravijuhiseid HIV-nakkuse optimaalseks raviks HBV-ga nakatunud patsientidel.
Samaaegse B- või C -hepatiidi viirusevastase ravi korral lugege palun ka nende ravimite omaduste kokkuvõtet.
Eviplera ohutust ja efektiivsust kroonilise HBV infektsiooni ravis ei ole tõestatud. Farmakodünaamilistes uuringutes leiti, et emtritsitabiin ja tenofoviir eraldi või kombinatsioonis on HBV vastu aktiivsed (vt lõik 5.1).
Patsientidel, kes on samaaegselt nakatunud HIV-i ja HBV-ga, võib Eviplera-ravi katkestamist seostada hepatiidi ägeda ägenemisega. Patsiente, kes on samaaegselt nakatunud HIV-i ja HBV-ga ning kes on lõpetanud Eviplera manustamise, tuleb hoolikalt jälgida a jälgima nii kliinilises kui ka laboratoorses uuringus vähemalt mitu kuud pärast ravi lõpetamist. Vajadusel võib olla õigustatud B-hepatiidi ravi jätkamine. Kaugelearenenud maksahaiguse või tsirroosiga patsientidel ei ole ravi katkestamine soovitatav. kuna pärast ravi võib hepatiit ägeneda maksa dekompensatsioon.
Maksahaigus
Eviplera ohutust ja efektiivsust ei ole olulise maksakahjustusega patsientidel tõestatud. Emtritsitabiini farmakokineetikat ei ole maksakahjustusega patsientidel uuritud. Emtritsitabiin ei metaboliseeru maksaensüümide poolt märkimisväärselt, seega tuleb võimaliku maksakahjustuse mõju Kerge või mõõduka maksakahjustusega (CPT A või B) patsientidel ei ole rilpiviriinvesinikkloriidi annuse kohandamine vajalik. Rilpiviriinvesinikkloriidi ei ole uuritud raske maksakahjustusega (CPT klass C) patsientidel. Tenofoviiri farmakokineetikat on uuritud maksakahjustusega patsientidel ja nende patsientide puhul ei ole annuse kohandamine vajalik.
Kerge või mõõduka maksakahjustusega patsientidel ei ole Eviplera annuse muutmine tõenäoliselt vajalik (vt lõigud 4.2 ja 5.2). Eviplerat tuleb mõõduka maksakahjustusega (CPT klass B) patsientidel kasutada ettevaatusega ja raske maksakahjustusega (CPT aste C) patsientidel ei soovitata seda kasutada.
Patsiendid, kellel on olemasolev maksafunktsiooni häire, sealhulgas krooniline aktiivne hepatiit, kombineeritud retroviirusevastase ravi ajal (kombineeritud retroviirusevastane ravi(CART) näitavad maksafunktsiooni kõrvalekallete sageduse suurenemist ja neid tuleb jälgida vastavalt üldisele kliinilisele praktikale. Kui neil patsientidel süveneb maksahaigus, tuleb ravi katkestada või katkestada.
Rasked nahareaktsioonid
Turuletulekujärgselt on Eviplera kasutamisel teatatud raskete nahareaktsioonide juhtudest koos süsteemsete sümptomitega, sealhulgas, kuid mitte ainult, lööbega, millega kaasneb palavik, villid, konjunktiviit, angioödeem, maksafunktsiooni tõus ja / või eosinofiilia. Eviplera kasutamise lõpetamine. Niipea, kui täheldatakse tõsiseid naha- ja / või limaskestareaktsioone, tuleb Eviplera kasutamine katkestada ja alustada sobivat ravi.
Kaal ja metaboolsed parameetrid
Retroviirusvastase ravi ajal võib esineda kehakaalu ja vere lipiidide ja glükoosisisalduse suurenemist. Sellised muutused võivad osaliselt olla seotud haiguste tõrje ja elustiiliga. Lipiidide puhul on mõnel juhul tõendeid ravitoime kohta, samas kui kaalutõusu puhul ei ole kindlaid tõendeid selle kohta, et see oleks seotud konkreetse raviga. Vere lipiidide ja glükoosisisalduse jälgimiseks viidatakse kehtestatud juhistele HIV raviks. Lipiidide ainevahetuse häireid tuleb ravida kliiniliselt sobival viisil.
Mitokondriaalne düsfunktsioon pärast kokkupuudet emakas
Tuuma (t) identsed analoogid võivad mitokondriaalset funktsiooni mõjutada erineval määral, kõige enam väljendunud stavudiini, didanosiini ja zidovudiini puhul. HIV -negatiivsetel imikutel on teatatud mitokondriaalsest düsfunktsioonist, emakas ja / või pärast sündi nukleosiidi analoogidele; need puudutasid peamiselt zidovudiini sisaldavaid raviskeeme. Peamised teatatud kõrvaltoimed on hematoloogilised häired (aneemia, neutropeenia) ja ainevahetushäired (hüperlaktateemia, hüperlipaseemia). Need sündmused olid sageli mööduvad. Harva on teatatud hilinenud neuroloogilistest häiretest (hüpertoonia, krambid, ebanormaalne käitumine). Praegu pole teada, kas need neuroloogilised häired on mööduvad või püsivad. Neid tulemusi tuleb iga kokkupuutel oleva lapse puhul arvesse võtta emakas nukleose (t) identsetele analoogidele, millel on teadmata etioloogiaga tõsised kliinilised ilmingud, eriti neuroloogilised ilmingud. Need tulemused ei muuda kehtivaid riiklikke soovitusi retroviirusevastase ravi kasutamiseks rasedatel, et vältida HIV vertikaalset levikut.
Immuunsüsteemi reaktivatsiooni sündroom
HIV-nakkusega patsientidel, kellel on CART-i alustamise ajal raske immuunpuudulikkus, võib tekkida põletikuline reaktsioon asümptomaatilistele või allesjäänud oportunistlikele patogeenidele, põhjustades tõsiseid kliinilisi seisundeid või sümptomite süvenemist. Tavaliselt on selliseid reaktsioone täheldatud esimestel nädalatel või kuudel pärast CART -i alustamist. Selle olulised näited on tsütomegaloviiruse retiniit, generaliseerunud ja / või fokaalsed mükobakteriaalsed infektsioonid ja kopsupõletik.
Pneumocystis jirovecii. Kõiki põletikulisi sümptomeid tuleb hinnata ja vajadusel ravi alustada.
Autoimmuunhäirete (nt Gravesi tõbi) esinemisest on teatatud ka immuunsuse taasaktiveerimise kontekstis; registreeritud aeg alguseni on siiski varieeruvam ja need sündmused võivad ilmneda mitu kuud pärast ravi algust.
Osteonekroos
Kuigi etioloogiat peetakse multifaktoriaalseks (sealhulgas kortikosteroidide kasutamine, alkoholi tarbimine, raske immunosupressioon, kõrgem kehamassiindeks), on teatatud osteonekroosi juhtudest, eriti kaugelearenenud HIV-haigusega patsientidel. Ja / või pikaajalist kokkupuudet CART-ga soovitatakse pöörduda arsti poole liigeste ebamugavustunde, valu ja jäikuse või liikumisraskuste korral.
Eakad kodanikud
Eviplerat ei ole uuritud üle 65 -aastastel patsientidel. Eakatel patsientidel on neerufunktsiooni langus tõenäolisem, seetõttu tuleb Eviplera -ravi eakatel patsientidel kasutada ettevaatusega (vt lõigud 4.2 ja 5.2).
Abiained
Eviplera sisaldab laktoosmonohüdraati. Patsiendid, kellel on harvaesinev pärilik galaktoositalumatus, Lapp-laktaasi puudulikkus või glükoosi-galaktoosi imendumishäire, ei tohi seda ravimit võtta.
Eviplera sisaldab värvainet nimega kollakasoranž alumiiniumlakk (E110), mis võib põhjustada allergilisi reaktsioone.
04.5 Koostoimed teiste ravimitega ja muud koostoimed -
Kuna Eviplera sisaldab emtritsitabiini, rilpiviriinvesinikkloriidi ja tenofoviirdisoproksiilfumaraati, võivad nende toimeainetega täheldatud koostoimed esineda ka Eviplera kasutamisel. Koostoimeuuringuid nende toimeainetega on läbi viidud ainult täiskasvanutel.
Rilpiviriin metaboliseerub peamiselt tsütokroom P450 (CYP3A) kaudu. Seetõttu võivad CYP3A indutseerivad või inhibeerivad ravimid mõjutada rilpiviriini kliirensit (vt lõik 5.2).
Samaaegne ravi on vastunäidustatud
On täheldatud, et Eviplera ja CYP3A indutseerivate ravimite samaaegne manustamine vähendab rilpiviriini plasmakontsentratsiooni, mis võib viia Eviplera terapeutilise efektiivsuse vähenemiseni (vt lõik 4.3).
On täheldatud, et Eviplera samaaegsel manustamisel koos prootonpumba inhibiitoritega väheneb rilpiviriini plasmakontsentratsioon mao pH suurenemise tõttu, mis võib põhjustada Eviplera terapeutilise toime kadumist (vt lõik 4.3).
Samaaegne ravi ei ole soovitatav
Eviplerat ei tohi manustada koos teiste emtritsitabiini, tenofoviirdisoproksiilfumaraati või tenofoviirialafenamiidi sisaldavate ravimitega. Eviplerat ei tohi manustada koos rilpiviriinvesinikkloriidiga, välja arvatud juhul, kui see on vajalik rifabutiini manustamisel annuse kohandamiseks (vt lõik 4.2).
Sarnasuse tõttu emtritsitabiiniga ei tohi Eviplerat manustada koos teiste tsütidiini analoogidega, näiteks lamivudiiniga (vt lõik 4.4). Eviplerat ei tohi manustada koos adefoviirdipivoksiiliga.
Didanosiin
Eviplera ja didanosiini samaaegne manustamine ei ole soovitatav (vt lõik 4.4 ja tabel 1).
Ravimid, mis erituvad neerude kaudu
Kuna emtritsitabiin ja tenofoviir erituvad peamiselt neerude kaudu, võib Eviplera manustamine koos ravimitega, mis vähendavad neerufunktsiooni või konkureerivad aktiivse tubulaarsekretsiooni (nt tsidofoviir), emtritsitabiini, tenofoviiri ja / või teiste samaaegselt manustatavate ravimite kontsentratsiooni seerumis tooted.
Eviplera kasutamist tuleks vältida nefrotoksiliste ravimite samaaegsel või hiljutisel kasutamisel. Mõned näited hõlmavad, kuid ei piirdu nendega: aminoglükosiidid, amfoteritsiin B, foskarnet, gantsükloviir, pentamidiin, vankomütsiin, tsidofoviir või interleukiin-2 (nimetatakse ka aldesleukiiniks).
Muud NNRTI -d
Eviplera manustamine koos teiste NNRTI-dega ei ole soovitatav.
Samaaegne ravi, mille puhul on soovitatav olla ettevaatlik
Tsütokroom P450 ensüümide inhibiitorid
On täheldatud, et Eviplera manustamisel koos ravimitega, mis inhibeerivad CYP3A ensüümide aktiivsust, suureneb rilpiviriini plasmakontsentratsioon.
QT -intervalli pikendavad ravimid
Eviplerat tuleb kasutada ettevaatusega, kui seda manustatakse koos ravimiga, millel on teadaolev Torsade de Pointes'i oht. Rilpiviriini ja elektrokardiogrammi QTc -intervalli pikendavate ravimite võimalike farmakodünaamiliste koostoimete kohta on piiratud teave. Tervete isikutega läbi viidud uuringus näidati, et rilpiviriini terapeutilised annused (75 mg üks kord ööpäevas ja 300 mg üks kord ööpäevas) pikendavad EKG QTc-intervalli (vt lõik 5.1).
P-glükoproteiini substraadid
Rilpiviriin pärsib in vitro glükoproteiin P (IC50 võrdub 9,2 mcM). Kliinilises uuringus ei avaldanud rilpiviriin digoksiini farmakokineetikale olulist mõju. Siiski ei saa täielikult välistada, et rilpiviriin võib suurendada kokkupuudet teiste ravimitega, mida transpordib P-glükoproteiin ja mis on tundlikumad soolestiku P-glükoproteiini inhibeerimise suhtes (nt dabigatraaneteksilaat).
Rilpiviriin on inhibiitor in vitro konveieri MATE-2K, IC50 on
Muud koostoimed
Koostoimed Eviplera või selle üksiku (te) komponendi (te) ja samaaegselt manustatavate ravimite vahel on toodud tabelis 1 ("suurenemist nimetatakse" ↑ ", vähenemist" ↓ ", muutust" ↔ ").
Tabel 1: Eviplera või selle üksikute komponentide ja teiste ravimite koostoimed
NC = pole arvutatud
1 See koostoimeuuring viidi läbi rilpiviriinvesinikkloriidi annusega, mis oli suurem kui soovitatud maksimaalse toime hindamiseks samaaegselt manustatavale ravimile. Annustamissoovitused kehtivad soovitatud rilpiviriini annuse 25 mg üks kord ööpäevas kohta.
2 Need on ravimid, mis kuuluvad klassidesse, mille puhul võib eeldada sarnast koostoimet.
3 See koostoimeuuring viidi läbi rilpiviriinvesinikkloriidi annusega, mis oli suurem kui soovitatud maksimaalse toime hindamiseks samaaegselt manustatavale ravimile.
4 Sofosbuviiri peamine ringlev metaboliit.
04.6 Rasedus ja imetamine -
Fertiilses eas naised / rasestumisvastased vahendid meestel ja naistel
Eviplera kasutamisega peab kaasnema tõhusate rasestumisvastaste vahendite kasutamine (vt lõik 4.5).
Rasedus
Eviplera või selle komponentide kohta rasedatel ei ole piisavalt ja hästi kontrollitud uuringuid. Andmed rilpiviriini kasutamise kohta rasedatel puuduvad või on piiratud (vähem kui 300 rasedust). Suur hulk andmeid rasedate kohta (rohkem kui 1000 rasedust) ei viita emtritsitabiini ja tenofoviirdisoproksiil.
Loomkatsed ei näita otsest ega kaudset kahjulikku toimet Eviplera komponentide reproduktiivtoksilisusele (vt lõik 5.3).
Ettevaatusabinõuna on soovitatav vältida Eviplera kasutamist raseduse ajal.
Toitmisaeg
Emtritsitabiin ja tenofoviirdisoproksiil erituvad rinnapiima. Ei ole teada, kas rilpiviriin eritub rinnapiima.
Eviplera toime kohta vastsündinutele / imikutele ei ole piisavalt teavet. Ravi ajal Evipleraga tuleb rinnaga toitmine katkestada.
Vältimaks HIV ülekandumist vastsündinule, soovitatakse HIV-nakkusega naistel mitte mingil juhul vastsündinuid rinnaga toita.
Viljakus
Puuduvad andmed Eviplera toime kohta inimese fertiilsusele. Loomkatsed ei ole näidanud emtritsitabiini, rilpiviriinvesinikkloriidi või tenofoviirdisoproksiilfumaraadi kahjulikku toimet fertiilsusele.
04.7 Toime autojuhtimise ja masinate käsitsemise võimele -
Eviplera ei mõjuta või mõjutab ebaoluliselt autojuhtimise ja masinate käsitsemise võimet. Siiski tuleb patsiente teavitada, et Eviplera komponentidega ravi ajal on teatatud väsimusest, pearinglusest ja unisusest (vt lõik 4.8). Neid mõjusid tuleb arvestada patsiendi autojuhtimise ja masinate käsitsemise võime hindamisel.
04.8 Kõrvaltoimed -
Ohutusprofiili kokkuvõte
Emtritsitabiini, rilpiviriini ja tenofoviirdisoproksiilfumaraadi kombinatsiooni uuriti iga komponendi puhul eelnevalt ravimata patsientidel (III faasi uuringud C209 ja C215). Ühe tableti raviskeemi Eviplera uuriti supressiooniga patsientidel, keda varem raviti ritonaviiri sisaldava raviskeemiga -võimendatud proteaasi inhibiitor (III faasi uuring GS-US-264-0106) või koos efavirensi / emtritsitabiini / tenofoviirdisoproksiilfumaraadiga (IIb faasi uuring GS-US-264-0111). Varem ravimata patsientidel võeti kõige sagedamini teatatud kõrvaltoimed arvesse tõenäoliselt või tõenäoliselt seotud rilpiviriinvesinikkloriidi ja emtritsitabiini / tenofoviirdisoproksiilfumaraadiga olid iiveldus (9%), pearinglus (8%), ebanormaalsed unenäod (8%), peavalu (6%), kõhulahtisus (5%) ja unetus (5%) (III faasi kliiniliste uuringute C209 ja C215 koondandmed, vt lõik 5.1). Viroloogiliselt pärsitud patsientidel läks Eviple üle ra, kõige sagedamini teatatud kõrvaltoimed, mida peetakse Evipleraga tõenäoliselt või tõenäoliselt seotud, olid väsimus (3%), kõhulahtisus (3%), iiveldus (2%) ja unetus (2%) (andmed uuringu faasi 48 nädala kohta) III GS-US-264-0106). Nendes uuringutes leiti, et emtritsitabiini ja tenofoviirdisoproksiilfumaraadi ohutusprofiil on kooskõlas sellega, mida on varem kogetud samade ainete kasutamisel koos teiste retroviirusevastaste ravimitega.
Tenofoviirdisoproksiilfumaraati kasutavatel patsientidel on harvadel juhtudel teatatud neerukahjustusest, neerupuudulikkusest ja proksimaalsest neerutubulopaatiast (sh Fanconi sündroom), mis mõnikord põhjustavad luumuutusi (ja harva luumurde). Eviplerat võtvatel patsientidel on soovitatav jälgida neerufunktsiooni (vt lõik 4.4).
Patsientidel, kes on samaaegselt nakatunud HIV-i ja HBV-ga, võib Eviplera-ravi katkestamist seostada hepatiidi ägeda ägenemisega (vt lõik 4.4).
Kõrvaltoimete tabel
Kliinilistest uuringutest ja turuletulekujärgsetest kogemustest tulenevad kõrvaltoimed, mis võivad olla seotud raviga Eviplera komponentidega, on loetletud allpool tabelis 2, jaotatuna organsüsteemi klasside ja esinemissageduse järgi. Igas klassis on esinenud kõrvaltoimeid. raskusastme vähenemise järjekord. Esinemissagedused on määratletud järgmiselt: väga sage (≥ 1/10), sage (≥ 1/100,
Tabel 2: Eviplera kõrvaltoimete tabel, mis põhineb kliinilistel uuringutel ja Eviplera ja selle üksikute komponentide turuletulekujärgsetel kogemustel
1 Emtritsitabiini puhul tuvastatud kõrvaltoime.
2 Rilpiriviinvesinikkloriidi puhul tuvastatud kõrvaltoime.
3 Tenofoviirdisoproksiilfumaraadi puhul tuvastatud kõrvaltoime.
4 Emtritsitabiini manustamisel lastele oli aneemia tavaline ja naha värvimuutus (suurenenud pigmentatsioon) väga levinud (vt lõik 4.8, Lapsed).
See kõrvaltoime võib ilmneda proksimaalse neeru tubulopaatia tagajärjel. Selle seisundi puudumisel ei loeta seda tenofoviirdisoproksiilfumaraadiga seotuks.
6 See oli tenofoviirdisoproksiilfumaraadi harvaesinev kõrvaltoime. Seda tuvastati ka turuletulekujärgse järelevalve käigus emtritsitabiini kõrvaltoimena, kuid seda ei täheldatud täiskasvanud randomiseeritud kontrollitud uuringutes ega emtritsitabiini HIV-i laste kliinilistes uuringutes. Aeg-ajalt esinemissagedust hinnati statistilise arvutuse alusel, mis põhineb kokkupuutunud patsientide koguarvul. neis kliinilistes uuringutes emtritsitabiinile (n = 1563).
See kõrvaltoime tuvastati Eviplera (fikseeritud annuste kombinatsioon) turuletulekujärgse jälgimise käigus, kuid seda ei täheldatud Eviplera randomiseeritud kontrollitud kliinilistes uuringutes. Esinemissagedust hinnati statistilise arvutusega, mis põhines Eviplera või selle kõikide komponentidega kokku puutunud patsientide koguarvul randomiseeritud kontrollitud uuringutes (n = 1261). Vt lõik 4.8, Mõnede kõrvaltoimete kirjeldus.
See kõrvaltoime tuvastati tenofoviirdisoproksiilfumaraadi turuletulekujärgse jälgimise käigus. kuid seda ei täheldatud randomiseeritud kontrollitud uuringutes ega tenofoviirdisoproksiilfumaraadi laiendatud juurdepääsuprogrammides. Sagedust hinnati statistilise arvutuse alusel, mis põhines tenofoviirdisoproksiilfumaraadiga kokku puutunud patsientide koguarvul randomiseeritud kontrollitud uuringutes ja vastuvõtuprogrammide laienemisel (n = 7319).
Laboratoorsete analüüside kõrvalekalded
Lipiidid
III faasi koonduuringutes C209 ja C215, mis viidi läbi eelnevalt ravimata patsientidel rilpiviriini rühmas 96 nädala jooksul, oli keskmine (tühja kõhu) kolesterooli keskmine muutus algväärtusest 5 mg / dl. HDL -kolesterool (tühja kõhuga) 4 mg / dl , LDL -kolesterool (tühja kõhuga) 1 mg / dl ja triglütseriidid (tühja kõhuga) -7 mg / dl. III faasi uuringus GS-US-264-0106, mis viidi läbi viroloogiliselt pärsitud patsientidel, kes lülitusid 48 nädala pärast üle ritonaviiriga võimendatud proteaasi inhibiitorit kasutavalt skeemilt Eviplerale, oli keskmine (tühja kõhu) kolesterooli keskmine muutus algväärtusest -24 mg / dl, HDL -kolesterool (tühja kõhuga) -2 mg / dl, LDL -kolesterool (tühja kõhuga) -16 mg / dl ja triglütseriidid (tühja kõhuga) -64 mg / dl.
Mõnede kõrvaltoimete kirjeldus
Neerukahjustus
Kuna Eviplera võib põhjustada neerukahjustusi, on soovitatav jälgida neerufunktsiooni (vt lõigud 4.4 ja 4.8) Ohutusprofiili kokkuvõte). Proksimaalne neeru tubulopaatia lahenes või paranes tavaliselt pärast tenofoviirdisoproksiilfumaraadi kasutamise lõpetamist. Mõnedel patsientidel ei kadunud kreatiniini kliirensi langus siiski täielikult, hoolimata tenofoviirdisoproksiilfumaraadi kasutamise lõpetamisest. Neerukahjustuse riskiga patsientidel (nt patsientidel, kellel on algne neeruriskifaktor, HIV -haigus või patsiendid, kes kasutavad samaaegselt nefrotoksilisi ravimeid) hoolimata tenofoviirdisoproksiilfumaraadi kasutamise lõpetamisest (vt lõik 4.4).
Koostoimed didanosiiniga
Eviplera ja didanosiini samaaegset manustamist ei soovitata, kuna see suurendab didanosiini süsteemset ekspositsiooni 40–60% ja võib suurendada didanosiiniga seotud kõrvaltoimete riski (vt lõik 4.5). Harva on teatatud pankreatiidist ja laktatsidoosist, mõnikord surmaga lõppenud.
Metaboolsed parameetrid
Retroviirusvastase ravi ajal võivad kehakaal ja vere lipiidide ja glükoosi tase suureneda (vt lõik 4.4).
Immuunsüsteemi reaktivatsiooni sündroom
HIV-nakkusega patsientidel, kellel on CART-i alustamise ajal raske immuunpuudulikkus, võib tekkida põletikuline reaktsioon asümptomaatilistele või allesjäänud oportunistlikele infektsioonidele. Teatatud on ka autoimmuunhäiretest (nt Gravesi tõbi), kuid registreeritud aeg alguseni on varieeruvam ja need sündmused võivad ilmneda ka mitu kuud pärast ravi alustamist (vt lõik 4.4).
Osteonekroos
Osteonekroosi juhtudest on teatatud peamiselt patsientidel, kellel on üldiselt teadaolevad riskifaktorid, kaugelearenenud HIV-haigus ja / või pikaajaline kokkupuude CART-iga. Selliste juhtude esinemissagedus on teadmata (vt lõik 4.4).
Rasked nahareaktsioonid
Eviplera turuletulekujärgselt on teatatud rasketest nahareaktsioonidest koos süsteemsete sümptomitega, sealhulgas lööve, millega kaasneb palavik, villid, konjunktiviit, angioödeem, maksafunktsiooni tõus ja / või eosinofiilia (vt lõik 4.4).
Lapsed
Alla 18 -aastaste laste kohta ei ole piisavalt andmeid. Eviplerat ei soovitata sellele patsientide populatsioonile (vt lõik 4.2).
Kui emtritsitabiini (üks Eviplera koostisosadest) manustati lastele, täheldati lisaks täiskasvanutele teatatud kõrvaltoimetele sagedamini järgmisi kõrvaltoimeid: aneemia oli sage (9,5%) ja nahavärvi muutus (suurenenud pigmentatsioon). oli väga sage (31,8%) lastel (vt lõik 4.8, Kõrvaltoimete tabel).
Muud eripopulatsioonid
Eakad kodanikud
Eviplerat ei ole uuritud üle 65 -aastastel patsientidel. Eakatel patsientidel on neerufunktsiooni langus tõenäolisem, seetõttu tuleb Eviplerat nende patsientide ravimisel kasutada ettevaatusega (vt lõik 4.4).
Neerukahjustusega patsiendid
Kuna tenofoviirdisoproksiilfumaraat võib põhjustada neerutoksilisust, soovitatakse Evipleraga ravitud neerukahjustusega patsientidel hoolikalt jälgida neerufunktsiooni (vt lõigud 4.2, 4.4 ja 5.2).
Patsiendid co-nakatunud HIV / HBV või HCV -ga
Emtritsitabiini, rilpiviriinvesinikkloriidi ja tenofoviirdisoproksiilfumaraadi kõrvaltoimete profiil HIV / HBV või HIV / HCV kaasinfektsiooniga patsientidel oli sarnane sellega, mida täheldati HIV-nakkusega patsientidel, kellel ei olnud HBV kaasinfektsiooni. Kuid nagu selles patsientide populatsioonis oodati, esines ASAT ja ALAT taseme tõusu sagedamini kui üldises HIV-nakkusega populatsioonis.
Hepatiidi ägenemised pärast ravi lõpetamist
Kliinilised ja laboratoorsed tõendid hepatiidi ägenemiste kohta on ilmnenud pärast ravi lõpetamist HIV-nakkusega patsientidel, kes on nakatunud samaaegselt HBV-ga (vt lõik 4.4).
Arvatavatest kõrvaltoimetest teatamine
Pärast ravimi müügiloa väljastamist tekkinud arvatavatest kõrvaltoimetest teatamine on oluline, kuna see võimaldab pidevalt jälgida ravimi kasu ja riski suhet. Tervishoiutöötajatel palutakse teavitada kõigist võimalikest kõrvaltoimetest riikliku teavitussüsteemi kaudu.
04.9 Üleannustamine -
Üleannustamise korral võib täheldada Eviplera ja selle üksikute komponentidega seotud kõrvaltoimete riski suurenemist.
Üleannustamise korral tuleb patsienti jälgida toksilisuse nähtude suhtes (vt lõik 4.8) ja vajadusel rakendada tavalist toetavat ravi, jälgides patsiendi kliinilist seisundit, jälgides elutähtsaid näitajaid ja EKG -d (intervall QT). .
Eviplera üleannustamise korral puudub spetsiifiline antidoot. Hemodialüüsi abil saab eemaldada kuni 30% emtritsitabiini annusest ja ligikaudu 10% tenofoviiri annusest. Ei ole teada, kas emtritsitabiini saab peritoneaaldialüüsi teel elimineerida. Kuna rilpiviriin seondub tugevalt valkudega, ei ole dialüüsi abil tõenäoliselt võimalik toimeainet märkimisväärselt eemaldada.
Aktiivsöe manustamine võib hõlbustada rilpiviriinvesinikkloriidi imendumata osa eemaldamist.
05.0 FARMAKOLOOGILISED OMADUSED
05.1 "Farmakodünaamilised omadused -
Farmakoterapeutiline rühm: viirusevastased ravimid süsteemseks kasutamiseks; viirusevastased ravimid HIV -nakkuste raviks, kombinatsioonid. ATC -kood: J05AR08.
Toimemehhanism ja farmakodünaamilised toimed
Emtritsitabiin on tsütidiini sünteetiline nukleosiidi analoog. Tenofoviirdisoproksiilfumaraat muundatakse in vivo toimeaine tenofoviir, mis on adenosiinmonofosfaadi nukleosiidmonofosfaadi (nukleotiid) analoog. Nii emtritsitabiinil kui ka tenofoviiril on spetsiifiline toime inimese immuunpuudulikkuse viiruse (HIV-1 ja HIV-2) ja inimese immuunpuudulikkuse viiruse, B-hepatiidi vastu.
Rilpiviriin on HIV-1 diarüülpürimidiini NNRTI. Rilpiviriini aktiivsust vahendab HIV-1 pöördtranskriptaasi (RT) mittekonkureeriv pärssimine.
Emtritsitabiin ja tenofoviir fosforüülitakse rakuensüümide poolt, moodustades vastavalt emtritsitabiini trifosfaadi ja tenofoviirdifosfaadi. Haridus in vitro on näidanud, et nii emtritsitabiini kui ka tenofoviiri saab rakkudes kombineerituna täielikult fosforüülida. Emtritsitabiini trifosfaat ja tenofoviirdifosfaat inhibeerivad konkureerivalt HIV-1 RT, põhjustades DNA ahela katkemist.
Nii emtritsitabiintrifosfaat kui ka tenofoviirdifosfaat on imetajate DNA polümeraaside nõrgad inhibiitorid ning puuduvad tõendid toksilisuse kohta mitokondritele ja in vitro kumbki in vivo. Rilpiviriin ei inhibeeri inimese raku DNA polümeraase α ja β ning mitokondriaalset DNA polümeraasi γ.
Viirusevastane toime in vitro
Emtritsitabiini, rilpiviriini ja tenofoviiri kolmekordse kombinatsiooni korral täheldati rakukultuurides sünergistlikku viirusevastast toimet.
Emtritsitabiini viirusevastast toimet HIV-1 kliiniliste ja laboratoorsete isolaatide suhtes hinnati lümfoblastoidsetes rakuliinides, MAGI-CCR5 rakuliinis ja perifeerse vere mononukleaarsetes rakkudes. Emtritsitabiini efektiivsed kontsentratsiooniväärtused 50% (EC50) olid vahemikus 0,0013-0,64 mcM.
Emtritsitabiinil oli rakukultuurides viirusevastane toime HIV-1 alatüüpide A, B, C, D, E, F ja G vastu (EC50 väärtused vahemikus 0,007 kuni 0,075 μM) ja see näitas tüvespetsiifilist aktiivsust HIV-2 vastu (EC50 väärtused Vahemikus 0,007 kuni 1,5 mcM).
Emtritsitabiini ja NRTI -de (abakaviir, didanosiin, lamivudiin, stavudiin, tenofoviir ja zidovudiin), NNRTI (delavirdiin, efavirenz, nevirapiin ja rilpiviriin) ja PI (amprenaviir, nelfinaviir, ritonaviir) ja sünergori kombineeritud uuringutes
Rilpiviriin näitas aktiivsust ägeda nakatunud T-rakuliini HIV-1 metsiktüüpi laboratoorsete tüvede vastu, keskmine HIV-1 / IIIB EC50 väärtus oli 0,73 nM (0,27 ng / ml). Kuigi rilpiviriin näitas piiratud aktiivsust in vitro HIV-2 puhul, mille EC50 väärtused jäävad vahemikku 2510–10 830 nM (920–3 970 ng / ml), ei soovitata kliiniliste andmete puudumisel HIV-2 infektsiooni ravi rilpiviriinvesinikkloriidiga.
Rilpiviriinil oli ka viirusevastane toime laia spektri M-rühma esmaste HIV-1 isolaatide (alatüüp A, B, C, D, F, G, H) vastu, mille EC50 väärtused olid vahemikus 0,07 kuni 1, 01 nM (vahemikus 0,03 kuni 0,37 ng / ml) ja O -rühma esmaste isolaatide EC50 väärtustega vahemikus 2,88 kuni 8,45 nM (vahemikus 1,06 kuni 3,10 ng / ml).
Tenofoviiri viirusevastast toimet HIV-1 kliiniliste ja laboratoorsete isolaatide suhtes hinnati lümfoblastoidsetel rakuliinidel, primaarsetel monotsüütidel / makrofaagidel ja perifeerse vere lümfotsüütidel. Tenofoviiri EC50 väärtused olid vahemikus 0,04-8,5 mcM).
Tenofoviir näitas rakukultuuridel viirusevastast toimet HIV-1 alatüüpide A, B, C, D, E, F, G ja O vastu (EC50 väärtused vahemikus 0,5 kuni 2,2 mcM) ja HIV-2 vastase tüve spetsiifilist aktiivsust (EC50 väärtused vahemikus 1,6 kuni 5,5 mcM).
NRTI-ga seotud tenofoviiri (abakaviir, didanosiin, emtritsitabiin, lamivudiin, stavudiin ja zidovudiin), NNRTI (delavirdiin, efavirenz, nevirapiin ja rilpiviriin) ja PI (amprenaviir, indinaviir, nelfinaviir, ritonaviir
Vastupidavus
Arvestades kõiki olemasolevaid andmeid in vitro ja andmed, mis on saadud varem ravimata patsientidelt, võivad järgmised HIV-1 pöördtranskriptaasi resistentsusega seotud mutatsioonid, kui need olid algul, mõjutada Eviplera aktiivsust: K65R, K70E, K101E, K101P, E138A, E138G, E138K, E138Q, E138R, V179L, Y181C , Y181I, Y181V, M184I, M184V, Y188L, H221Y, F227C, M & SUP2; 30I, M & SUP2; 30L ning L100I ja K103N kombinatsioon.
Ei saa välistada muude kui eespool loetletud NNRTI resistentsusega seotud mutatsioonide negatiivset mõju (nt ainult K103N või L100I mutatsioonid), kuna neid ei ole uuritud. in vivo piisaval arvul patsientidel.
Nagu teiste retroviirusevastaste ravimite puhul, peaks Eviplera kasutamisel olema resistentsuse analüüs ja / või resistentsuse ajalugu (vt lõik 4.4).
Rakukultuurides
In vitro ning mõnedel HIV-1 nakatunud patsientidel on täheldatud resistentsust emtritsitabiini või tenofoviiri suhtes, kuna on arenenud M184V või M184I asendus RT-s emtritsitabiiniga või K65R asendus RT-s tenofoviiriga. Lisaks valiti HIV-1 pöördtranskriptaasis K70E asendus tenofoviiriga, mille tulemuseks oli veidi vähenenud tundlikkus abakaviiri, emtritsitabiini, tenofoviiri ja lamivudiini suhtes. Muid resistentsusjärjestusi emtritsitabiini või tenofoviiri suhtes ei ole tuvastatud. Emtritsitabiinile resistentsed viirused M184V / I mutatsiooniga olid ristresistentsed lamivudiini suhtes, kuid säilitasid tundlikkuse didanosiini, stavudiini, tenofoviiri, zaltsitabiini ja zidovudiini suhtes. K65R mutatsiooni saab valida ka abakaviiri või didanosiini abil ja see võib vähendada tundlikkust nende ainete ning lamivudiini, emtritsitabiini ja tenofoviiri suhtes. Tenofoviirdisoproksiilfumaraati tuleks vältida K65R mutatsiooniga HIV-1 patsientidel. HIV-1 mutandid K65R, M184V ja K65R + M184V säilitavad tundlikkuse rilpiviriini suhtes.
Rilpiviriini suhtes resistentsed tüved on valitud rakukultuuridest erineva päritolu ja alatüübiga metsiku HIV-1 ning NNRTI-resistentse HIV-1 hulgast. Kõige sagedamini täheldatud resistentsusega seotud mutatsioonid hõlmasid L100I, K101E, V108I, E138K, V179F, Y181C, H221Y, F227C ja M & SUP2; 30I.
Varem ravimata HIV-1 nakatunud patsientidel
Resistentsusanalüüsides kasutati viroloogilise ebaõnnestumise laiemat määratlust kui esmaste efektiivsuse analüüside puhul. Resistentsuse kumulatiivses koondanalüüsis 96. nädalal patsientidel, kes said rilpiviriini kombinatsioonis emtritsitabiini / tenofoviirdisoproksiilfumaraadiga, nende uuringute alguses 48 nädalat. , täheldati viroloogilise ebaõnnestumise riski suurenemist rilpiviriini haru patsientidel (11,5% rilpiviriini rühmas ja 4,2% efavirensi rühmas), samas kui kahel ravigrupil täheldati madalat viroloogilise ebaõnnestumise määra 48 kuni 96. nädala analüüs (15 patsienti või 2,7% rilpiviriini rühmas ja 14 patsienti või 2,6% efavirensi rühmas). Viroloogilised ebaõnnestumised, 5/15 (rilpiviriin) ja 5/14 (efavirenz) esinesid viiruse algtasemel patsientidel koormus ≤ 100 000 koopiat / ml.
96-nädalase kombineeritud resistentsuse analüüsi käigus patsientidel, kes võtsid III faasi kliinilistes uuringutes C209 ja C215 emtritsitabiini / tenofoviirdisoproksiilfumaraati + rilpiviriinvesinikkloriidi, täheldati 78 viroloogilise ebaõnnestumisega patsienti; teave resistentsuse kohta oli kättesaadav 71 patsiendile. Selles analüüsis NNRTI resistentsusega seotud mutatsioonid, mis nendel patsientidel kõige sagedamini arenesid, olid V90I, K101E, E138K / Q, V179I, Y181C, V189I, H221Y ja F227C. Kõige sagedasemad mutatsioonid olid analüüsis samad 48 ja 96 nädala pärast. esialgsed mutatsioonid V90I ja V189I ei mõjutanud uuringute ravivastust. E138K asendus tekkis sagedamini ravi ajal rilpiviriiniga, sageli seoses M184I asendusega. 52% rilpiviriini haru viroloogilise ebaõnnestumisega patsientidest tekkis samaaegne NNRTI ja NRTI mutatsioonid. NRTI resistentsusega seotud reaktsioonid, mis tekkisid raviperioodi jooksul 3 või enama patsiendi puhul, olid K65R, K70E, M184V / I ja K219E.
96. nädalal esines vähemal patsiendil rilpiviriini rühmas ja algtasemel viiruskoormus ≤ 100 000 koopiat / ml tekkivaid asendusi, mis olid seotud rilpiviriiniresistentsuse ja / või fenotüübilise resistentsusega (7/288), kui patsientidel, kelle algviiruse koormus oli> 100 000 koopiat / ml (30 / 262). Patsientide seas, kellel tekkis resistentsus rilpiviriini suhtes, esines ristresistentsust teiste NNRTI-de suhtes 4/7 patsiendil, kelle viiruskoormus oli algtasemel ≤ 100 000 koopiat / ml ja 28/30 patsiendil, kelle viiruskoormus oli> 100 000 koopiat / ml.
Viroloogiliselt pärsitud HIV-1 nakatunud patsientidel
Uuring GS-US-264-0106: 469 -st Eviplera -ga ravitud patsiendist [317 patsienti läks Eviplera -ravile üle algul (Eviplera -rühm) ja 152 -l patsiendil vahetati Eviplera -ravi üle 24. nädalal (hilinenud lülitusharu)] hinnati resistentsuse tekke suhtes kokku 7 patsienti; nende patsientide kohta olid kättesaadavad kõik andmed genotüübi ja fenotüübi kohta. 24. nädalal läks kaks patsienti ravi alguses üle Eviplera-le (2 patsienti 317-st, 0,6%) ja ühel patsiendil, kes jätkas ritonaviiriga võimendatud proteaasi inhibiitorite raviskeemi [jätkuv rühm] (1 patsient 159-st, 0,6%), tekkis genotüüp ja / või fenotüüpiline resistentsus uuritavate ravimite suhtes. Pärast 24. nädalat tekkis kaheksal Eviplera haru patsiendil HIV-1 resistentsus 48. nädalaks (kokku 4 patsiendil 469-st, 0,9%). Ülejäänud 3 Eviplera-ga ravitud patsiendil ei tekkinud resistentsust.
Kõige sagedasemad tekkivad resistentsusmutatsioonid Evipleraga ravitud patsientidel olid pöördtranskriptaasi korral M184V / I ja E138K. Kõik patsiendid säilitasid tundlikkuse tenofoviiri suhtes. 24-st Eviplera-ga ravitud patsiendist, kellel oli algul HIV-1 NNRTI-ga seotud K103N-asendus, oli 17-l 18-l Eviplera haru patsiendil ja 5-l 6-l patsiendil pärast Eviplera-le üleminekut viroloogiline supressioon säilinud Vastavalt 48 nädalat ja 24 nädalat. Patsiendil, kellel oli ravi alguses K103N asendus, esines viroloogiline ebaõnnestumine ja 48. nädalaks tekkis täiendav resistentsus.
Uuring GS-US-264-0111: 48 nädala jooksul ei tekkinud tekkivat resistentsust kahel viroloogilise ebaõnnestumisega patsiendil nende seas, kes vahetasid efavirensi / emtritsitabiini / tenofoviirdisoproksiili kasutamise Eviplera vastu (0 patsiendil 49 -st).
Risttakistus
Rilpiviriini ja emtritsitabiini või tenofoviiri suhtes resistentsete HIV-1 variantide või emtritsitabiini või tenofoviiri ja rilpiviriini suhtes resistentsete variantide vahel ei ole tõestatud olulist ristresistentsust.
Rakukultuurides
Emtritsitabiin
Emtritsitabiini suhtes resistentsed viirused, millel on asendus M184V / I, olid lamivudiini suhtes ristresistentsed, kuid jäid tundlikuks didanosiini, stavudiini, tenofoviiri ja zidovudiini suhtes.
Viirused, mille asendused vähendavad tundlikkust stavudiini ja zidovudiini suhtes (tümidiini analoogmutatsioonid, TAM) (M41L, D67N, K70R, L210W, T215Y / F, K219Q / E) või didanosiin (L74V), jäid emtritsitabiini suhtes tundlikuks. HIV-1, mis sisaldas asendust K103N või muid resistentsusega seotud asendusi rilpiviriini ja teiste NNRTI-de suhtes, oli emtritsitabiini suhtes tundlik.
Rilpiviriinvesinikkloriid
67 rekombinantse laboratoorse HIV-1 tüve kogumis, millel on resistentsusega seotud mutatsioon NNRTI-de suhtes resistentsusega seotud RT-positsioonides, sealhulgas sagedamini esinevad K103N ja Y181C, näitas rilpiviriin viirusevastast toimet 64 (96%) tüve vastu. -seotud üksikud mutatsioonid, mis on seotud tundlikkuse vähenemisega rilpiviriini suhtes, olid: K101P ja Y181V / I. Ainult K103N asendamine ei vähendanud tundlikkust rilpiviriini suhtes, kuid K103N ja L100I seostamisel vähenes tundlikkus rilpiviriin. Teises uuringus vähendas Y188L asendamine kliiniliste isolaatide tundlikkust rilpiviriini suhtes 9 korda ja saidile suunatud mutantide puhul 6 korda.
Tenofoviirdisoproksiilfumaraat
K65R asendamine ja ka K70E asendamine vähendavad tundlikkust abakaviiri, didanosiini, lamivudiini, emtritsitabiini ja tenofoviiri suhtes, kuid säilitavad tundlikkuse zidovudiini suhtes.
HIV-1-ga patsientidel, kellel on 3 või enam TAM-i, mis sisaldavad pöördtranskriptaasi M41L või L210W asendusi, on vähenenud ravivastus tenofoviirdisoproksiilfumaraadile.
Viroloogiline vastus tenofoviirdisoproksiilfumaraadile ei vähenenud HIV-1-ga nakatunud patsientidel, kes väljendasid abakaviiri / emtritsitabiini / lamivudiini resistentsusega seotud M184V asendust.
HIV-1 tüved, mis sisaldasid K103N, Y181C või rilpiviriiniga seotud asendusi NNRTI resistentsusega, olid tenofoviiri suhtes tundlikud.
Patsientidel, keda pole varem ravitud
Tabelis 3 on esitatud resistentsuse tulemused, sealhulgas ristresistentsus teiste NNRTI-de suhtes patsientidel, kes said rilpiviriinvesinikkloriidi kombinatsioonis emitritsitabiini / tenofoviirdisoproksiilfumaraadiga (koondandmed uuringutest C209 ja C215) ja kellel esines viroloogiline ebaõnnestumine.
Tabel 3: Fenotüübilise resistentsuse ja ristresistentsuse tulemused, mis on saadud uuringutest C209 ja C215 (koondandmed) patsientidele, kes said 96. nädalal rilpiviriinvesinikkloriidi kombinatsioonis emtritsitabiini / tenofoviirdisoproksiilfumaraadiga (põhineb resistentsuse analüüsil)
1 BLVL = Baasviiruse koormus (baasviiruse koormus).
2 Fenotüüpne resistentsus rilpiviriini suhtes (> 3,7-kordne muutus võrreldes kontrolliga).
3 Fenotüüpne resistentsus (viirusevastane).
Viroloogiliselt pärsitud HIV-1 nakatunud patsientidel
Uuringus GS-US-264-0106 vähenes HIV-1 tundlikkus 48 nädala jooksul neljal 469 patsiendist, kes vahetasid Eviplerale ritonaviiriga võimendatud proteaasi inhibiitorite raviskeemi, tundlikkuse vähemalt ühe Eviplera komponendi suhtes. de novo emtritsitabiini/lamivudiini suhtes ja 4 juhul ka rilpiviriini suhtes, mille tulemuseks oli ristresistentsus efavirensi (2/2), nevirapiini (2/2) ja etraviriini (1/2) suhtes.
Mõju elektrokardiogrammile
Rilpiviriinvesinikkloriidi soovitatud annuse 25 mg üks kord ööpäevas mõju QTcF-intervallile hinnati randomiseeritud, platseebokontrolliga toimeaine (moksifloksatsiin 400 mg üks kord ööpäevas) ristuvuuringus, milles osales 60 täiskasvanut. Terve, 13 mõõtmist üle 24 Rilpiviriinvesinikkloriid soovitatud annuses 25 mg üks kord ööpäevas ei ole seotud kliiniliselt olulise toimega QTc -le.
Kui tervetel täiskasvanutel uuriti rilpiviriinvesinikkloriidi ületerapeutilisi annuseid 75 mg üks kord ööpäevas ja 300 mg üks kord ööpäevas, oli QTcF intervalli ajaga sobitatud maksimaalsed keskmised erinevused (ülemine 95% usalduspiir) võrreldes platseeboga pärast algtaseme korrigeerimist vastavalt 23,3 ms. Rilpiviriinvesinikkloriidi püsikontsentratsiooni manustamine 75 mg üks kord päevas ja 300 mg üks kord ööpäevas andis Cmax vastavalt 2,6 ja 6,7 korda. ligikaudu kõrgem kui keskmine soovitusliku annuse 25 korral täheldatud püsiseisundi Cmax mg rilpiviriinvesinikkloriidi päevas.
Kliiniline kogemus
Varem ravitud HIV-1 nakatunud patsiendid
Eviplera efektiivsus põhineb kahe randomiseeritud, topeltpime, kontrollitud uuringu C209 ja C215 96-nädalaste andmete analüüsil. Uuringusse kaasati HIV-1 nakatunud patsiente, keda ei olnud varem viirusevastaste ravimitega ravitud (n = 1 368). plasma HIV RNA ≥ 5000 koopiat / ml ja skriiniti tundlikkuse suhtes N (t) RTI-de suhtes ja spetsiifiliste NNRTI resistentsusega seotud mutatsioonide puudumise suhtes. Uuringud on identse ülesehitusega, välja arvatud põhirežiim (taustrežiim, BR). Patsiendid randomiseeriti suhtega 1: 1, et nad saaksid lisaks BR -le 25 mg rilpiviriinvesinikkloriidi (n = 686) üks kord ööpäevas või 600 mg efavirensi (n = 682) üks kord päevas. Uuringus C209 (n = 690) oli BR emtritsitabiin / tenofoviirdisoproksiilfumaraat. Uuringus C215 (n = 678) koosnes BR uurija valitud 2 N (t) RTIst: emtritsitabiin / tenofoviirdisoproksiilfumaraat (60%, n = 406) või lamivudiin / zidovudiin (30%, n = 204) või abakaviir pluss lamivudiin (10%, n = 68).
C209 ja C215 andmete koondanalüüsis patsientide kohta, kes said taustravi emtritsitabiini / tenofoviirdisoproksiilfumaraadiga, olid demograafilised andmed ja algtaseme omadused rilpiviriini ja efavirensi haru vahel tasakaalus. Tabel 4 näitab haiguse demograafilisi ja algväärtusi. Keskmine plasma HIV-1 RNA oli vastavalt 5,0 ja 5,0 log 10 koopiat / ml ning CD4 keskmine mediaan vastavalt 247 x 106 rakku / l ja 261 x 106 rakku / l patsientidel, kes randomiseeriti võtma rilpiviriini ja efavirensi.
Tabel 4. HIV-1 nakatunud retroviirusevastaste täiskasvanud patsientide demograafilised ja algväärtused uuringutes C209 ja C215 (koondandmed patsientide kohta, kes said rilpiviriinvesinikkloriidi või efavirensi kombinatsioonis emtritsitabiini / tenofoviirdisoproksiilfumaraadiga) 96. nädalal.
Viroloogilise vastuse alamrühma analüüs (
Tabel 5. Randomiseeritud ravi viroloogilised tulemused uuringutest C209 ja C215 (koondandmed patsientide kohta, kes said rilpiviriinvesinikkloriidi või efavirensi kombinatsioonis emtritsitabiini / tenofoviirdisoproksiilfumaraadiga) 48. nädalal (esmane) ja 96. nädalal.
n = patsientide koguarv ravigrupi kohta.
a ITT TLOVR = aeg viroloogilise vastuse kadumiseni populatsioonis kavatsus ravida.
b Vastuste määra erinevus on tavalise lähenduse korral 1% (95% usaldusintervall -3% kuni 6%).
c 48. ja 96. nädala esmase analüüsi vahel esines 17 uut viroloogilist ebaõnnestumist (6 patsienti, kelle viiruskoormus oli algtasemel ≤ 100 000 koopiat / ml ja 11 patsienti, kelle viiruskoormus oli algtasemel> 100 000 koopiat / ml). analüüs 48. nädalal, millest kõige sagedamini esines viroloogiline ebaõnnestumine kuni ravi katkestamiseni põhjustel, mis ei olnud seotud kõrvaltoimetega.
d 48. nädalal ja 96. nädalal esmase analüüsi vahel esines 10 uut viroloogilist ebaõnnestumist (3 patsienti, kelle viiruskoormus oli algtasemel ≤ 100 000 koopiat / ml ja 7 patsienti, kelle viiruskoormus oli algtasemel> 100 000 koopiat / ml). analüüs 48. nädalal, millest kõige sagedamini esines viroloogiline ebaõnnestumine kuni ravi katkestamiseni põhjustel, mis ei olnud seotud kõrvaltoimetega.
ja nt. kadunud järelkontrolli, mittejärgimise, nõusoleku tagasivõtmise ajal.
On näidatud, et emtritsitabiin / tenofoviirdisoproksiilfumaraat + rilpiviriinvesinikkloriid ei ole halvemad HIV-1 RNA alla 50 koopia / ml saamisel võrreldes emtritsitabiini / tenofoviirdisoproksiilfumaraadi + efavirensiga.
Keskmine CD4 arvu muutus algväärtusest kuni 96. nädalani oli emtritsitabiini / tenofoviirdisoproksiilfumaraadi raviskeemi saanud patsientide rilpiviriini ja efavirensi rühmas vastavalt +226 x 106 rakku / l ja +222 x 106 rakku / l.
96. nädalal ei täheldatud uusi ristresistentsuse mustreid võrreldes 48. nädalaga. Tabelis 6 on näidatud resistentsuse tulemused viroloogilise ebaõnnestumise ja fenotüübilise resistentsusega patsientidel, mis on määratletud vastavalt 96. nädala protokollile:
Tabel 6. Fenotüübilise resistentsuse tulemused uuringutel C209 ja C215 96. nädalal (resistentsuse analüüsi põhjal) (koondandmed patsientide kohta, kes said rilpiviriinvesinikkloriidi või efavirensi kombinatsioonis emtritsitabiini / tenofoviirdisoproksiilfumaraadiga)
Ristresistentsust teiste heakskiidetud NNRTI-de (etraviriini, efavirensi, nevirapiini) suhtes on üldiselt täheldatud patsientidel, kes ei allunud Eviplera ravile ja kellel tekkis resistentsus Eviplera suhtes.
Viroloogiliselt pärsitud HIV-1 nakatunud patsiendid
Uuring GS-US-264-0106
Ritonaviiriga võimendatud proteaasi inhibiitorilt kombinatsioonis kahele NRTI-le Eviplera ühe tableti režiimile ülemineku tõhusus ja ohutus määrati randomiseeritud avatud uuringus, milles osalesid HIV-1 nakatunud, viroloogiliselt pärsitud täiskasvanud. esimene või teine retroviirusevastane raviskeem ilma eelneva viroloogilise ebaõnnestumiseta, praegune või varasem resistentsus Eviplera kolme komponendi suhtes ja stabiilne supressioon (HIV-1 RNA)
Ravitulemused 24 nädala jooksul on toodud tabelis 7.
Tabel 7: randomiseeritud ravitulemused uuringus GS-US-264-0106 24. nädalal
24. nädala aken päevade 127 ja 210 vahel (kaasa arvatud).
b Analüüs hetktõmmis.
c Hõlmab patsiente, kelle HIV-1 RNA oli 24. nädala aknas ≥ 50 koopiat / ml, patsiente, kes lõpetasid oma manustamise varakult efektiivsuse puudumise või efektiivsuse vähenemise tõttu, patsiente, kes lõpetasid ravimi võtmise muudel põhjustel kui kõrvaltoime või surm. kellel oli katkestamise ajal viiruse koormus ≥ 50 koopiat / ml.
d Hõlmab patsiente, kes lõpetasid ravi kõrvaltoimete või surma tõttu igal ajal alates 1. päevast kuni 24. nädala ajavahemikuni ja kelle puhul ei ole selle aja jooksul saadaval viroloogilisi andmeid ravi kohta.
e Hõlmab patsiente, kes katkestasid ravi muudel põhjustel peale kõrvaltoimete, surma või efektiivsuse puudumise või efektiivsuse vähenemise, st nõusoleku tagasivõtmise, kadusid järelkontrolli ajal jne.
Üleminek Eviplerale ei olnud HIV-1 RNA säilitamisel halvem
92% -l (140/152) oli HIV-1 RNA 92% (140/152)
48. nädalal oli 89% (283/317) patsientidest, kes randomiseeriti ravieelselt Eviplerale (Eviplera), HIV-1 RNA-ga
Eviplera rühmas oli 7/317 patsienti (2%) ja hilinenud lülitusgrupis 6/152 patsienti (4%), kes katkestasid uuringuravimi jäädavalt raviga seotud kõrvaltoimete (EAET) tõttu. Ükski patsient ei katkestanud uuringut EAET -le basaalravi jätkamise rühmas.
Uuring GS-US-264-0111
Efavirensi / emtritsitabiini / tenofoviirdisoproksiili ühe tableti režiimilt Eviplera ühe tableti raviskeemile ülemineku efektiivsust, ohutust ja farmakokineetilisi omadusi hinnati avatud uuringus HIV-1 nakatunud, viroloogiliselt pärsitud täiskasvanutega. et olete varem saanud ainult efavirensi / emtritsitabiini / tenofoviirdisoproksiili
retroviirusevastast raviskeemi vähemalt kolm kuud ja soovivad raviskeemi muuta efavirensi talumatuse tõttu. Enne uuringusse kaasamist pidid patsiendid olema vähemalt 8 nädala jooksul stabiilsed viroloogilised supressioonid, ilma et nad oleksid praegu või varem resistentsed ühegi Eviplera kolme komponendi ja HIV-1 RNA suhtes.
Lapsed
Euroopa Ravimiamet on edasi lükanud kohustuse esitada Evipleraga läbi viidud uuringute tulemused HIV-1-ga ravitud laste ühe või mitme alarühma kohta (teave lastel kasutamise kohta vt lõik 4.2).
05.2 "Farmakokineetilised omadused -
Imendumine
Pärast ühekordse annuse manustamist hinnati ühe Eviplera õhukese polümeerikattega tableti bioekvivalentsust ühe emtritsitabiini 200 mg kõvakapsli, ühe rilpiviriini (vesinikkloriidina) 25 mg õhukese polümeerikattega tableti ja ühe tenofoviirdisoproksiili (fumaraadina) 245 mg õhukese polümeerikattega tabletiga. toidetud olekus tervetele isikutele. Pärast Eviplera suukaudset manustamist koos toiduga imendub emtritsitabiin kiiresti ja ulatuslikult ning maksimaalne plasmakontsentratsioon saavutatakse 2,5 tunni jooksul pärast manustamist. Tenofoviiri maksimaalne kontsentratsioon plasmas täheldatakse 2 tunni jooksul ja rilpiviriini maksimaalne plasmakontsentratsioon saavutatakse tavaliselt 4-5 tunni jooksul . Pärast tenofoviirdisoproksiilfumaraadi suukaudset manustamist HIV -nakkusega patsientidele imendub tenofoviirdisoproksiilfumaraat kiiresti ja muundatakse tenofoviiriks. Emtritsitabiini 200 mg kõvakapslite absoluutne biosaadavus on hinnanguliselt 93%. Tenofoviiri suukaudne biosaadavus tenofoviirdisoproksiilfumaraadi tablettidest tühja kõhuga patsientidel oli ligikaudu 25%. Rilpiviriini absoluutne biosaadavus ei ole teada. Eviplera manustamine tervetele täiskasvanud isikutele koos kerge einega (390 kcal) või tavalise toidukorraga (540 kcal) suurendas rilpiviriini ja tenofoviiri kokkupuuteid võrreldes tühja kõhuga manustamisega. Rilpiviriini Cmax ja AUC suurenesid kerge einega vastavalt 34% ja 9% ning standardtoiduga 26% ja 16%. Tenofoviiri Cmax ja AUC suurenesid vastavalt 12% ja 28%.% Kerge einega ja 32% ja 38% tavalise toiduga. Toit ei mõjutanud emtritsitabiini ekspositsiooni Optimaalse imendumise tagamiseks tuleb Eviplerat manustada koos toiduga (vt lõik 4.2).
Levitamine
Pärast intravenoosset manustamist hinnati emtritsitabiini ja tenofoviiri üksikute komponentide jaotusruumalaks vastavalt ligikaudu 1400 ml / kg ja 800 ml / kg. Pärast üksikute komponentide suukaudset manustamist on emtritsitabiin ja tenofoviirdisoproksiilfumaraat laialt levinud kogu kehas. In vitro emtritsitabiini seondumine inimese plasmavalkudega oli in vitro ligikaudu 99,7% ja see on peamiselt albumiin. Tenofoviiri kontsentratsioonivahemikus 0,01 ... 25 mcg / ml seondub in vitro plasmavalk või tenofoviiri seerumivalk oli vastavalt alla 0,7% ja 7,2%.
Biotransformatsioon
Emtritsitabiini metabolism on piiratud. Emtritsitabiini biotransformatsioon hõlmab tioolrühma oksüdeerimist 3 "-sulfoksiid-diastereomeerideks (ligikaudu 9% annusest) ja konjugeerimist glükuroonhappega, et saada 2" -O-glükuroniid (ligikaudu 4% annusest). Katsed in vitro näitavad, et rilpiviriinvesinikkloriid läbib peamiselt oksüdatiivse metabolismi, mida vahendab tsütokroom P450 (CYP) 3A süsteem. Uuringud in vitro leidis, et ei tenofoviirdisoproksiilfumaraat ega tenofoviir ei ole CYP450 ensüümide substraadid. Ei emtritsitabiin ega tenofoviir inhibeeri in vitro ravimi metabolismi vahendab üks inimese peamisi CYP450 isovorme, mis on seotud ravimite biotransformatsiooniga. Lisaks ei inhibeeri emtritsitabiin glükuroniseerimise eest vastutavat ensüümi uridiin-5 "-difosfoglukuronüültransferaasi.
Elimineerimine
Emtritsitabiin eritub peamiselt neerude kaudu, kusjuures annus taastub täielikult uriiniga (ligikaudu 86%) ja väljaheitega (ligikaudu 14%). Kolmteist protsenti emtritsitabiini annusest eritub uriiniga kolme metaboliidina. Emtritsitabiini süsteemne kliirens on keskmiselt 307 ml / min. Pärast suukaudset manustamist on emtritsitabiini eliminatsiooni poolväärtusaeg ligikaudu 10 tundi.
Rilpiviriini lõplik eliminatsiooni poolväärtusaeg on ligikaudu 45 tundi. Pärast 14C-rilpiviriini ühekordse annuse suukaudset manustamist leiti radioaktiivsusest vastavalt väljaheites ja uriinis keskmiselt 85% ja 6,1%. Väljaheites muutumatu rilpiviriin moodustas ligikaudu 25% manustatud annusest. Uriinis leiti ainult muutumatu rilpiviriini jälgi (
Tenofoviir elimineeritakse peamiselt neerude kaudu nii filtreerimise kui ka aktiivse tubulaarse transpordisüsteemi (inimese orgaanilise aniooni transporter 1 [hOAT1]) kaudu, ligikaudu 70 ... 80% annusest eritub muutumatul kujul uriiniga pärast intravenoosset manustamist. Tenofoviiri näiv kliirens oli ligikaudu 307 ml / min. Neerukliirens oli hinnanguliselt ligikaudu 210 ml / min, mis on suurem kui glomerulaarfiltratsiooni kiirus. See näitab, et aktiivne tubulaarsekretsioon on tenofoviiri "eliminatsiooni" oluline element. Pärast suukaudset manustamist oli tenofoviiri eliminatsiooni poolväärtusaeg ligikaudu 12 ... 18 tundi.
Eakad kodanikud
HIV -nakkusega patsientide populatsiooni farmakokineetilised analüüsid näitasid, et rilpiviriini farmakokineetika ei varieerunud vaadeldavas vanusevahemikus (18 kuni 78 aastat), vaid kaks patsienti olid 65 -aastased või vanemad.
Seks
Emtritsitabiini ja tenofoviiri farmakokineetika on meestel ja naistel sarnane. Rilpiviriini farmakokineetikas ei esinenud kliiniliselt olulisi erinevusi meeste ja naiste vahel.
Rahvus
Rahvuslikult seotud kliiniliselt olulisi farmakokineetilisi erinevusi ei tuvastatud.
Lapsed
Üldiselt on emtritsitabiini farmakokineetika imikutel, lastel ja noorukitel (vanuses 4 kuud kuni 18 aastat) sarnane täiskasvanute omadega. Rilpiviriini ja tenofoviirdisoproksiilfumaraadi farmakokineetikat lastel ja noorukitel ei ole võimalik anda ebapiisavate andmete tõttu (vt lõik 4.2).
Neerukahjustus
Kliiniliste uuringute piiratud andmed toetavad Eviplera annustamist üks kord ööpäevas kerge neerukahjustusega patsientidel (kreatiniini kliirens 50 ... 80 ml / min). Eviplera emtritsitabiini ja tenofoviirdisoproksiilfumaraadi komponentide pikaajalisi ohutusandmeid ei ole kerge neerukahjustusega patsientidel siiski hinnatud. Seetõttu tuleb kerge neerukahjustusega patsientidel kasutada Eviplerat ainult juhul, kui ravi võimalik kasu kaalub üles võimalikud riskid (vt lõigud 4.2 ja 4.4).
Eviplerat ei soovitata mõõduka või raske neerukahjustusega (kreatiniini kliirens) patsientidele
Farmakokineetilised parameetrid määrati peamiselt pärast 200 mg emtritsitabiini või 245 mg tenofoviirdisoproksiili ühekordse annuse manustamist erineva raskusastmega neerupuudulikkusega patsientidele. Neerukahjustuse aste määrati kreatiniini kliirensiga (CrCL) (normaalne neerufunktsioon, kui CrCL> 80 ml / min; kerge kahjustus CrCL = 50-79 ml / min; mõõdukas kahjustus CrCL = 30-49 ml / min ja raske kahjustus CrCL = 10-29 ml / min).
Emtritsitabiini keskmine (%CV) ekspositsioon suurenes normaalse neerufunktsiooniga patsientidel 12 (25%) mcg / h / ml kuni 20 (6%) mcg / h, ml (25 (23%) mcg / h / ml ja 34 ( Vastavalt 6%) mcg • h / ml kerge, mõõduka ja neerukahjustusega patsientidel.
Keskmine (%CV) tenofoviiri ekspositsioon suurenes normaalse neerufunktsiooniga patsientidel 2185 (12%) ng • h / ml kuni 3064 (30%) ng • h / ml, 6009 (42%) ng • h / ml ja 15 985 ( 45%) ng • h / ml vastavalt kerge, mõõduka ja raske neerukahjustusega patsientidel.
Lõppstaadiumis neeruhaigusega patsientidel (lõppstaadiumis neeruhaigus(ESRD), mis vajab hemodialüüsi, suureneb ravimi ekspositsioon dialüüside vahel märkimisväärselt 53 mikrogrammi / h (ml) (72%) 72 tunni jooksul emtritsitabiini puhul ja 42 857 ng • h / ml (29%) tenofoviiri puhul 48 tunni jooksul.
Väike kliiniline uuring viidi läbi, et hinnata tenofoviirdisoproksiilfumaraadi ohutust, viirusevastast toimet ja farmakokineetikat kombinatsioonis emtritsitabiiniga HIV -nakkusega neerukahjustusega patsientidel. Patsientide alarühm, kelle kreatiniini kliirens oli algul vahemikus 50 kuni 60 ml / min, manustatuna üks kord ööpäevane annustamine näitas 2 ... 4 korda suuremat tenofoviiri ekspositsiooni ja neerufunktsiooni halvenemist.
Rilpiviriini farmakokineetikat ei ole neerupuudulikkusega patsientidel uuritud. Rilpiviriini eritumine neerude kaudu on ebaoluline. Raske neerukahjustusega või ESRD -ga patsientidel võib neerupuudulikkusest tingitud ravimi imendumise, jaotumise ja / või metabolismi muutumise tõttu olla plasmakontsentratsioon suurem. Kuna rilpiviriin seondub tugevalt plasmavalkudega, ei ole tõenäoline, et hemodialüüsi või peritoneaaldialüüsi abil (vt lõik 4.9).
Maksakahjustus
Eviplera annust ei ole vaja muuta, kuid mõõduka maksakahjustusega patsientidel tuleb olla ettevaatlik. Eviplerat ei ole uuritud raske maksakahjustusega (CPT aste C) patsientidel. Seetõttu ei ole Eviplerat soovitatav kasutada raske maksakahjustusega patsientidel (vt lõigud 4.2 ja 4.4).
Emtritsitabiini farmakokineetikat ei ole uuritud erineva raskusastmega maksapuudulikkusega patsientidel.
Rilpiviriinvesinikkloriid metaboliseerub ja eritub peamiselt maksas. Uuringus, milles võrreldi 8 kerge maksakahjustusega (CPT aste A) patsienti 8 sobiva kontrolliga ja 8 mõõduka maksakahjustusega patsienti (CPT aste B) 8 sobiva kontrolliga, oli rilpiviriini korduvate annuste manustamine kergete patsientidega 47% kõrgem. maksapuudulikkus ja 5% kõrgem mõõduka maksakahjustusega patsientidel. Rilpiviriini ei ole uuritud raske maksakahjustusega (CPT klass C) patsientidel (vt lõik 4.2). Seda ei saa siiski uurida. välistada võimalus, et farmakoloogiliselt aktiivne rilpiviriin suureneb mõõduka kahjustuse korral märkimisväärselt.
Tenofoviirdisoproksiili ühekordne 245 mg annus manustati mitte-HIV-nakkusega isikutele, kellel oli erineva raskusastmega maksakahjustus, nagu on määratletud CPT klassifikatsioonis. Maksakahjustusega patsientidel ei muutunud tenofoviiri farmakokineetika oluliselt, mis viitab sellele, et neil patsientidel ei ole vaja annust kohandada. Keskmine (%CV) tenofoviiri Cmax ja AUC0-∞ väärtused olid normaalsetel isikutel vastavalt 223 (34,8%) ng / ml ja 2050 (50,8%) ng • h / ml, võrreldes 289 (46,0%) ng / ml ja 2310 (43,5%) ng • h / ml mõõduka maksakahjustusega isikutel ning 305 (24,8%) ng / ml ja 2740 (44,0%) ng • h / ml raske maksakahjustusega isikutel.
Kaasinfektsioon B- ja / või C-hepatiidi viirusega
Üldiselt oli emtritsitabiini farmakokineetika HBV -ga nakatunud patsientidel sarnane tervete ja HIV -nakkusega patsientide omaga.
Populatsiooni farmakokineetilised analüüsid näitavad, et samaaegsel nakatumisel B- ja / või C-hepatiidi viirusega ei ole kliiniliselt olulist mõju rilpiviriini ekspositsioonile.
Üleminek efavirenssipõhiselt raviskeemilt
Uuringu GS-US-264-0111 efektiivsusandmed (vt lõik 5.1) näitavad, et lühike rilpiviriiniga kokkupuute aeg ei muuda Eviplera viirusevastast toimet. Pärast efavirensi plasmakontsentratsiooni langust vähenes induktiivne toime ja rilpiviriin kontsentratsioon hakkas normaliseeruma. Ravijärgsel perioodil, mil efavirensi plasmakontsentratsioon vähenes ja rilpiviriini plasmakontsentratsioon suurenes, ei olnud ühelgi patsiendil efavirensi või rilpiviriini tase samal ajal alla vastava IC90 taseme. Pärast efavirensi sisaldavalt ravirežiimist üleminekut ei ole annuse kohandamine vajalik.
05.3 Prekliinilised ohutusandmed -
Mittekliinilised andmed emtritsitabiini kohta ei ole näidanud kahjulikku toimet inimesele ohutuse farmakoloogia, korduvdoosi toksilisus, genotoksilisus, kantserogeenne toime ja toksilisus reproduktsioonile ja arengule.
Rilpiviriinvesinikkloriidi mittekliinilised andmed ei näita uuringute põhjal erilist ohtu inimestele ohutuse farmakoloogia, ravimite paigutus, genotoksilisus, kantserogeenne potentsiaal ning reproduktiiv- ja arengutoksilisus. Närilistel on täheldatud maksaensüümide indutseerimisega seotud maksatoksilisust Koertel on täheldatud kolestaasiga sarnast toimet.
Rilpiviriini kartsinogeensusuuringud hiirtel ja rottidel näitasid nende liikide puhul spetsiifilist kantserogeensust, kuid seda ei peetud inimestele oluliseks.
Loomkatsed on näidanud rilpiviriini piiratud läbipääsu platsentasse. Ei ole teada, kas rilpiviriin kandub platsentasse rasedatel. Rottidel ja küülikutel ei ilmnenud rilpiviriiniga teratogeensust.
Mittekliinilised andmed tenofoviirdisoproksiilfumaraadi kohta ei näita tavapäraste uuringute põhjal erilist ohtu inimestele ohutuse farmakoloogia, genotoksilisus, kantserogeenne potentsiaal ning toksilisus reproduktsioonile ja arengule. Korduva annuse toksilisuse uuringute tulemused, mis viidi läbi rottidel, koertel ja ahvidel kliinilise ekspositsiooni tasemega või sellest kõrgemal tasemel ja millel on võimalik kliiniline tähtsus, hõlmavad muutusi neerudes ja luudes ning seerumi fosfaatide kontsentratsiooni vähenemist. Luu diagnoositi osteomalaatsiana (ahvidel ) ja vähenenud BMD (luude mineraalne tihedus) (rottidel ja koertel).
Emtritsitabiini ja tenofoviirdisoproksiilfumaraadi kombinatsiooni kuni ühekuulise kestusega genotoksilisuse uuringutes ja korduvannuse toksilisuse uuringutes ei täheldatud toksikoloogiliste toimete süvenemist võrreldes üksikute komponentidega tehtud uuringutega.
06.0 FARMATSEUTILINE TEAVE -
06.1 Abiained -
Tahvelarvuti tuum
Kroskarmelloosnaatrium
Laktoosmonohüdraat
Magneesiumstearaat
Mikrokristalne tselluloos
Polüsorbaat 20
Povidoon
Eelželatiniseeritud maisitärklis
Kattekile
Hüpromelloos
Indigokarmiini alumiiniumjärv
Laktoosmonohüdraat
Polüetüleenglükool
Punane raudoksiid
Oranž kollane alumiiniumlakk (E110)
Titaan dioksiid
Triatsetiin
06.2 Sobimatus "-
Ei ole asjakohane.
06.3 Kehtivusaeg "-
3 aastat.
06.4 Säilitamise eritingimused -
Hoida originaalpakendis, niiskuse eest kaitstult.
06.5 Vahetu pakendi iseloom ja pakendi sisu -
Suure tihedusega polüetüleenist (HDPE) pudel lastekindla polüpropüleenist korgiga, mis sisaldab 30 õhukese polümeerikattega tabletti ja kuivatusainena silikageeli.
Saadaval on järgmised pakendi suurused: väliskarp, mis sisaldab 1 pudelit 30 õhukese polümeerikattega tabletti, ja välispakend, mis sisaldab 90 (3 pudelit 30) õhukese polümeerikattega tabletti. Kõik pakendi suurused ei pruugi olla müügil.
06.6 Kasutamis- ja käsitsemisjuhised -
Kasutamata ravim ja sellest tekkinud jäätmed tuleb hävitada vastavalt kohalikele eeskirjadele.
07.0 MÜÜGILOA HOIDJA -
Gilead Sciences Intl Ltd.
Cambridge
CB21 6GT
Ühendkuningriik
08.0 MÜÜGILOA NUMBER -
EL/1/11/737/001
EL/1/11/737/002
041711019
041711021
09.0 MÜÜGILOA VÕI UUENDAMISE KUUPÄEV -
Müügiloa esmase väljastamise kuupäev: 28. november 2011
Viimane uuendamiskuupäev: {DD kuu YYYY}
10.0 TEKSTI LÄBIVAATAMISE KUUPÄEV -
D.CCE 22.07.2016