Mis on Foscan?
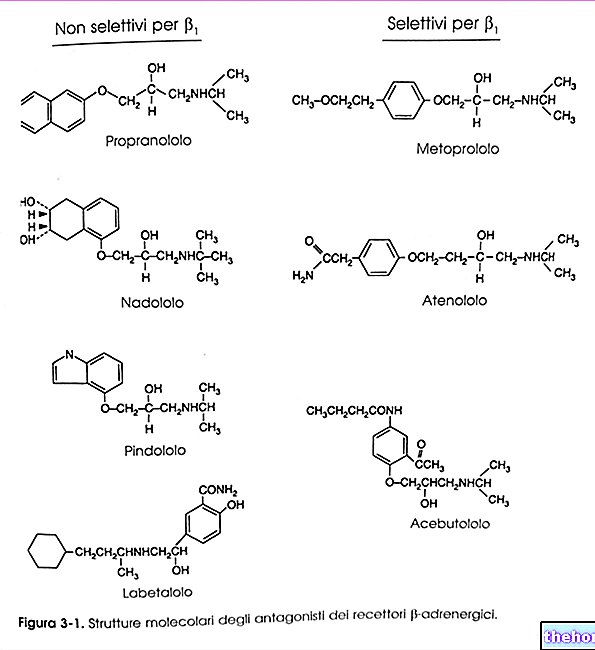
Foscan on süstelahus, mis sisaldab toimeainena temoporfiini (1 või 4 mg / ml).
Milleks Foscanit kasutatakse?
Foscanit kasutatakse pea ja kaela kaugelearenenud lamerakk -kartsinoomi (vähitüüp, mis algab suu, nina, kõri või kõrva vooderdavatest rakkudest) sümptomite leevendamiseks. Seda kasutatakse patsientidel, kellel ei ole muud ravi. enam efektiivsed ega sobi kiiritusravi (kiiritusravi), operatsiooni või süsteemse keemiaravi jaoks (ravimid, mida kasutatakse vähi ravis; "süsteemne" tähendab, et need on mõeldud kogu kehale toimimiseks).
Ravimit saab ainult retsepti alusel.
Kuidas Foscanit kasutatakse?
Foscanit tohib manustada ainult vähiravile spetsialiseerunud keskuses, kus meeskond saab hinnata patsiendi ravi fotodünaamilise ravi (ravi, mis kasutab valgust) kogemusega arsti järelevalve all. Ravi Foscaniga on kaheastmeline protsess: ravim manustatakse esmalt ja seejärel aktiveeritakse laseriga. Ravimit manustatakse püsiva intravenoosse kanüüli kaudu (õhuke tuub, mis on sisestatud püsivalt veeni) ühekordse aeglase süstiga vähemalt kuue minuti jooksul. Annus on 0,15 mg kehakaalu kilogrammi kohta. Neli päeva hiljem peaks kogu kasvajast mõjutatud piirkond olema valgustatud, kuni 0,5 cm ümbritsevast servast kaugemal, kasutades laserkiirguse poolt tekitatud valgust lainepikkusel umbes 3 minuti ja 20 sekundi jooksul, kasutades kiudoptilist kaablit. Iga kasvajakoe piirkonda tuleks valgustada ainult üks kord iga ravi ajal.Ravi ajal tuleb teised kehapiirkonnad valguse eest varjata, nii et ravim aktiveerub ainult kasvajal. Kui on vaja teist tsüklit, tuleks seda teha vähemalt nelja nädala intervalliga.
Kuidas Foscan toimib?
Foscanis sisalduv toimeaine temoporfiin on valgustundlik aine (aine, mis muutub valguse käes). Pärast Foscani süstimist jaotub temoporfiin kogu kehas, kaasa arvatud kasvaja mass. Kui see on laservalgusega ühes valgustatud
antud lainepikkusel aktiveerub temoporfiin ja reageerib rakkudes oleva hapnikuga, luues väga reaktiivse ja toksilise hapniku tüübi. See tapab rakke, reageerides nende komponentidega (valgud ja DNA) ning hävitades need. Piirates valgustuse ainult kasvajaga, kahjustatakse ainult kasvajarakke, mõjutamata seejuures teisi kehaosi.
Kuidas Foscanit uuriti?
Foscanit uuriti neljas põhiuuringus, milles osales kokku 409 pea- või kaelavähiga patsienti. Esimese kolme uuringu eesmärk oli uurida, kas vähk paranes pärast kuni kolme ravikuuri Foscaniga kokku 189 patsiendil. Neljas uuring keskendus sümptomite vähendamisele 220 kaugelearenenud pea- ja kaelavähiga patsiendil, kes ei saanud operatsiooni ega kiiritusravi. Kõigis uuringutes hinnati ravivastust 12. ja 16. nädala vahel pärast viimast Foscan -tsüklit; siiski ei võrreldud Foscani teiste ravimitega.
Milles seisneb uuringute põhjal Foscan kasulikkus?
Esimese kolme uuringu tulemused ei tundunud piisavad, et kinnitada Foscani efektiivsust pea- ja kaelavähi likvideerimisel.Teisest küljest näitas uuringus, milles hinnati kaugelearenenud pea- ja kaelavähiga patsientide sümptomite paranemist, 28 patsiendil (22%) 128 -st vaadeldavast isikust kõige tülikamate sümptomite märkimisväärne paranemine. Kasvaja suuruse vähenemist täheldati ka umbes veerandil selles uuringus osalenud patsientidest.
Mis riskid Foscaniga kaasnevad?
Foscani kõige sagedasemad kõrvaltoimed (esinenud rohkem kui 1 patsiendil 10 -st) on valu süstekohas, kasvajas või näos, verejooks, armid, suu nekroos (rakkude või kudede surm suus) , düsfaagia (neelamisraskused), näo turse (turse) ja kõhukinnisus Foscani kohta teatatud kõrvalnähtude täieliku loetelu leiate pakendi infolehelt.
Foscanit ei tohi kasutada inimesed, kes võivad olla ülitundlikud (allergilised) temoporfiini või selle mõne koostisosa suhtes. Foscanit ei tohi kasutada patsientidel, kellel on porfüüria (võimetus metaboliseerida porfüriine), muud valguse poolt süvenenud haigused, porfüriiniallergia või kasvajad, mis levivad veresoontesse või on valgustuskoha lähedal. Foscanit ei tohi anda ka patsientidele, kellele järgneva 30 päeva jooksul tehakse operatsioon, samuti silmahaigusega patsientidele, kes vajavad "pilulambi" hindamist (vahend, mida silmaarstid kasutavad silma vaatamiseks). järgmise 30 päeva jooksul või patsientidele, keda ravitakse juba mõne teise ravimiga, mis suurendab valgustundlikkust.
Kuue kuu jooksul pärast Foscan'i süstimist peaksid patsiendid vältima ereda valguse käes viibimist, et vältida nahapõletuse ohtu. Lisateavet leiate pakendi infolehelt.
Miks Foscan heaks kiideti?
Inimtervishoius kasutatavate ravimite komitee jõudis järeldusele, et Foscani toime kaugelearenenud pea- ja kaelavähiga seotud sümptomite leevendamisel on tähelepanuväärne. Seetõttu otsustas komitee, et Foscani kasulikkus patsientide palliatiivseks raviks on suurem kui sellega kaasnevad riskid. pea ja kaela kaugelearenenud lamerakk -kartsinoomiga, kellel on varasem ravi ebaõnnestunud ja kes ei sobi kiiritus-, kirurgia- ega süsteemseks keemiaraviks. Komitee soovitas Foscani müügiloa vabastada.
Algselt anti Foscanile müügiluba erandlikel asjaoludel, kuna haigus on haruldane ja teaduslikel põhjustel oli teavet loa andmise ajal napilt. Kuna ettevõte esitas nõutud lisateabe, piiras erandlike asjaolude "eemaldati 21. mail 2008.
Muu teave Foscani kohta:
24. oktoobril 2001 andis Euroopa Komisjon Foscanile müügiloa, mis kehtib kogu Euroopa Liidus.
kaubandust uuendati 24. oktoobril 2006. Müügiloa omanik on ettevõte Biolitec Pharma ltd.
Foscan EPARi täisversiooni leiate siit.
Selle kokkuvõtte viimane uuendus: 05-2008
Sellel lehel avaldatud teave Foscan -temoporfiini kohta võib olla aegunud või puudulik. Selle teabe õigeks kasutamiseks vaadake vastutusest loobumise ja kasuliku teabe lehte.