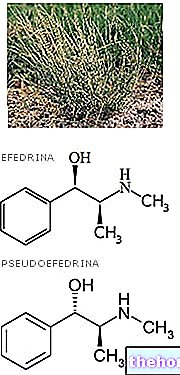
Toimeained: klomifeen (klomifeentsitraat)
CLOMID 50 mg tabletid
Miks kasutatakse Clomidi? Milleks see mõeldud on?
FARMAKOTERAPEUTILINE KATEGOORIA
CLOMIDi toimeaine klomifeentsitraat on sünteetiline mittesteroidne östrogeen, mis on efektiivne ovulatsiooni esilekutsumiseks naistel, kellel on anovulatsioonitsükkel ja ebapiisav luteaalfaasi tsükkel.
RAVI NÄIDUSTUSED
CLOMID on näidustatud ovulatsiooni puudumise raviks rase soovivatel patsientidel, kui on kindlaks tehtud piisav munasarjade funktsioon. Endogeensete estrusgeenide hea tase (tuvastatav tupe määrimise, endoomi trio biopsia, östrogeeni uriiniannuse või verejooksu tõttu progesteroonile) on soodsad prognostilised elemendid. Östrogeeni taseme langus ei välista alati edukat ravi
Vastunäidustused Kui Clomidi ei tohi kasutada
CLOMIDi ei tohi raseduse ajal manustada, kuna rottidel ja küülikutel, kellele ravimit manustati tiinuse ajal, on täheldatud väärarenguid. Et vältida CLOMIDi tahtmatut manustamist raseduse alguses, tuleb ravitsüklite ajal mõõta basaaltemperatuuri.
CLOMID on vastunäidustatud patsientidele, kellel on aktiivne maksahaigus või kellel on teadaolev maksafunktsiooni häire.
CLOMID on vastunäidustatud ka menometrorraagiaga patsientidel ja hormoonsõltuvate neoformatsioonide kandjatel.
Ettevaatusabinõud kasutamisel Mida on vaja teada enne Clomidi võtmist
Diagnoos enne CLOMID -ravi
Enne ravi on kohustuslik põhjalik vaagnauuring ja seda tuleb korrata enne iga järgmist ravitsüklit. CLOMIDi ei tohi manustada munasarjatsüsti (või munasarju hõlmava endometrioosi) juuresolekul edasise laienemise ohu tõttu. Samal põhjusel tuleb olla ettevaatlik klomifeeni kasutamisel emaka fibroidide juuresolekul.
Nägemishäired
Kui CLOMID -ravi ajal tekivad mööduvad nägemishäired, nagu hägustumine, laigud, vilkumine (vt „Erihoiatused“), tuleb ravi CLOMIDiga kohe lõpetada.
Munasarjade hüperstimulatsioon CLOMID -ravi ajal
Patsiente tuleb soovitada teavitada oma arsti kõhu- või vaagnavalu, kehakaalu tõusu, kõhupuhitusnähtude või -tunde tekkimisest.
Maksimaalne CLOMID-i poolt põhjustatud munasarjade suurenemine, olenemata sellest, kas see on füsioloogiline või ebanormaalne, ilmneb alles mitu päeva pärast soovitatud CLOMID-annuse katkestamist. Olge ettevaatlik kõhu ja vaagna hoolika uurimise suhtes. Kui tekib munasarjade suurenemine, tuleb CLOMID peatada, kuni munasarjad on taastunud nende ravieelsele suurusele ja järgmise tsükli annust või kestust tuleks vähendada. Kogemused on näidanud, et munasarjade suurenemine ja tsüstide moodustumine koos CLOMID -raviga taanduvad spontaanselt mõni päev või nädal pärast ravi lõpetamist.
Koostoimed Millised ravimid või toiduained võivad muuta Clomidi toimet
Puuduvad teadaolevad kliiniliselt olulised koostoimed teiste ravimitega.
Hoiatused Oluline on teada, et:
Kliiniline kogemus on näidanud, et mitmikraseduste esinemissagedus suureneb, kui rasestumine toimus CLOMID -ravi käigus. Uuritud 2369 rasedusega rühmas oli 2183 (92,1%) üksik, 165 (6,9%kaksik), 11 (0,5%) kolmiknärvi, 7 (0,3%) neljakordne ja 3 (0, 13%) viie lapsega. Seetõttu oli 186 rasedust (võrdne 7,9%) mitmekordne.
Nii patsienti kui ka partnerit tuleb enne ravi alustamist nendest võimalustest ja mitmikraseduse võimalikest tüsistustest teavitada.165 kaksikrasedusest oli homosügootsete ja dizigootiliste kaksikute suhe 1 kuni 5.
CLOMID -i kasutamisega seotud raseduse väärarengute üldine esinemissagedus oli kirjanduses üldpopulatsioonile teatatud piirides. On pakutud trisoomiate ja Downi sündroomi riski võimalikku suurenemist, kuid vaatluste vähesus ei võimalda täna seda hüpoteesi kinnitada või mitte ja seega õigustada süstemaatilist amniotsenteesi, kui puuduvad muud tegurid, nagu vanus. Arenenud või perekond ajalugu. Abordi või loote surma esinemissagedus oli 21,4% (spontaanne abort 19% -l), emakaväline rasedus 1,18%, samas kui 0,17, 0,04 ja 1,01% vastasid vastavalt hüdrokujulisele moolile, papüüruslootele ja surnultsündimisele.
Kasutamine raseduse ja imetamise ajal.
CLOMIDi ei tohi manustada raseduse ja kahtlustatava raseduse ajal. Mõnel juhul on täheldatud piima koguse ja laktatsiooniperioodi vähenemist.
Mõju autojuhtimise ja masinate käsitsemise võimele.
Aeg -ajalt esinevad mööduvad nägemishäired, nagu uduvihm, laigud, vilkumine, võivad mõjutada sõiduki juhtimist või masinate käsitsemist, eriti muutliku valgustingimuse korral (vt „Ettevaatusabinõud kasutamisel”).
Neile, kes tegelevad spordiga: ravimi kasutamine ilma terapeutilise vajaduseta kujutab endast dopingut ja võib igal juhul määrata positiivse dopinguvastase testi. Ravim ei ole vastunäidustatud tsöliaakia all kannatavatele isikutele.
Annustamine ja kasutusviis Kuidas Clomidi kasutada: Annustamine
Patsientidel, kellel pole hiljuti olnud menstruatsiooni, võib ravi alustada igal ajal.
Kui kavatsetakse voolu esile kutsuda progestageenide manustamisega või kui see tekib spontaanselt vahetult enne kavandatud ravi, tuleb ravi 50 mg ööpäevas 5 päeva jooksul alustada ligikaudu tsükli 5. päevast.
Kui selle annuse korral toimub ovulatsioon, ei ole järgmiste ravitsüklite korral annuste suurendamisel mingit eelist.
Võimaliku raseduse eesmärgil tuleb rõhutada sobiva ajalise valiku "tähtsust" suguelu jaoks.
Kui pärast esimest ravikuuri ovulatsiooni ei teki, võib alustada teist 5-päevast ravikuuri 100 mg-ga päevas (2 tabletti 50 mg üks kord ööpäevas).
See ravikuur võib alata 30 päeva pärast eelmist.
Ravi annustega või kestusega üle 100 mg ööpäevas 5 päeva jooksul ei tohi kunagi alustada. Võimaliku 3 ravikuuri saab määrata samamoodi. Kui ovulatoorset menstruatsiooni ei saavutata pärast 3 tsüklit, tuleb diagnoos uuesti läbi vaadata.
Siiski ei ole soovitatav ravi pikendada ülaltoodud piiridest patsientidel, kellel puuduvad ovulatsiooni tunnused.
Enamikul patsientidest ilmneb ovulatsioonivastus kolme ravikuuri jooksul. CLOMIDi ei tohi manustada igakuise säilitusravina patsientidele, kellel pärast ravi lõpetamist korduvad anovulatoorsed tsüklid.
Pikaajaline klomifeeni kasutamine võib suurendada munasarjade invasiivsete metaplaasiate või pahaloomuliste kasvajate riski.
Üleannustamine Mida teha, kui olete võtnud liiga palju Clomidi
Ägeda mürgistuse juhtumeid pole registreeritud. Kroonilise mürgistuse võimalikud nähud ja sümptomid on: iiveldus ja / või oksendamine, vasomotoorne õhetus, nägemise hägustumine ja skotoomid, kõhuvalu ja / või vaagnavalu, kehakaalu tõus ja astsiit.
Kõrvaltoimed Millised on Clomidi kõrvaltoimed
Soovitatud annuste kasutamisel ei ole kõrvaltoimed silmatorkavad ja mõjutavad ravi harva. Kõige sagedasemate kõrvaltoimete hulka kuuluvad: kuumahood, ebamugavustunne kõhus (turse või valulikkus või valu), harvem iiveldus, oksendamine, kõhukinnisus ja kõhulahtisus, suurenenud munasarjad, hägune nägemine (vt "Kasutamine" ja "Erihoiatused" ) ja skotoomid.
Harvadel juhtudel on teatatud kae ja optilise neuriidi juhtudest.
Teised harvemini teatatud kaebused ravi ajal on: iiveldus või oksendamine, suurenenud närvipinge, väsimus, pearinglus või kerge peapööritus peas, unetus, valu rinnus, rikkalikum menstruatsioon, urtikaaria või allergiline dermatiit, multiformne erüteem, ekhümoos ja angioneurootiline turse, kehakaalu tõus, polüuuria või pollakiuria. Väga vähestel patsientidel leiti ka tagasihoidlik, pöörduv juuste väljalangemine, peaaegu alati pikema ravitsükli jooksul.
Klomifeenravi ajal on esinenud endometrioosi juhtumeid ja olemasoleva endometrioosi ägenemist.
Endokriinsõltuvate neoplasmide tekkimise või süvenemise kohta on üksikuid teateid. Harva on teatatud epilepsiahoogudest.
Soovitatav on teavitada raviarsti kõikidest kõrvaltoimetest, mida selles infolehes ei ole nimetatud ja mis võivad tekkida ravi ajal.
Laboratoorsed testid
32 -st 141 -st patsiendist, kellel seda mõõdeti, on teatatud rohkem kui 5% -lisest bromosulfonftaleiini retentsioonist. Teised maksafunktsiooni testid olid tavaliselt normaalsed.
Järgnevas uuringus, kus patsientidele tehti 6 järjestikust igakuist CLOMID -i tsüklit (50 ja 100 mg päevas 3 päeva jooksul) ja platseebot, viidi BSF -testid läbi 94 patsiendil. Retentsiooniväärtused olid suuremad kui 5% 11 patsiendil, kellest 6 said CLOMIDi ja 5 platseebot. Ühel patsiendil tekkis 19. ravipäeval kollatõbi (50 mg päevas); maksa biopsia näitas sapiteede staasi, millel puudusid ilmsed hepatiidi nähud.
Aegumine ja säilitamine
HOIATUS: Ärge kasutage ravimit pärast kõlblikkusaega, mis on märgitud välispakendil. Pidage meeles, et kõlblikkusaeg viitab puutumata pakendis olevale tootele, mis on õigesti hoitud.
Säilitamine: Hoiustamisel ei ole erilisi ettevaatusabinõusid.
HOIDA RAVIMPREPARAAT LASTE EEST KÄTTESAAMATUS KOHAS
Koostis ja ravimvorm
KOOSTIS
Üks tablett sisaldab:
Toimeaine: klomifeentsitraat 50 mg. Abiained: sahharoos; Laktoos; Lahustuv maisitärklis; Magneesiumstearaat; Maisitärklis; Kollane raudoksiid.
RAVIMVORM JA PAKEND
- Karp 10 tabletiga 50 mg blisterpakendis.
Allika pakendi infoleht: AIFA (Itaalia ravimiamet). Sisu avaldati jaanuaris 2016. Esitatud teave ei pruugi olla ajakohane.
Kõige ajakohasemale versioonile juurdepääsu saamiseks on soovitatav külastada AIFA (Itaalia ravimiamet) veebisaiti. Vastutusest loobumine ja kasulik teave.
01.0 RAVIMPREPARAADI NIMETUS
CLOMID
02.0 KVALITATIIVNE JA KVANTITATIIVNE KOOSTIS
Üks 320 mg tablett sisaldab:
Toimeaine: klomifeentsitraat 50 mg
Abiained: sahharoos 67,50 mg, laktoos 67,50 mg, lahustuv maisitärklis 25 mg, magneesiumstearaat 3 mg, maisitärklis 106,752 mg, kollane raudoksiid 0,248 mg
03.0 RAVIMVORM
Tabletid
04.0 KLIINILINE TEAVE
04.1 Näidustused
CLOMID on näidustatud ovulatsiooni puudumise raviks rase soovivatel patsientidel, kui on kindlaks tehtud rahuldav munasarjade funktsioon. Endogeensete östrogeenide hea tase (tuvastatav tupe määrimise, endomeetriumi biopsia, östrogeeni uriiniannuse või progesteroonivastase verejooksu tõttu) on soodsad prognostilised elemendid; östrogeeni taseme langus ei välista alati ravi edukust.
04.2 Annustamine ja manustamisviis
Patsientidel, kellel pole hiljuti olnud menstruatsiooni, võib ravi alustada igal ajal.Kui kavatsetakse voolu esile kutsuda progestageenide manustamisega või kui see juhtub spontaanselt vahetult enne kavandatud ravi, tuleb ravi 50 mg päevas 5 päeva jooksul alustada ligikaudu tsükli 5. päevast.
Kui selle annuse korral toimub ovulatsioon, ei ole järgmiste ravitsüklite korral annuste suurendamisel mingit eelist. Võimaliku raseduse eesmärgil tuleb rõhutada sobiva ajalise valiku "tähtsust" suguelu jaoks. Kui pärast esimest ravikuuri ovulatsiooni ei teki, võib alustada teist 5-päevast ravikuuri 100 mg-ga päevas (2 tabletti 50 mg üks kord ööpäevas).
See ravikuur võib alata 30 päeva pärast eelmist. Ravi annustega või kestusega üle 100 mg ööpäevas 5 päeva jooksul ei tohi kunagi alustada. Võimaliku kolmanda ravitsükli saab alustada samamoodi. Kui ovulatoorset menstruatsiooni ei saavutata pärast 3 tsüklit, tuleb diagnoos uuesti läbi vaadata.
Siiski ei ole soovitatav ravi pikendada ülaltoodud piiridest patsientidel, kellel puuduvad ovulatsiooni tunnused. Enamikul patsientidest ilmneb ovulatsioonivastus kolme ravikuuri jooksul. CLOMIDi ei tohi manustada igakuise säilitusravina patsientidele, kellel pärast ravi lõpetamist korduvad anovulatoorsed tsüklid.
04.3 Vastunäidustused
Rasedus: väärarenguid on täheldatud rottidel ja küülikutel, kes said raseduse ajal CLOMIDi; seetõttu ei tohi ravimit raseduse ajal manustada.
Et vältida Clomidi tahtmatut manustamist raseduse alguses, tuleb kõigi ravitsüklite ajal mõõta basaaltemperatuuri.
Hepatopaatiad: CLOMID -ravi on vastunäidustatud patsientidele, kellel on progresseeruv maksahaigus või kellel on anamneesis teadaolev maksafunktsiooni häire.
Menometrorraagia: CLOMID on menometrorraagiaga patsientidel vastunäidustatud.
04.4 Erihoiatused ja asjakohased ettevaatusabinõud kasutamisel
Diagnoos enne CLOMID -ravi:
Enne ravi on kohustuslik põhjalik vaagnauuring ja seda tuleb korrata enne iga järgmist ravitsüklit.
CLOMIDi ei tohi manustada munasarjatsüsti (või munasarju hõlmava endometrioosi) juuresolekul munasarjade edasise suurenemise ohu tõttu.
Nägemishäired:
CLOMID -ravi ajal võivad aeg -ajalt tekkida mööduvad nägemishäired, nagu hägustumine, laigud, vilkumine. Need võivad mõjutada teatud toimingute (nt sõiduki juhtimine või masinatega töötamine) tavapärast toimimist, eriti muutuva valgustuse korral.
Kui need ilmuvad, tuleb CLOMID -ravi jäädavalt katkestada.
Munasarjade hüperstimulatsioon CLOMID -ravi ajal:
Patsiente tuleb soovitada teavitada oma arsti kõhu- või vaagnavalu, kehakaalu tõusu, kõhupuhitusnähtude või -tunde tekkimisest. Maksimaalne CLOMID-i poolt põhjustatud munasarjade suurenemine, olenemata sellest, kas see on füsioloogiline või ebanormaalne, ilmneb alles mitu päeva pärast soovitatud CLOMID-annuse katkestamist. Patsient, kes kaebab pärast CLOMID-i manustamist vaagnavalu, tuleb hoolikalt uurida. Tekib munasarjade suurenemine, tuleb CLOMID-i peatatakse, kuni munasarjad on taastanud oma ravieelse suuruse ja järgmise tsükli annust või kestust vähendatakse. Kogemused on näidanud, et munasarjade suurenemine ja tsüstide moodustumine koos CLOMID -raviga taanduvad spontaanselt mõni päev või nädal pärast ravi lõpetamist.
Mitmikrasedus:
Kliiniline kogemus on näidanud, et mitmikraseduste esinemissagedus suureneb, kui rasestumine toimus CLOMID -ravi käigus. Uuritud 2369 rasedust sisaldavas rühmas oli 2183 (92,1%) vallaline, 165 (6,9%kaksik), 11 (0,5%) kolmikut, 7 (0,3%) nelikut ja 3 (0,13)%) viie lapsega. Seetõttu oli 186 rasedust (võrdne 7,9%) mitmekordne. Neid võimalusi ja mitmikraseduse võimalikke tüsistusi tuleb enne ravi alustamist teavitada nii patsiendile kui ka partnerile. 165 kaksikrasedusest oli homosügootsete ja dizigootiliste kaksikute suhe 1 kuni 5.
CLOMID -i kasutamisega seotud raseduse väärarengute üldine esinemissagedus oli kirjanduses üldpopulatsioonile teatatud piirides. On pakutud trisoomiate ja Downi sündroomi riski võimalikku suurenemist, kuid vaatluste vähesus ei võimalda täna seda hüpoteesi kinnitada või mitte ja seega õigustada süstemaatilist amniotsenteesi, kui puuduvad muud tegurid, nagu vanus. Arenenud või perekond ajalugu.
Abordi või loote surma esinemissagedus oli 21,4% (spontaanne abort 19% -l), emakaväline rasedus 1,18%, samas kui 0,17, 0,04 ja 1,01% vastasid vastavalt hüdrokujulisele moolile, papüüruslootele ja surnultsündimisele.
Toitmisaeg:
Mõnel juhul on täheldatud piima koguse ja laktatsiooniperioodi vähenemist.
Enne ravi tuleb läbi viia vaagna põhjalik uurimine ja korrata enne iga järgmist ravikuuri. Munasarjade edasise suurenemise ohu tõttu ei tohi CLOMIDi manustada munasarjatsüsti juuresolekul. Erilist tähelepanu tuleks pöörata patsientidele, kes on reproduktiivse elu kaugelearenenud staadiumis anovulatoorsete häirete suurema esinemissageduse või suurenenud kalduvuse tõttu endomeetriumi kartsinoomide tekkele. Sarnast tähelepanu tuleb pöörata patsientidele, kellel on enne ravi ebanormaalne verejooks; eriti on vajalik tagamaks, et neoplastiliste kahjustuste esinemine ei oleks vaatlusest kõrvale jäänud. Mõlemas patsiendikategoorias on vaja teha endomeetriumi biopsia, enne ravi CLOMIDiga peab alati eelnema maksafunktsiooni kliiniline hindamine. Munasarjade ebanormaalse suurenemise ohu minimeerimiseks tuleb kasutada väikseimat CLOMIDi annust, mis sobib positiivse tulemuse saamiseks. Mõnedel polütsüstiliste munasarjade sündroomiga patsientidel võib CLOMIDi tavaliste annuste korral olla liialdatud reaktsioon. Sellisel juhul on soovitatav vähendada annuseid ja tsükli pikkusi. Lõpuks tuleb meeles pidada, et munasarjade maksimaalne suurenemine, olgu see siis füsioloogiline või ebanormaalne, toimub alles mitu päeva pärast soovitatud CLOMID -annuste peatamist.
04.5 Koostoimed teiste ravimitega ja muud koostoimed
Puuduvad teadaolevad kliiniliselt olulised koostoimed teiste ravimitega.
04.6 Rasedus ja imetamine
Ravimit ei tohi kasutada raseduse ja imetamise ajal
04.7 Mõju autojuhtimise ja masinate käsitsemise võimele
Vt lõik 4.4 "Hoiatused ja ettevaatusabinõud kasutamisel"
04.8 Kõrvaltoimed
Soovitatud annuste kasutamisel ei ole kõrvaltoimed silmatorkavad ja mõjutavad ravi harva. Kõige sagedasemate kõrvaltoimete hulka kuuluvad: kuumahood, ebamugavustunne kõhus (puhitus või valulikkus või valu), harvem iiveldus, oksendamine, kõhukinnisus ja kõhulahtisus, suurenenud munasarjad, hägune nägemine (vt „Hoiatused ja ettevaatusabinõud“) ja skotoomid.
Harvadel juhtudel on teatatud kataraktist.
Teised harvemini teatatud häired ravi ajal on:
iiveldus või oksendamine, suurenenud närvipinge, väsimus, pearinglus või kerge peapööritus peas, unetus, valu rinnus, rasked perioodid, urtikaaria või allergiline dermatiit, multiformne erüteem, ekseem ja angioneurootiline turse, kehakaalu tõus, polüuuria või pollakiuria. Tagasihoidlikku, pöörduvat juuste väljalangemist leiti ka väga vähestel patsientidel, peaaegu alati pikaajaliste ravikuuride ajal.
Laboratoorsed testid:
32 -st 141 -st patsiendist, kellel seda mõõdeti, on teatatud üle 5% -lisest bromosulfonftaleiini retentsioonist. Teised maksafunktsiooni testid olid tavaliselt normaalsed.
Järgnevas uuringus, kus patsientidele tehti 6 järjestikust igakuist CLOMID -i kuuri (50 ja 100 mg päevas 3 päeva jooksul) ja platseebot, viidi BSF -i uuringud läbi 94 patsiendil. Retentsiooniväärtused olid suuremad kui 5% 11 patsiendil, kellest 6 said CLOMIDi ja 5 platseebot. Ühel patsiendil tekkis 19. ravipäeval kollatõbi (50 mg päevas); maksa biopsia näitas sapiteede staasi, millel puudusid ilmsed hepatiidi nähud.
04.9 Üleannustamine
Ägeda mürgistuse juhtumeid pole registreeritud.
Kroonilise mürgistuse võimalikud nähud ja sümptomid on: iiveldus ja / või oksendamine, vasomotoorne õhetus, nägemise hägustumine ja skotoomid, kõhuvalu ja / või vaagnavalu, kehakaalu tõus ja astsiit.
05.0 FARMAKOLOOGILISED OMADUSED
05.1 Farmakodünaamilised omadused
CLOMIDi toimeainet esindab klomifeentsitraat, sünteetiline östrogeen suukaudseks kasutamiseks, mittesteroidne, efektiivne ovulatsiooni esilekutsumiseks naistel, kellel on anovulatsioonitsükkel ja ebapiisav luteaalfaas. Klomifeen koosneb kahe isomeeri ratseemilisest segust, mida nimetatakse vastavalt tsisklomifeeniks ja transklomifeeniks, ning see on isoleeritud klorotrianisene analoogide ja derivaatide uurimisel, mille kasutamist on esile tõstetud östrogeenist sõltuvate patoloogiliste olukordade ravis ja Arvukad loomadega läbi viidud farmakoloogilised ja bioloogilised uuringud on näidanud, et klomifeen toimib nõrga östrogeeni ja antiöstrogeenina. Leiti, et ravim suudab normaalsetel rottidel tõkestada inna tsükli, vältida östrogeenide uterotroofset toimet normaalsetel või kastreeritud rottidel, takistada looduslike östrogeenide antiovulatoorset toimet ja takistada tõeliste looduslike östrogeenide fikseerimist. spetsiifilised emaka-, piimanäärme- ja võimalik, et ka hüpotalamuse retseptorid. Klomifeeni östrogeenivastane toime näib olevat seotud hüpotalamuse ja hüpofüüsi keskse toimega. Tänu hüpotaalamuse östrogeeniretseptorite blokeerivale toimele ja sellest tulenevalt suurenenud hüpofüüsi gonadotropiinide (eriti FSH, mis mõjutab spetsiifiliselt folliikulite küpsemise mehhanisme munasarjade tasandil) sekretsioonile, jäljendab see ühend enneaegset füsioloogilist suurenemist. folliikulite gonadotropiin - stimuleeriv, nii et see võib omakorda alustada folliikulite seeria küpsemist, nagu tavaliselt iga tsükli alguses. Seetõttu loob klomifeen tingimused sööda poolt indutseeritud järgnevaks ovulatsiooniks. positiivne tagasi et saavutatud kõrged östrogeenimäärad tekitavad hüpofüüsi taset .. klomifeenil puudub nii androgeenne kui ka antiandrogeenne toime; see ei avalda mõju hüpofüüsi-neerupealiste teljele ja hüpofüüsi-kilpnäärme teljele; see ei muuda basaalse ultraheli jälgimist isegi kliinikus soovitatutest oluliselt suuremate annuste korral ega mõjuta vererõhu ja hingamisega seotud normaalseid väärtusi. Ravim määrab basaaltemperatuuri tõusu, kuid ei muuda või mõnel juhul rõhutab progestiini aktiivsusele tüüpiliste tupe tsütoloogiliste modifikatsioonide normaalset välimust.
05.2 Farmakokineetilised omadused
Pärast suukaudset manustamist imendub klomifeen kiiresti ja eritub peamiselt väljaheitega. Märgistatud ravimiga läbi viidud uuringutes hinnati plasma poolväärtusaega rottidel intravenoosseks manustamiseks 24 tunniks ja ahvidele intravenoosseks manustamiseks 48 tunniks.
Entero-maksa tsirkulatsiooni olemasolu tõestati nii rottidel kui ahvidel. Viimaste loomaliikide puhul pärast kuue päeva möödumist suukaudsest ravist, kui ligikaudu 90% manustatud annusest oli juba väljaheitega eritunud ja vähemal määral leiti uriinis maksas ja sapis maksimaalne jääkkontsentratsioon 14C; samas kui minimaalseid koguseid leiti neerupealistes, silma koes, kõhunäärmes, hüpofüüsis ja munasarjades. Intravenoosselt leiti kõrget 14C taset silmakoes nii rottidel kui küülikutel ja ahvidel. Kahe isomeeri jaotusmudel erinevates kudedes ja elundites oli väga sarnane klomifeeniga, mis sisaldas klomifeeni cis- ja trans -vormide segu, kuna kõrgeimad kontsentratsioonid saadi maksas, neerupealistes, silmas, munasarjas ja hüpofüüsis. transklomifeeni suurem afiinsus rasvkoe suhtes selgitada selle isomeeri aeglast ja kahefaasilist eritumist.
14C-märgistatud ravimiga inimestel läbi viidud uuringud näitasid ka, et imendumine pärast suukaudset manustamist on kiire ja eliminatsioon toimub peamiselt väljaheitega, 51% esimese 5 päeva jooksul, samal ajal kui ühendi jäägid ja nende metaboliidid elimineeritakse aeglaselt järgmise 5 nädala jooksul, tõenäoliselt enterohepaatilise retsirkulatsiooni kaudu. 100 mg klomifeeniga ravitud patsientidel on kahe isomeeri kontsentratsioon vastavalt tsisklomifeeni ja transklomifeeni puhul 14,6 ng / ml ja 30,4 ng / ml; annuses 150 mg need väärtused olid vastavalt 42,3 ja 80,9 mg / ml.
Klomifeen metaboliseeritakse katselooma mikrosomaalsete ensüümide toimel, moodustades desetüülklomifeeni, 4-hüdroksüklomifeeni ja klomifeen-N-oksiidi.
05.3 Prekliinilised ohutusandmed
Klomifeeni äge toksilisus on nii suukaudseks kui ka parenteraalseks manustamiseks väga madal. Hiirtel oli erinevates laborites saadud LD50 1700-1919 mg / kg suu kaudu, 350-390 mg / kg intravenoosselt ja 86 mg / kg intravenoosselt. Rottidel on äge toksilisus veelgi madalam, mille tulemuseks on suukaudne LD50 5504-5750 mg / kg ja endoperitoneaalselt 449-530 mg / kg. Need andmed näitavad, et hiirtel ja rottidel suukaudselt arvutatud LD50 väärtused on vastavalt ligikaudu 1919 ja 5750 korda suuremad kui kliinikus soovitatud ravimi annused. Endoperitoneaalse ja suukaudse manustamise võrdluskatsete tulemused näitasid samuti, et klomifeeni ning selle kahe eksomeeri tsisklomifeeni ja transklomifeeni LD50 väärtuste vahel ei ole olulisi erinevusi.
Kroonilise toksilisuse testide tulemused rottidel ja koertel 53 -nädalase korduva suukaudse ravi korral (annused 5, 15 ja 40 mg / kg päevas) ja 180 päeva minisiga (5,40 mg / kg päevas) näitasid, et klomifeen võib ainult terapeutilistest annustest suurematel annustel põhjustada mõningaid kõrvaltoimeid, mis tuleb seostada ühendi omapärase farmakodünaamilise toimega. Tegelikult võivad kehakaalu ja alopeetsia ilmnemise erinevused olla seotud ravimi östrogeense aktiivsusega, kuna on teada, et östrogeenid pärsivad kehakaalu ja põhjustavad juuste kasvu muutusi. Katarakti ilmnemine rottidel võib olla tingitud klomifeeni toimest kolesterooli ainevahetusele, mille tulemuseks on desmosterooli taseme tõus. Reproduktiivsüsteemile leitud toksiline toime nii meestel kui ka naistel võib väljendada klomifeeni farmakoloogilise toime tulemust, pidades eelkõige silmas selle omapärast toimemehhanismi kesktasandil. Reproduktsiooniuuringute ajal hiirtele, rottidele ja küülikutele manustatud klomifeen põhjustas kliinikus soovitatud annustest üldiselt suuremate annuste korral soovimatuid toimeid fertiilsusele, tiinusele ning loote ja vastsündinu arengule. Need modifikatsioonid, mis tuleb seostada ravimi östrogeense toimega, näivad olevat tingitud katsetes kasutatud loomaliigist, arvestades, et ahvil ei täheldatud teratogeenset toimet isegi naistel kasutatavatest annustest oluliselt suuremate annuste korral.
Mutageensuse testid, mis viidi läbi in vitro Amesi ja DNA parandustestide abil ning in vivo, hinnates kromosomaalseid aberratsioone mikrotuumakatses, andsid negatiivseid tulemusi selles mõttes, et need ei näidanud klomifeeni tekitatud mutageenset toimet.
06.0 FARMATSEUTILINE TEAVE
06.1 Abiained
Sahharoos, laktoos, lahustuv maisitärklis, magneesiumstearaat, maisitärklis, kollane raudoksiid
06.2 Sobimatus
Ühtegi sobimatut juhtumit ei ole esile tõstetud.
06.3 Kehtivusaeg
5 aastat.
06.4 Säilitamise eritingimused
Puudub.
06.5 Vahetu pakendi iseloomustus ja pakendi sisu
Karp, mis sisaldab 10 tabletti 50 mg
06.6 Kasutamis- ja käsitsemisjuhised
-----
07.0 MÜÜGILOA HOIDJA
BRUNO FARMACEUTICI S.p.A. - Via Delle Ande, 15 - 00144 ROOMA
08.0 MÜÜGILOA NUMBER
Kood nr. 020773026
09.0 MÜÜGILOA VÕI UUENDAMISE KUUPÄEV
Juuni 2000
10.0 TEKSTI LÄBIVAATAMISE KUUPÄEV
Juuni 2000