Mis on Vidaza?
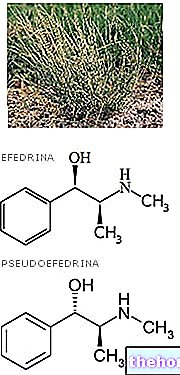
Vidaza on pulber, millest valmistatakse süstesuspensioon. Selles sisalduv toimeaine on asatsitidiin.
Milleks Vidazat kasutatakse?
Vidaza on näidustatud järgmiste haigustega täiskasvanud patsientide raviks, kes ei saa luuüdi siirdada:
- müelodüsplastilised sündroomid, mis on haiguste rühm, mille puhul luuüdi toodab ebapiisavat arvu vererakke. Mõnel juhul võivad need sündroomid põhjustada ägeda müeloidse leukeemia (AML) arengut, mis on vähitüüp, mis mõjutab teatud valgeid vereliblesid, müeloidrakke. Vidaza't kasutatakse patsientidel, kellel on keskmine või kõrge risk haigestuda AML -i või surra;
- krooniline müelomonotsüütiline leukeemia (KML), vähitüüp, mis mõjutab teatud valgeid vereliblesid, monotsüüte. Vidazat kasutatakse juhul, kui luuüdi koosneb 10–29% ebanormaalsetest rakkudest ja ei tooda piisavalt valgeid vereliblesid;
- AML pärast müelodüsplastilist sündroomi. Vidaza’t kasutatakse ainult siis, kui luuüdi koosneb 20–30% ebanormaalsetest rakkudest.
Kuna nende haigustega patsientide arv on väike, peetakse neid haigusi haruldasteks ja seetõttu määrati Vidaza 6. veebruaril 2002 müelodüsplastiliste sündroomide ja 29. novembril 2007 AML -i jaoks harva kasutatavaks ravimiks (haruldaste haiguste raviks kasutatav ravim). Selle määramise ajal klassifitseeriti LMMC müelodüsplastiliste sündroomide hulka.
Ravimit saab ainult retsepti alusel.
Kuidas Vidazat kasutatakse?
Ravi Vidazaga peab alustama ja jälgima keemiaravi kogemustega arsti järelevalve all. Enne Vidaza -ravi alustamist tuleb patsientidele anda iivelduse ja oksendamise ravimeid.
Vidaza soovitatav algannus on 75 mg kehapinna ruutmeetri kohta (arvutatakse patsiendi kehakaalu ja pikkuse alusel) ning seda manustatakse nahaaluse süstena õlavarre, reie või kõhu alla iga päev ühe nädala jooksul, millele järgneb kolm nädalat ilma ravita. See nelja nädala pikkune periood moodustab "tsükli". Ravi jätkub vähemalt kuus tsüklit ja seejärel seni, kuni patsient sellest kasu saab. Enne iga
tuleb kontrollida teie maksa, neere ja verd. Kui vereanalüüs langeb liiga madalale või kui patsiendil tekivad neeruprobleemid, lükatakse järgmine ravi edasi või viiakse läbi vähendatud annusega. Raskete maksaprobleemidega patsiente tuleb hoolikalt jälgida kõrvaltoimete suhtes, kuid Vidaza't ei tohi kasutada kaugelearenenud maksavähiga patsientidel.
Kõik üksikasjad leiate Euroopa avaliku hindamisaruande lisatud ravimi omaduste kokkuvõttest.
Kuidas Vidaza toimib?
Vidaza toimeaine asatsitidiin on antimetaboliitide klassi kuuluv ravim Asatsitidiin on tsütidiini analoog; see tähendab, et see on lisatud rakkude geneetilisse materjali (RNA ja DNA). Arvatakse, et see toimib, muutes raku geenide sisse- ja väljalülitamise viisi ning sekkudes ka uue RNA ja DNA tootmisse. Arvatakse, et need sekkumised parandavad luuüdis uute vererakkude küpsemise ja kasvu probleeme, mis põhjustavad müelodüsplastilisi sündroome ja tapavad leukeemia korral vähirakke.
Kuidas Vidazat uuriti?
Enne inimestega uurimist testiti Vidaza toimet esmalt katsemudelites.
Vidaza kohta tehti üksainus põhiuuring, milles osales 358 täiskasvanut, kellel oli keskmise kuni kõrge riskiga müelodüsplastiline sündroom, KML või AML ja kellel ei olnud tõenäoliselt võimalik luuüdi siirdamist läbi viia. Nende patsientide luuüdi sisaldas 10–29% ebanormaalseid rakke, mille valgete vereliblede arv ei olnud väga kõrge. Uuringus võrreldi Vidazat tavapäraste ravimitega (ravi valiti individuaalselt, lähtudes kohalikest tavadest ja patsiendi haigusest). Kõik patsiendid said ka "parimat toetavat ravi" (st patsienti abistavaid ravimeid või ravimeetodeid, näiteks antibiootikume, valuvaigisteid ja vereülekandeid); mõnda patsienti on ravitud ka teiste vähivastaste ravimitega, nagu tsütarabiin koos antratsükliiniga või ilma. Efektiivsuse põhinäitaja oli patsientide eluiga. Uuring kestis 44 kuud.
Milles seisneb uuringute põhjal Vidaza kasulikkus?
Vidaza on osutunud ellujäämise pikendamiseks tõhusamaks kui traditsioonilised ravimeetodid. Vidazaga ravitud patsiendid elasid keskmiselt 24,5 kuud, võrreldes tavapärase hooldusega patsientidega 15 kuud. Vidaza toime on kõigi kolme haiguse puhul sarnane.
Mis riskid Vidazaga kaasnevad?
Vidaza kõige sagedasemad kõrvaltoimed (esinenud üle 60% ravitud patsientidest) on verereaktsioonid, sealhulgas trombotsütopeenia (madal trombotsüütide arv), neutropeenia (madal neutrofiilide tase, teatud tüüpi valgeid vereliblesid) ja leukopeenia (madal trombotsüütide arv). valged verelibled), magu ja soolestikku mõjutavad kõrvaltoimed, sealhulgas iiveldus ja oksendamine, ning süstekoha reaktsioonid. Vidaza kohta teatatud kõrvalnähtude täieliku loetelu leiate pakendi infolehelt.
Vidaza't ei tohi kasutada patsiendid, kes võivad olla asatsitidiini või selle ravimi mis tahes muu koostisaine suhtes ülitundlikud (allergilised).
Miks Vidaza heaks kiideti?
Inimtervishoius kasutatavate ravimite komitee (CHMP) otsustas, et Vidaza kasulikkus on suurem kui sellega kaasnevad riskid täiskasvanud patsientide ravis, kes ei sobi hematopoeetiliste tüvirakkude siirdamiseks koos vaheastme 2 ja kõrge riskiga müelodüsplastiliste sündroomidega, MMC 10–29% ebanormaalsete blastidega müeloproliferatiivne häire või AML 20–30% blastide ja mitmerealise düsplaasiaga. Komitee soovitas anda Vidaza müügiloa.
Muu teave Vidaza kohta:
17. detsembril 2008 andis Euroopa Komisjon Celgene Europe Ltd -le Vidaza müügiloa, mis kehtib kogu Euroopa Liidus.
Vidaza harva kasutatavaks ravimiks nimetamise registreerimiseks siin (müelodüsplastilised sündroomid) e siin (LMA).
Vidaza EPARi täisversiooni leiate siit.
Selle kokkuvõtte viimane uuendus: 11-2008.
Sellel lehel avaldatud teave Vidaza - asatsitidiini kohta võib olla aegunud või puudulik. Selle teabe õigeks kasutamiseks vaadake vastutusest loobumise ja kasuliku teabe lehte.