Toimeained: erütropoetiin (alfaepoetiin)
EPREX 2000 RÜ / ml, 4000 RÜ / ml, 10 000 RÜ / ml ja 40 000 RÜ / ml süstelahus eeltäidetud süstaldes
Miks kasutatakse Eprexi? Milleks see mõeldud on?
Mis ravim on EPREX ja milleks seda kasutatakse
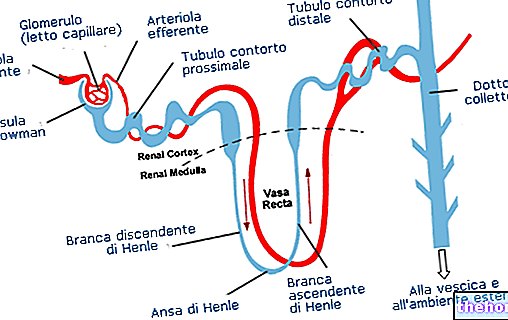
EPREX sisaldab toimeainena alfaepoetiini, valku, mis stimuleerib luuüdi tootma rohkem punaseid vereliblesid, rakke, mis kannavad hemoglobiini (hapnikku kandev aine). Alfaepoetiin on inimese erütropoetiini koopia ja toimib sellel viisil.
- EPREXi kasutatakse neerupuudulikkusest tingitud sümptomaatilise aneemia raviks.
- hemodialüüsi saavatel lastel
- täiskasvanutel, kes saavad hemodialüüsi ja peritoneaaldialüüsi
- raske aneemiaga täiskasvanutel, kes ei saa veel dialüüsi.
Kui teil on neerupuudulikkus ja teie neerud ei tooda piisavalt erütropoetiini (mis on vajalik punaste vereliblede tootmiseks), võib teie veres olla vähe punaseid vereliblesid. EPREX on ette nähtud, et stimuleerida luuüdi tootma rohkem punaseid vereliblesid.
- EPREXi kasutatakse aneemia raviks, mis võib tekkida soliidtuumorite, pahaloomulise lümfoomi või hulgimüeloomi (luuüdi vähk) keemiaravi ajal, kui teie arst arvab, et teil võib olla vajalik vereülekanne.
- EPREXi kasutatakse mõõduka aneemiaga patsientide raviks, kes kandideerivad oma verd enne operatsiooni ootama, nii et seda saab operatsiooni ajal või pärast seda üle kanda. Kuna EPREX stimuleerib punaste vereliblede tootmist, on võimalik nendelt inimestelt verd välja võtta suurem kogus verd.
- EPREXi kasutatakse mõõduka aneemiaga täiskasvanud patsientide raviks, kellele tehakse suur ortopeediline operatsioon (nt puusa- või põlveliigese asendus), et vähendada vereülekande vajadust.
Vastunäidustused Kui Eprexi ei tohi kasutada
Ärge kasutage EPREXi
- Kui te olete allergiline (ülitundlik) alfaepoetiini või EPREXi mõne koostisosa (loetletud pakendi sisu ja muu teave) suhtes;
- Kui teil on diagnoositud "puhas punaliblede aplaasia (luuüdi ei suuda toota piisavalt punaseid vereliblesid) pärast eelnevat ravi mis tahes ainega, mis stimuleerib punaste vereliblede tootmist (sh EPREX)." Vt lõik Võimalikud kõrvaltoimed.
- Kui teil on probleeme kontrollimatu kõrge vererõhuga
- Ergutada punaste vereliblede tootmist (et saaksite rohkem verd võtta), kui te ei saa operatsiooni ajal või pärast seda oma vereülekannet saada.
- Kui teile tehakse plaaniline suur ortopeediline operatsioon (nt puusa- või põlveliigese asendamine) ja
- on raske südamehaigus
- teil on tõsiseid probleeme veenide ja arteritega
- teil on hiljuti olnud südameatakk või insult
- ei saa võtta verd vedeldavaid ravimeid
EPREX ei pruugi teile sobida. Arutage seda oma arstiga. EPREXi kasutamise ajal võivad mõned inimesed vajada verehüüvete tekke riski vähendavaid ravimeid. Kui te ei saa antikoagulante võtta, ei tohi te EPREXi võtta.
Ettevaatusabinõud kasutamisel Mida on vaja teada enne Eprexi võtmist
Eriline ettevaatus on vajalik ravimiga EPREX
EPREX ja teised punaseid vereliblesid stimuleerivad ained võivad kõigil patsientidel suurendada verehüüvete tekke riski.See risk võib olla suurem, kui teil on muid verehüüvete tekke riskitegureid (näiteks kui teil on varem olnud verehüübe või olete ülekaaluline, teil on diabeet, teil on südamehaigus või olete pikka aega olnud operatsioon või haigus). Rääkige oma arstile nendest asjadest. Arst aitab teil otsustada, kas EPREX sobib teile.
On oluline, et te räägiksite oma arstile, kui mõni järgmistest teie kohta kehtib.
Võite endiselt kasutada EPREXi, kuid arutage seda kõigepealt oma arstiga.
- Kui teate, et teil on valu või teil on:
- Kõrge vererõhk;
- Krambid või krambid
- Maksahaigus;
- muudel põhjustel tekkiv aneemia;
- Porfüüria (harvaesinev verehaigus).
- Kui teil on vähk, peaksite teadma, et punaste vereliblede tootmist stimuleerivad ained (näiteks EPREX) võivad toimida kasvufaktorina ja teoreetiliselt mõjutada kasvaja progresseerumist. Sõltuvalt teie individuaalsest seisundist võib olla eelistatav vereülekanne. Arutage seda oma arstiga.
Pöörake erilist tähelepanu ainetele, mis stimuleerivad punaste vereliblede tootmist:
EPREX kuulub ainete rühma, mis stimuleerivad punaste vereliblede tootmist nagu inimese erütropoeetilised tegurid. Arst hoolitseb alati selle eest, et ta registreeriks täpselt kasutatava toote nime. Kui teile manustatakse ravi ajal ainet, mis kuulub samasse rühma, kuid erineb EPREXist, võtke enne kasutamist ühendust oma arsti või apteekriga.
Koostoimed Millised ravimid või toidud võivad muuta Eprexi toimet
Tavaliselt ei mõjuta EPREX teiste ravimite toimet, kuid rääkige alati oma arstile, kui te kasutate või olete hiljuti kasutanud mingeid muid ravimeid, kaasa arvatud retseptiravimeid.
Kui te võtate tsüklosporiini -nimelist ravimit (kasutatakse näiteks pärast neeru siirdamist), võib teie arst tellida vereanalüüse tsüklosporiini taseme kontrollimiseks EPREX -ravi ajal.
Raudpreparaadid ja muud aneemiavastased tegurid võivad suurendada EPREXi efektiivsust. Teie arst otsustab, kas te peaksite neid võtma.
Haiglaravi või tervisekontrolli korral teatage palun, et teid ravitakse EPREXiga. See võib mõjutada muid ravimeetodeid või testitulemusi.
Hoiatused Oluline on teada, et:
Rasedus ja imetamine
Oluline on rääkida oma arstile, kui mõni järgmistest tingimustest kehtib teie kohta. Võite endiselt kasutada EPREXi, kuid arutage seda kõigepealt oma arstiga.
- Kui olete rase või arvate end olevat rase.
- Kui te toidate last rinnaga.
Annus, manustamisviis ja aeg Kuidas Eprexi kasutada: Annustamine
Kasutage seda ravimit alati täpselt nii, nagu arst on teile rääkinud. Kui te pole milleski kindel, pidage nõu oma arstiga.
Arst on teie vereanalüüside põhjal otsustanud, et vajate EPREXi.
EPREXi võib süstida:
- Veeni või torusse veeni (intravenoosselt)
- Naha alla (subkutaanselt)
Arst otsustab, kuidas EPREXi manustada. Süste teeb tavaliselt arst, õde või tervishoiutöötaja; mõned inimesed võivad õppida iseseisvalt ravimit subkutaanselt manustama: vaadake juhiseid EPREXi ise süstimiseks.
- Eprexi ei tohi kasutada:
- pärast kõlblikkusaega, mis on märgitud sildil või välispakendil
- kui teate või arvate, et ravim võis kogemata külmuda või jah
- ja oli külmiku rike
EPREXi annus põhineb teie kehakaalul kilogrammides ja arst valib selle sõltuvalt aneemia põhjusest.
Arst kontrollib regulaarselt teie vererõhku EPREX -ravi ajal.
Neerupuudulikkusega patsiendid
- Teie hemoglobiini väärtus hoitakse vahemikus 10–12 g / dl, kuna kõrgem hemoglobiinisisaldus võib suurendada tromboosi ja surma riski.
- Tavaline EPREXi algannus täiskasvanutele või lastele on 50 rahvusvahelist ühikut (RÜ) kilogrammi (/ kg) kehakaalu kohta, manustatuna 3 korda nädalas.
- Peritoneaaldialüüsi saavatel patsientidel võib manustamist teha kaks korda nädalas.
- EPREXi manustatakse täiskasvanutele ja lastele intravenoosselt (veeni või tuubi kaudu veeni). Kui intravenoosne manustamisviis (veen või tuub veeni) pole saadaval, võib arst otsustada, kas süstida EPREXi naha alla (subkutaanselt). Sealhulgas dialüüsipatsiendid ja patsiendid, kes ei saa veel dialüüsi.
- Teie arst teeb teile regulaarselt vereanalüüse, et kontrollida, kas teie aneemia reageerib, ja võib kohandada annust, tavaliselt mitte sagedamini kui üks kord iga 4 nädala järel.
- Kui aneemia on korrigeeritud, jätkab arst regulaarselt teie vereanalüüside kontrollimist. EPREXi annust ja manustamissagedust võib ravivastuse säilitamiseks veelgi kohandada.
- Kui teid ravitakse EPREXiga pikemate annustamisintervallidega (rohkem kui üks kord nädalas), ei pruugi teil olla võimalik oma hemoglobiinisisaldust piisavalt säilitada ja peate võib -olla suurendama oma EPREXi annust või manustamissagedust.
- Ravi efektiivsemaks muutmiseks võivad rauapreparaadid olla teile kasulikud enne EPREX -ravi ja ravi ajal.
- Kui te alustate EPREX -ravi alustamist hemodialüüsi, võib osutuda vajalikuks dialüüsirežiimi kohandamine. Arst otsustab.
Täiskasvanud patsiendid, kes saavad keemiaravi
- Arst võib alustada ravi EPREXiga, kui teie hemoglobiinisisaldus on 10 g / dl või vähem.
- Teie hemoglobiinisisaldus jääb vahemikku 10–12 g / dl, kuna kõrgem hemoglobiinisisaldus võib suurendada tromboosi ja surma riski.
- Algannus on 150 RÜ kehakaalu kilogrammi kohta 3 korda nädalas või 450 RÜ kehakaalu kilogrammi kohta üks kord nädalas.
- EPREXi manustatakse subkutaanse süstena.
- Teie arst teeb teile regulaarselt vereanalüüse ja võib kohandada annust sõltuvalt teie ravivastusest EPREXiga.
- Ravi efektiivsemaks muutmiseks võib rauapreparaat olla teile kasulik enne EPREX -ravi ja ravi ajal.
- Tavaliselt jätkatakse EPREX -ravi 1 kuu jooksul pärast keemiaravi lõppu.
Täiskasvanud patsiendid, kes annavad oma verd
- Tavaline annus on 600 RÜ kehakaalu kilogrammi kohta 2 korda nädalas.
- EPREX manustatakse veeni kohe pärast vere sadestamist 3 nädalat enne operatsiooni.
- Ravi efektiivsemaks muutmiseks võib rauapreparaat olla teile kasulik enne EPREX -ravi ja ravi ajal.
Täiskasvanud patsiendid, kes kandideerivad suurele ortopeedilisele kirurgiale
- Soovitatav annus on 600 RÜ kehakaalu kilogrammi kohta üks kord nädalas.
- EPREXi manustatakse subkutaanse süstena iga nädal 3 nädala jooksul enne operatsiooni ja operatsiooni päeval.
- Kui on vaja lühendada operatsioonieelset aega, määratakse teile ööpäevane annus 300 RÜ / kg operatsioonile eelneva 10 päeva jooksul, operatsiooni päeval ja 4 päeva jooksul pärast operatsiooni.
- Kui vereanalüüsid enne operatsiooni näitavad liiga kõrgeid hemoglobiinisisaldusi, lõpetatakse ravi.
- Ravi efektiivsemaks muutmiseks võivad rauapreparaadid olla teile kasulikud enne EPREX -ravi ja ravi ajal.
Juhised EPREXi ise süstimiseks
- Ravi alguses manustab EPREXi tavaliselt arst või õde. Seejärel võib arst soovitada teil (või teie hooldajal) õppida (subkutaanselt) süstimist.
- Ärge proovige ennast süstida, kui arst või õde pole teile seda öelnud.
- Järgige alati oma arsti või õe juhiseid.
- Kasutage EPREXi ainult siis, kui see on õigesti salvestatud - vt lõiku Kuidas EPREXi säilitada
- Enne kasutamist eemaldage Eprexi süstal külmkapist ja laske sellel soojeneda toatemperatuurini. Tavaliselt kulub 15-30 minutit.
Tõmmake igast eeltäidetud süstlast välja üks EPREXi annus Kui EPREXi manustatakse naha alla (subkutaanselt), ei ületa tavaliselt ühe süsti maht 1 milliliitrit (1 ml).
EPREXi tuleb manustada üksi ja seda ei tohi segada teiste süstevedelikega.
Ärge raputage EPREXi eeltäidetud süstlaid. Pikaajaline tugev raputamine võib toodet kahjustada. Ärge kasutage toodet, kui seda on tugevalt loksutatud.
Kuidas süstida endale eeltäidetud süstlaid kasutades
Eeltäidetud süstlad on varustatud nõelakaitseseadmega PROTECS ™, et vältida nõela kinnijäämist pärast kasutamist. See on pakendil märgitud.
- Eemaldage süstel enne kasutamist külmkapist. Vedelik peab jõudma toatemperatuurini. Ärge eemaldage nõelakatet, oodates, kuni see jõuab toatemperatuurini.
- Kontrollige eeltäidetud süstalt, et veenduda, et see on õige annus, et see ei ole aegunud, et see pole kahjustatud ja kas vedelik on selge ega külmunud.
- Valige süstekoht. Kõige sobivamad süstekohad on reie ülaosa ja kõht, välja arvatud naba ümbrus. Vahetage süstekohta iga kord.
- Käte pesemiseks. Süstekoha desinfitseerimiseks kasutage antiseptilist salvrätikut.
- Hoidke eeltäidetud süstalt süstla silindrist, kaetud nõel ülespoole.
- Ärge hoidke kinni kolvi peast, kolbist, nõela kaitsetiibast ega nõelakattest.
- Ärge mingil juhul tõmmake kolbi tagasi
- Ärge eemaldage süstli nõelakatet enne, kui olete valmis EPREXi manustama
- Eemaldage süstlanõelast kaitsekork, hoides seda kehast kinni ja tõmmates korki seda keeramata. Ärge vajutage kolbi, puudutage nõela ega raputage süstalt. - Ärge puudutage turvaseadme aktiveerimisklambreid, et vältida nõela kaitseklapiga enneaegset katmist
- Tõstke nahk pöidla ja nimetissõrme vahele seda liigselt pigistamata.
- Lükake nõel lõpuni sisse. Teie arst või õde on teile seda näidanud.
- Lükake kolbi pöidlaga, kuni on süstitud kogu õigele annusele vastav vedeliku kogus. Vajutage aeglaselt ja ühtlaselt, hoides nahka üleval. PROTECS ™ nõela ohutusseade ei aktiveeru enne süsti manustamist. Annus täielikult. Kui nõelakaitse PROTECS ™ on aktiveeritud, võite kuulda klõpsatust.
- Kui kolb on oma löögi lõppu jõudnud, tõmmake nõel välja ja vabastage nahk.
- Eemaldage pöial aeglaselt kolbilt, et nõel oleks ohutusseadisega täielikult kaetud.
- Süstimise lõpus võib süstekohas olla väike kogus verd. See on normaalne. Süstekoha saate desinfitseerida, vajutades mõneks sekundiks antiseptilist padja.
- Visake kasutatud süstlad ohutusse konteinerisse - vt lõiku Eprexi säilitamine
Üleannustamine Mida teha, kui olete võtnud liiga palju Eprexi
Kui te kasutate EPREXi rohkem kui ette nähtud
Rääkige otsekohe oma arstile või meditsiiniõele, kui arvate, et olete EPREXi liiga palju kasutanud. Üleannustamise kõrvaltoimed on ebatõenäolised.
Kui te unustate EPREXi süstida
Tehke järgmine süst niipea, kui see teile meenub. Kui järgmine süst jääb päeva jooksul, jätke vahelejäänud annus vahele ja jätkake tavapärase skeemiga. Ärge kahekordistage süstimist.
Kui olete C -hepatiidiga patsient ja saate interferooni ja ribaviriini
Peaksite pöörduma oma arsti poole, sest alfaepoetiini kombinatsioon interferooni ja ribaviriiniga on harvadel juhtudel põhjustanud toime kadumise ja raske aneemia vormi, mida nimetatakse puhtaks punaste vereliblede aplaasiaks (PRCA), tekkeks. EPREX ei ole heaks kiidetud C -hepatiidiga seotud aneemia ravi.
Kui teil on lisaküsimusi selle ravimi kasutamise kohta, pidage nõu oma arsti, meditsiiniõe või apteekriga.
Kõrvaltoimed Millised on Eprexi kõrvaltoimed
Nagu kõik ravimid, võib ka EPREX põhjustada kõrvaltoimeid, kuigi kõigil neid ei teki. Kui mõni allpool loetletud kõrvaltoimetest ilmneb, rääkige sellest kohe oma arstile või meditsiiniõele.
Väga sageli esinevad kõrvaltoimed
Neid esineb rohkem kui ühel patsiendil 10 -st, kes kasutavad EPREXi
- Kõhulahtisus
- Iiveldus maos
- Ta tõmbus tagasi
- Palavik
- Neeruhaigusega patsientidel, kes ei saa veel dialüüsi, on teatatud hingamisteede ummistustest, nagu kinnine nina ja kurguvalu.
Sageli esinevad kõrvaltoimed
Need mõjutavad kuni 1 patsienti 10 -st, kes kasutavad EPREXi
- Vererõhu väärtuste tõstmine. Peavalu (eriti kui see on äkiline, äge ja migreenitaoline) või segasus või krambid. Need võivad olla märgid vererõhu järsust tõusust, mis nõuab kohest ravi. Vererõhu tõus võib vajada ravi. Ravimitega (või kõrge vererõhu korral juba kasutatavate ravimite annuse kohandamine).
- Verehüübed (sealhulgas süvaveenide tromboos ja emboolia), mis võivad vajada kiiret ravi. Sümptomiteks võivad olla valu rinnus, vilistav hingamine, alajäsemete valulik turse ja punetus, tavaliselt jalgades.
- köha.
- Nahaärritus, mis võib olla põhjustatud allergilisest reaktsioonist.
- Luu- või lihasvalu.
- Gripilaadne sündroom, nagu peavalu, liigesvalu, nõrkus, külmavärinad, väsimus ja pearinglus. Need reaktsioonid on sagedasemad ravi alguses.Kui teil tekivad need sümptomid veeni süstimise ajal, aitab aeglasem manustamine neid tulevikus vältida.
- Süstekoha punetus, põletustunne ja valu.
- Pahkluude, jalgade või sõrmede turse.
Aeg -ajalt esinevad kõrvaltoimed
Need esinevad kuni ühel patsiendil 100 -st, kes kasutavad EPREXi
- Kõrge kaaliumisisaldus veres, mis võib põhjustada südame rütmihäireid (see on dialüüsi saavatel patsientidel väga levinud kõrvaltoime).
- Krambid
- Ninakinnisus või hingamisteed
Väga harva esinevad kõrvaltoimed
Need esinevad kuni ühel patsiendil 10 000 -st, kes kasutavad EPREXi
- Puhta punaliblede aplaasia (PRCA) sümptomid. PRCA tähendab võimetust toota piisavalt punaseid vereliblesid luuüdis. PRCA võib põhjustada tõsist ja äkilist aneemiat, mille sümptomiteks on:
- ebatavaline väsimus,
- pearingluse tunne,
- õhupuudus.
PRCA -d on leitud väga harva, eriti neeruhaigusega patsientidel pärast kuid või aastaid kestnud ravi EPREX -i ja teiste punaste vereliblede tootmist stimuleerivate ainetega. Eriti ravi alguses võib esineda tavaliselt verehüüvete moodustamisega seotud väikeste vererakkude (nn trombotsüütide), mida nimetatakse trombotsüütideks, taseme tõus. Arst kontrollib seda.
Kui te saate hemodialüüsi:
- Dialüüsi šundis võivad tekkida verehüübed (tromboos). See võib juhtuda kergemini, kui teil on madal vererõhk (hüpotensioon) või kui teil on probleeme fistuliga.
- Verehüübed võivad tekkida ka hemodialüüsi süsteemis.Arst võib otsustada suurendada dialüüsi ajal hepariini annust.
Rääkige otsekohe oma arstile või meditsiiniõele, kui teil tekib mõni nendest mõjudest või kui te märkate mõnda muud toimet EPREXi võtmise ajal.
Kui ükskõik milline kõrvaltoimetest muutub tõsiseks või kui te märkate mõnda kõrvaltoimet, mida selles infolehes ei ole nimetatud, palun rääkige sellest oma arstile, meditsiiniõele või apteekrile.
Neile, kes tegelevad spordiga: ravimi kasutamine ilma terapeutilise vajaduseta kujutab endast dopingut ja võib igal juhul määrata positiivse dopinguvastase testi.
Aegumine ja säilitamine
Hoida laste eest varjatud ja kättesaamatus kohas.
Ärge kasutage seda ravimit pärast kõlblikkusaega, mis on märgitud karbil ja sildil pärast tähti EXP. Kõlblikkusaeg on märgitud kuu viimane päev.
EPREXi tuleb hoida külmkapis (2 ° C ... 8 ° C).
EPREXi saab külmkapist välja võtta ja hoida toatemperatuuril (mitte üle 25 ° C) kuni 3 päeva. Kui süstel on külmkapist välja võetud ja see on saavutanud toatemperatuuri (mitte üle 25 ° C), tuleb see 3 päeva jooksul ära kasutada või ära visata.
Seda ei tohi külmutada ega loksutada
Hoida valguse eest kaitsmiseks originaalpakendis.
Ärge kasutage seda ravimit, kui tihend on katki või kui lahus on värvunud või on täheldatud hõljuvaid osakesi. Kui neid tingimusi täheldatakse, hävitage ravim
Ravimeid ei tohi ära visata kanalisatsiooni kaudu ega koos majapidamisprügiga. Küsige oma apteekrilt, kuidas visata ära ravimeid, mida te enam ei kasuta. See aitab kaitsta keskkonda.
Pakendi sisu ja muu teave
Mida Eprex sisaldab
Toimeaine on: alfaepoetiin (koguse kohta vt allolevat tabelit).
Abiained on: polüsorbaat 80, naatriumkloriid, ühealuseline naatriumfosfaatdihüdraat, kahealuseline naatriumfosfaatdihüdraat, glütsiin ja süstevesi. See ravim sisaldab vähem kui 1 mmol naatriumi (23 mg) annuse kohta, seega on see sisuliselt naatriumivaba.
Kuidas EPREX välja näeb ja pakendi sisu
EPREX on süstelahus süstlis. Eeltäidetud süstlad on varustatud PROTECS ™ nõela turvaseadmega (vt tabelit allpool) EPREX on selge ja värvitu lahus.
Kõik pakendi suurused ei pruugi olla müügil
Allika pakendi infoleht: AIFA (Itaalia ravimiamet). Sisu avaldati jaanuaris 2016. Esitatud teave ei pruugi olla ajakohane.
Kõige ajakohasemale versioonile juurdepääsu saamiseks on soovitatav külastada AIFA (Itaalia ravimiamet) veebisaiti. Vastutusest loobumine ja kasulik teave.
01.0 RAVIMPREPARAADI NIMETUS
EPREX 10000 RÜ / ml süstelahus eeltäidetud süstlas
02.0 KVALITATIIVNE JA KVANTITATIIVNE KOOSTIS
Alfaepoetiin 10 000 RÜ / ml (84,0 μg / ml), toodetud rekombinantse DNA tehnoloogia abil hiina hamstri munasarja (CHO) rakkudes.
Üks 0,3 ml süstel sisaldab 3000 RÜ (25,2 mikrogrammi) alfaepoetiini
Üks 0,4 ml süstel sisaldab 4000 RÜ (33,6 mcg) alfaepoetiini
Üks 0,5 ml eeltäidetud süstal sisaldab 5000 RÜ (42,0 mcg) alfaepoetiini
Üks 0,6 ml süstel sisaldab 6000 RÜ (50,4 mikrogrammi) alfaepoetiini
Üks 0,8 ml süstel sisaldab 8000 RÜ (67,2 mikrogrammi) alfaepoetiini
Üks 1,0 ml süstel sisaldab 10 000 RÜ (84,0 mikrogrammi) alfaepoetiini
See ravim sisaldab vähem kui 1 mmol (23 mg) naatriumi annuse kohta, st see on põhimõtteliselt „naatriumivaba“.
Abiainete täielik loetelu vt lõik 6.1
03.0 RAVIMVORM
Süstelahus eeltäidetud süstaldes
Selge värvitu lahus
04.0 KLIINILINE TEAVE
04.1 Näidustused
EPREX on näidustatud kroonilise neerupuudulikkusega seotud sümptomaatilise aneemia raviks:
• hemodialüüsi saavatel täiskasvanud ja lastel vanuses 1–18 aastat ja peritoneaaldialüüsi saavatel täiskasvanud patsientidel.
• täiskasvanud neerupuudulikkusega patsientidel, kes ei saa veel dialüüsi, raske neerupuudulikkusega aneemia raviks, millega kaasnevad kliinilised sümptomid patsientidel.
EPREX on näidustatud aneemia raviks ja selle vähendamiseks täiskasvanud patsientidel, kes saavad keemiaravi soliidtuumorite, pahaloomulise lümfoomi või hulgimüeloomi korral ning kellel on vereülekande oht, nagu näitab patsiendi üldine seisund (kardiovaskulaarne seisund, olemasolev aneemia keemiaravi alguses). vereülekande vajadusest.
EPREX on näidustatud täiskasvanud patsientidele, kes on osa autoloogse vere hulga suurendamise eelprogrammist. Ravi on näidustatud ainult mõõduka aneemiaga patsientidele (hemoglobiini kontsentratsioon vahemikus Hb 10–13 g / dl [6, 2–8,1] mmol / l], rauapuudus puudub), kui vere säilitamise protseduurid ei ole kättesaadavad või on ebapiisavad suure plaanilise operatsiooni korral, mis nõuab suurel hulgal verd (4 või enam ühikut naise kohta või 5 või enam ühikut meestel).
EPREX on näidustatud täiskasvanud patsientidele, kellel ei ole rauapuudust enne suurt plaanilist ortopeedilist operatsiooni, kellel arvatakse olevat suur vereülekande tüsistuste oht, et vähendada kokkupuudet allogeensete vereülekannetega. Kasutamine peaks piirduma mõõduka aneemiaga patsientidega (hemoglobiini kontsentratsioon) vahemikus Hb10-13 g / dl), kellele ei ole saadaval autoloogset vereloovutusprogrammi ja kelle puhul on oodata mõõdukat verekaotust (900 kuni 1800 ml).
04.2 Annustamine ja manustamisviis
Annustamine
Enne ravi alustamist alfaepoetiiniga ja annuse suurendamise otsustamisel kõik muud aneemia põhjused (raua, folaadi või B12 -vitamiini puudus, alumiiniumimürgitus, infektsioonid või põletik, verekaotus, hemolüüs ja mis tahes päritoluga luuüdi fibroos). Optimaalse ravivastuse tagamiseks alfaepoetiinile tuleb tagada piisavad rauavarud ja vajadusel manustada rauapreparaate (vt lõik 4.4).
Sümptomaatilise aneemia ravi kroonilise neerupuudulikkusega (CRI) täiskasvanud patsientidel
Aneemia sümptomid ja tagajärjed võivad varieeruda sõltuvalt soost, vanusest ja käimasolevatest kaasuvatest haigustest; arsti hinnang patsiendi individuaalsele seisundile on vajalik.
Soovitud hemoglobiini kontsentratsioon on vahemikus 10 g / dl kuni 12 g / dl (6,2 kuni 7,5 mmol / l). EPREXi tuleb manustada nii, et hemoglobiini kontsentratsioon ei ületaks 12 g / dl (7,5 mmol / l). Vältida tuleks hemoglobiini tõusu üle 2 g / dl (1,25 mmol / l) nelja nädala jooksul. Kui see juhtub, tuleb annust vastavalt kohandada.
Patsiendisisese varieeruvuse tõttu võib patsiendil aeg-ajalt täheldada hemoglobiini väärtusi, mis on soovitud hemoglobiini kontsentratsioonist kõrgemad ja madalamad. Seda varieeruvust tuleb reguleerida annust kohandades, järgides hemoglobiini kontsentratsiooni vahemikku 10 g / dl (6,2 mmol / l) kuni 12 g / dl (7,5 mmol / l).
Vältida tuleb hemoglobiini taset, mis on pidevalt üle 12 g / dl (7,5 mmol). Kui hemoglobiin suureneb rohkem kui 2 g / dl (1,25 mmol / l) kuus või kui hemoglobiini tase ületab pidevalt 12 g / dl (7,5 mmol), vähendage EPREXi annust 25%. Kui hemoglobiin ületab 13 g / dl ( 8,1 mmol / l), katkestage ravi, kuni see taastub tasemele 12 g / dl (7,5 mmol / l), ja jätkake seejärel EPREXi manustamist 25% madalamate annustega kui eelmised.
Patsiente tuleb hoolikalt jälgida, et tagada aneemia ja sellega seotud sümptomite piisava kontrolli tagamiseks EPREXi väikseima lubatud efektiivdoosi kasutamine, hoides hemoglobiini kontsentratsiooni 12 g / dl (7,5 mmol / l) või alla selle.
Kroonilise neerupuudulikkusega patsientidel tuleb ESA annuse suurendamisel olla ettevaatlik.Patsientidel, kellel on ESA -dele halb hemoglobiinivastus, tuleb otsida halva ravivastuse alternatiivset põhjust (vt lõigud 4.4 ja 5.1).
EPREX -ravi on jagatud kahte faasi - korrektsioonifaas ja hooldusfaas.
Täiskasvanud patsiendid, kes saavad hemodialüüsi
Hemodialüüsi saavatel patsientidel, kellel on venoosne juurdepääs kergesti kättesaadav, on eelistatav kasutada intravenoosset manustamisviisi.
Parandusetapp :
Algannus on 50 RÜ / kg kehakaalu kohta 3 korda nädalas.
Vajadusel suurendage või vähendage annust 25 RÜ / kg (3 korda nädalas) kuni soovitud hemoglobiini kontsentratsioonini vahemikus 10 g / dl kuni 12 g / dl (6,2 kuni 7,5 mmol / l) (seda tuleb teha järk -järgult vähemalt nelja nädala intervallidega).
- Hooldusetapp :
Soovitatav nädalane koguannus on 75 RÜ / kg kuni 300 RÜ / kg.
Tuleb kohandada annust, et hoida hemoglobiini väärtused soovitud hemoglobiini kontsentratsioonides vahemikus 10 g / dl kuni 12 g / dl (6,2 kuni 7,5 mmol / l).
Patsiendid, kellel on väga madal esialgne hemoglobiinitase (8 g / dl või> 5 mmol / l).
Neerupuudulikkusega täiskasvanud patsiendid, kes ei saa veel dialüüsi
Patsientidele, kellel veenide juurdepääs ei ole kergesti kättesaadav, võib EPREXi manustada subkutaanselt.
Parandusetapp
Algannus on 50 RÜ / kg kehakaalu kohta 3 korda nädalas, millele järgneb vajadusel annuse suurendamine 25 RÜ / kg (3 korda nädalas), kuni saavutatakse soovitud hemoglobiini kontsentratsioon (seda tuleb teha järk -järgult. vähemalt nelja nädala intervallidega).
Hooldusetapp
Säilitusfaasis võib EPREXi manustada kas 3 korda nädalas ja subkutaanse manustamise korral üks kord nädalas või kord kahe nädala jooksul.
Annust ja manustamisintervalle tuleb õigesti reguleerida, et hemoglobiinisisaldus püsiks soovitud tasemel: Hb vahemikus 10–12 g / dl (6,2–7,5 mmol / l). Annustamisintervalli pikendamine võib nõuda annuse suurendamist.
Maksimaalne annus ei tohi ületada 150 RÜ / kg 3 korda nädalas, 240 RÜ / kg (kuni 20 000 RÜ) üks kord nädalas või 480 RÜ / kg (kuni 40 000 RÜ) üks kord iga 2 nädala järel.
Täiskasvanud patsiendid, kes saavad peritoneaaldialüüsi
Patsientidele, kellel veenide juurdepääs ei ole kergesti kättesaadav, võib EPREXi manustada subkutaanselt.
Parandusetapp
Algannus on 50 RÜ / kg kaks korda nädalas.
Hooldusetapp
Soovitatav säilitusannus on 25 RÜ / kg kuni 50 RÜ / kg kaks korda nädalas, jagatuna kaheks võrdseks manustamiseks.
Hemoglobiini väärtuste säilitamiseks soovitud tasemel tuleb teha asjakohane annuse kohandamine: hemoglobiin vahemikus 10 g / dl kuni 12 g / dl (6,2-7,5 mmol / l).
Keemiaravist põhjustatud aneemiaga täiskasvanud patsientide ravi
Aneemia sümptomid ja tagajärjed võivad varieeruda sõltuvalt vanusest, soost ja haiguse üldisest olukorrast; arsti hinnang patsiendi individuaalsele seisundile on vajalik.
EPREXi tuleb manustada aneemiaga patsientidele, nt. hemoglobiini kontsentratsioon ≤10 g / dl (6,2 mmol / l).
Algannus on 150 RÜ / kg, manustatuna subkutaanselt 3 korda nädalas.
Alternatiivina võib EPREXi manustada subkutaanselt algannusega 450 RÜ / kg üks kord nädalas.
Hemoglobiini väärtuste säilitamiseks soovitud tasemel tuleb teha asjakohane annuse kohandamine: hemoglobiin vahemikus 10 g / dl kuni 12 g / dl (6,2-7,5 mmol / l).
Patsiendisisese varieeruvuse tõttu võib patsiendil aeg-ajalt täheldada hemoglobiini väärtusi, mis on soovitud hemoglobiini kontsentratsioonist kõrgemad ja madalamad. Seda varieeruvust tuleb reguleerida annust kohandades, järgides soovitud hemoglobiini kontsentratsiooni vahemikku 10 g / dl (6,2 mmol / l) kuni 12 g / dl (7,5 mmol / l).
Vältida tuleb hemoglobiini kontsentratsiooni püsivalt üle 12 g / dl (7,5 mmol). Allpool on toodud juhised annuse õigeks kohandamiseks, kui hemoglobiini kontsentratsioon ületab 12 g / dl (7,5 mmol).
Kui pärast 4 -nädalast ravi on hemoglobiini kontsentratsioon tõusnud vähemalt 1 g / dl (0,62 mmol / l) või retikulotsüütide arv ≥ 40 000 rakku / μl võrreldes algväärtusega, tuleb annus hoida 150 RÜ / kg 3 korda nädalas või 450 RÜ / kg üks kord nädalas.
Kui hemoglobiini kontsentratsiooni tõus on
Kui hemoglobiini kontsentratsiooni tõus oli
Annuse kohandamine hemoglobiini kontsentratsiooni hoidmiseks vahemikus 10 g / dl - 12 g / dl
Kui hemoglobiini kontsentratsioon tõuseb rohkem kui 2 g / dl (1,25 mmol / l) kuus või kui hemoglobiinisisaldus ületab 12 g / dl (7,5 mmol / l), vähendage EPREXi annust umbes 25-50%.
Kui hemoglobiini kontsentratsioon ületab 13 g / dl (8,1 mmol / l), katkestage ravi, kuni kontsentratsioon langeb alla 12 g / dl (7,5 mmol / l), ja jätkake seejärel ravi EPREXiga, mis on 25% väiksem kui eelmine annus.
Soovitatav annus on kirjeldatud järgmisel skeemil:
Patsiente tuleb hoolikalt jälgida, et tagada aneemia sümptomite piisava kontrolli tagamiseks väikseima heakskiidetud erütropoeesi stimuleerivate ainete (ESA) annuse kasutamine.
EPREX -ravi tuleb jätkata ühe kuu jooksul pärast keemiaravi lõppu.
Täiskasvanud patsientide ravi, kes kandideerivad operatsioonile, mis on osa autoloogse vereloovutusprogrammist
Kerge aneemiaga patsiente (hematokrit vahemikus 33–39%), kes vajavad eelnevalt 4 või enama vereühiku sadestamist, tuleb operatsioonieelse 3 nädala jooksul ravida intravenoosselt 600 RÜ / kg EPREXiga kaks korda nädalas.
EPREX tuleb manustada pärast vere loovutamise protseduuri lõppu.
Täiskasvanud patsientide ravi, kes kandideerivad suureks plaaniliseks ortopeediliseks operatsiooniks
Soovitatav annus on 600 RÜ / kg EPREXi subkutaanselt, üks kord nädalas kolme nädala jooksul enne operatsiooni (-21 päeva, -14 päeva ja -7 päeva) ning operatsiooni päeval.
Kui on meditsiiniline vajadus lühendada operatsioonieelset ooteaega alla kolme nädala, tuleb EPREXi annus 300 RÜ / kg manustada subkutaanselt iga päev 10 päeva järjest. Enne operatsiooni, operatsioonipäeval ja vahetult sellele järgnenud 4 päeva.
Kui hemoglobiinisisaldus operatsioonieelsel perioodil jõuab 15 g / dl või rohkem, tuleb EPREXi manustamine lõpetada ja edasisi annuseid manustada.
Lapsed
Sümptomaatilise aneemia ravi kroonilise neerupuudulikkusega patsientidel, kes saavad hemodialüüsi
Aneemia sümptomid ja tagajärjed võivad varieeruda sõltuvalt vanusest, soost ja käimasolevatest kaasuvatest haigustest; arsti hinnang patsiendi individuaalsele seisundile on vajalik.
Pediaatrilistel patsientidel on soovitud hemoglobiini kontsentratsioon vahemikus 9,5 g / dl kuni 11 g / dl (5,9 kuni 6,8 mmol / l). EPREXi tuleb manustada nii, et hemoglobiini kontsentratsioon ei ületaks 11 g / dl (6,8 mmol / l). Vältida tuleks hemoglobiini tõusu üle 2 g / dl (1,25 mmol / l) nelja nädala jooksul. Kui see juhtub, tuleb annust vastavalt kohandada.
Patsiente tuleb hoolikalt jälgida, et tagada aneemia ja sellega seotud sümptomite piisava kontrolli tagamiseks EPREXi väikseima lubatud annuse kasutamine.
EPREX -ravi on jagatud kahte faasi: korrektsioonifaas ja hooldusfaas.
Hemodialüüsi saavatel pediaatrilistel patsientidel, kellele intravenoosne juurdepääs on juba saadaval, on eelistatav intravenoosne manustamine.
Parandusetapp:
Algannus on 50 RÜ / kg kehakaalu kohta intravenoosselt 3 korda nädalas.
Vajadusel suurendage või vähendage annust 25 RÜ / kg (3 korda nädalas), kuni soovitud hemoglobiini kontsentratsioon on vahemikus 9,5 g / dl kuni 11 g / dl (5,9 kuni 6, 8 mmol / l) (see peaks juhtuma) järk -järgult vähemalt nelja nädala intervalliga).
Hooldusetapp :
Tuleb kohandada annust, et hoida hemoglobiini väärtused soovitud hemoglobiinisisalduse piires vahemikus 9,5 g / dl kuni 11 g / dl (5,9 kuni 6,8 mmol / l).
Üldiselt vajavad alla 30 kg kaaluvad lapsed suuremaid säilitusannuseid kui üle 30 kg kaaluvad lapsed ja täiskasvanud.
Väga madala esialgse hemoglobiinisisaldusega lapsed (6,8 g / dl või> 4,25 mmol / l).
Keemiaravist põhjustatud aneemiaga laste ravi.
EPREXi ohutus ja efektiivsus keemiaravi saavatel lastel ei ole tõestatud.
Laste kirurgiliste patsientide ravi, kes osalevad autoloogse eeltootmise programmis
EPREXi ohutus ja efektiivsus lastel ei ole tõestatud.
Andmed puuduvad.
Lastepatsientide ravi, kes ootavad suurt plaanilist ortopeedilist operatsiooni
EPREXi ohutus ja efektiivsus lastel ei ole tõestatud.
Andmed puuduvad.
Manustamisviis
Olge ettevaatlik enne ravimi käsitsemist või manustamist.
Enne kasutamist jätke EPREX süstal puhkama, kuni see saavutab toatemperatuuri. Tavaliselt kulub selleks 15 kuni 30 minutit.
Sümptomaatilise aneemia ravi kroonilise neerupuudulikkusega täiskasvanud patsientidel
Kroonilise neerupuudulikkusega patsientidel, kellel on tavaliselt intravenoosne juurdepääs (hemodialüüsi saavatel patsientidel), on eelistatav EPREXi intravenoosne manustamine.
Kui intravenoosne juurdepääs ei ole hõlpsasti kättesaadav (patsiendid, kes ei ole veel dialüüsil ja peritoneaaldialüüsil), võib EPREXi manustada subkutaanselt.
Keemiaravist põhjustatud aneemiaga täiskasvanud patsientide ravi.
EPREXi tuleb manustada subkutaanselt.
Täiskasvanud kirurgiliste patsientide ravi, kes osalevad autoloogses vereloovutusprogrammis
EPREX tuleb manustada intravenoosselt.
Täiskasvanud patsientide ravi plaanilise ortopeedilise operatsiooni jaoks
EPREXi tuleb manustada subkutaanselt.
Sümptomaatilise aneemia ravi kroonilise neerupuudulikkusega lastel, kes saavad hemodialüüsi
Kroonilise neerupuudulikkusega lastel, kellel intravenoosne juurdepääs on juba saadaval (hemodialüüsi saavad patsiendid), on eelistatav EPREXi intravenoosne manustamine.
Intravenoosne manustamine
Sõltuvalt koguannusest peab manustamine kestma vähemalt 1-5 minutit.
Hemodialüüsi saavatel patsientidel võib boolussüsti teha dialüüsi ajal piisava venoosse juurdepääsu kaudu dialüüsitorusse. Teise võimalusena võib süsti teha dialüüsi lõpus, fistuli kaudu, millele järgneb 10 ml manustamine füsioloogilist lahust, et loputada juurdepääsuteid ja tagada toote rahuldav sisenemine vereringesse.
Patsientidel, kellel on esinenud gripilaadseid reaktsioone, on eelistatav aeglasem manustamine (vt lõik 4.8).
Ärge manustage EPREXi intravenoosse infusiooni teel ega teiste ravimite lahuses.
Subkutaanne manustamine
Üldjuhul ei tohi ületada maksimaalset mahtu 1 ml igas süstekohas. Suuremate koguste korral tuleb valida rohkem kui üks süstekoht.
Süstid tuleb teha jäsemetesse või kõhu eesseina.
Kui arst usub, et patsient või hooldaja suudab EPREXi subkutaanselt ohutult ja nõuetekohaselt manustada, tuleb esitada juhised õige annuse ja manustamise kohta.
Nagu teistegi süstitavate toodete puhul, kontrollige, et lahuses ei oleks osakesi ega värvimuutusi.
04.3 Vastunäidustused
Ülitundlikkus toimeaine või ravimi ükskõik millise abiaine suhtes.
Patsiente, kellel tekib pärast ravi mis tahes erütropoetiiniga puhas punaste vereliblede aplaasia (PRCA), ei tohi ravida EPREXi ega teiste erütropoetiinidega (vt lõik 4.4).
Kontrollimatu hüpertensioon.
EPREX-iga ravitavatel patsientidel tuleb meeles pidada kõiki vastunäidustusi, mis on seotud autoloogse vere eellasustamise programmiga.
EPREXi kasutamine on vastunäidustatud tõsiste vaskulaarsete häirete esinemisel pärgarteri, perifeersete arterite, unearteri või aju tasemel patsientidel, kes on kandideerinud suurele plaanilisele ortopeedilisele kirurgiale ja ei kuulu autoloogse vereloome programmi. Kasutamine on samuti vastunäidustatud. patsientidel, kellel on hiljuti esinenud müokardiinfarkti või muid tserebrovaskulaarseid tüsistusi.
Patsiendid, kes kandideerivad operatsioonile ja kes mingil põhjusel ei saa adekvaatset tromboosivastast profülaktikat.
04.4 Erihoiatused ja asjakohased ettevaatusabinõud kasutamisel
Kindral
Kõigil alfaepoetiini saavatel patsientidel tuleb vererõhku hoolikalt jälgida ja vajadusel kontrollida. Alfaepoetiini tuleb ettevaatusega kasutada ravimata, ebapiisavalt ravitud või raskesti kontrollitava hüpertensiooni korral. Võib osutuda vajalikuks antihüpertensiivse ravi alustamine või intensiivistamine. Kui vererõhku ei ole võimalik kontrollida, tuleb ravi alfaepoetiiniga lõpetada.
Ravi ajal alfaepoetiiniga on esinenud entsefalopaatia ja krampidega hüpertensiivseid kriise, mis nõuavad kohest arstiabi ja intensiivset arstiabi, isegi patsientidel, kellel on normaalne või madal vererõhk. Erilist tähelepanu tuleks pöörata võimalikule hoiatusmärgile migreenitaolistele hammustustele (vt lõik 4.8).
Alfaepoetiini tuleb kasutada ettevaatusega epilepsiaga patsientidel, kellel on esinenud krampe või haigusseisundeid, mis on seotud eelsoodumusega krampide tekkeks, nagu kesknärvisüsteemi infektsioonid ja aju metastaasid.
Kroonilise maksapuudulikkusega patsientidel tuleb alfaepoetiini kasutada ettevaatusega.Alfa epoetiini ohutus maksapuudulikkusega patsientidel ei ole kindlaks tehtud.
ESA -sid saanud patsientidel on täheldatud vaskulaarsete trombootiliste sündmuste (VTE) esinemissageduse suurenemist (vt lõik 4.8). Nende hulka kuuluvad veenide ja arterite tromboos ja emboolia (sealhulgas mõned surmaga lõppenud), nagu süvaveenitromboos, kopsuemboolia, võrkkesta tromboos ja müokardiinfarkt Lisaks on teatatud tserebrovaskulaarsetest õnnetustest (sh ajuinfarkt, ajuverejooks ja mööduvad isheemilised atakid).
Nende VTE riski tuleb hoolikalt kaaluda, võrreldes alfaepoetiinravi kasulikkusega, eriti patsientidel, kellel on olemasolevad VTE riskifaktorid, sealhulgas ülekaalulisus ja varasem VTE (nt süvaveenitromboos, kopsuemboolia ja tserebrovaskulaarsed õnnetused).
Hemoglobiini taset tuleb kõigil patsientidel hoolikalt jälgida, kuna patsientidel, kes saavad ravi näidatud kontsentratsioonist kõrgemal, võib trombemboolia ja surmaga lõppeda suurem risk.
Ravi ajal alfaepoetiiniga võib esineda mõõdukas annusest sõltuv trombotsüütide arvu suurenemine, kuigi normaalses vahemikus. See nähtus taandub ravi ajal. Lisaks on teatatud trombotsüteemiast, mis ületab normi, soovitatakse esimese 8 ravinädala jooksul regulaarselt trombotsüüte kontrollida.
Enne ravi alustamist tuleb hinnata ja ravida kõiki võimalikke aneemia põhjuseid (rauapuudus, folaadi või B12 -vitamiini puudus, alumiiniumimürgitus, infektsioon või põletik, verekaotus, hemolüüs ja mis tahes päritoluga luuüdi fibroos). tehakse annuse suurendamiseks. Enamikul juhtudel vähenevad seerumi ferritiini väärtused samaaegselt hematokriti väärtuste tõusuga. Optimaalse ravivastuse tagamiseks alfaepoetiinile tuleb tagada piisavad rauavarud ja vajadusel manustada rauapreparaate ( vt lõik 4.2):
• Kroonilise neerupuudulikkusega patsientidel on soovitatav raua lisamine, kui ferritiini tase on alla 100 ng / ml (elementaarne raud täiskasvanutele 200 ... 300 mg / päevas suu kaudu ja lastele 100 ... 200 mg / päevas suu kaudu).
• Vähktõvega patsientidel soovitatakse raua lisamist, kui transferriini küllastusväärtused on alla 20% (elementaarne raud 200 kuni 300 mg päevas suu kaudu).
• Patsientidele, kes osalevad autoloogse eeltootmise programmis, tuleb rauapreparaate (elementaarne raud 200 mg / päevas suukaudselt) manustada paar nädalat enne autoloogse vereloome algust, et saavutada kõrge rauavarud. Enne ravi alustamist alfaepoetiiniga ja ravikuuri ajal ravi alfaepoetiiniga.
• Patsientidele, kellele on plaanis teha suur plaaniline ortopeediline operatsioon, tuleb alfaepoetiinravi ajal manustada rauapreparaate (elementaarne raud 200 mg / päevas suu kaudu). "Rauapreparaate enne alfaepoetiinravi alustamist, et saavutada piisav rauavarud.
Epoetiin alfaga ravitud patsientidel on väga harva täheldatud porfüüria tekkimist või ägenemist.
Alfaepoetiini tuleb porfüüriaga patsientidel kasutada ettevaatusega.
Erütropoeesi stimuleerivate ainete (ESA) jälgitavuse tagamiseks tuleb manustatud ESA ärinimi alati registreerida või näidata patsiendi haigusloos.
Ravi vahetamine ühelt ESA -lt teisele peaks toimuma ainult asjakohase järelevalve all.
Puhas punaste rakkude aplaasia (PRCA)
Antikehade vahendatud puhast punaliblede aplaasiat (PRCA) on kirjeldatud kuude kuni aastate pärast, peamiselt kroonilise neerupuudulikkusega patsientidel, keda raviti subkutaanselt manustatava epoetiiniga.
Samuti on teatatud juhtudest C -hepatiidiga patsientidel, keda raviti interferooni ja ribaviriiniga kombinatsioonis ESA -ga. Epoetiin alfa ei ole heaks kiidetud C -hepatiidiga seotud aneemia raviks.
Patsientidel, kelle efektiivsus kaob järsult, mis on määratletud kui hemoglobiinisisalduse langus (1–2 g / dl kuus) koos suurenenud vereülekande vajadusega, tuleb läbi viia retikulotsüütide arv ja hinnata teadaolevaid põhjuseid, mis takistavad reaktsioon (näiteks raua, folaadi ja B12 -vitamiini puudus, alumiiniumimürgitus, infektsioon või põletik, verekaotus, hemolüüs ja mis tahes päritoluga luuüdi fibroos).
Hemoglobiinisisalduse ebaproportsionaalne langus ja raske aneemia tekkimine, mis on seotud madala retikulotsüütide arvuga, peaks lõpetama alfa-epoetiinravi ja tegema testi erütropoetiinivastaste antikehade olemasolu kohta.
Samuti tuleks kaaluda luuüdi uuringut PRCA diagnoosimiseks.
Ristreaktsiooni ohu tõttu ei tohi alustada ravi teiste ESA -dega.
Sümptomaatilise aneemia ravi täiskasvanud ja lastel kroonilise neerupuudulikkusega (CRI) patsientidel:
Kroonilise neerupuudulikkusega patsientidel, kes saavad alfaepoetiini, tuleb regulaarselt mõõta hemoglobiini taset, kuni saavutatakse stabiilne tase ja seejärel perioodiliselt mõõta.
Kroonilise neerupuudulikkusega patsientidel, et vähendada vererõhu tõusu riski, peaks hemoglobiin suurenema ligikaudu 1 g / dl kuus (0,62 mmol / l) ja see ei tohiks ületada 2 g / dl kuus (1,25 mmol / l).
Kroonilise neerupuudulikkusega patsientidel ei tohiks hemoglobiini säilituskontsentratsioon ületada maksimaalset hemoglobiinisisalduse vahemikku, nagu on kirjeldatud lõigus 4.2. Kliinilistes uuringutes on täheldatud suurenenud suremuse ja tõsiste kardiovaskulaarsete sündmuste riski, kui kasutati erütropoeesi stimuleerivaid aineid (ESA). manustada, et saavutada hemoglobiini kontsentratsioon üle 12 g / dl (7,5 mmol / ml).
Kontrollitud kliinilised uuringud ei ole näidanud olulist kasu epoetiinide manustamisest, kui hemoglobiini kontsentratsioon ületab aneemia sümptomite kontrollimiseks ja vereülekande vältimiseks vajaliku taseme.
Kroonilise neerupuudulikkusega patsientidel tuleb EPREXi annuse suurendamisel olla ettevaatlik, kuna epoetiini suurte kumulatiivsete annustega võib kaasneda suurenenud suremuse, tõsiste kardiovaskulaarsete ja tserebrovaskulaarsete sündmuste risk. Patsientidel, kellel on halb hemoglobiinivastus. Epoetiinidele, alternatiiv selle halva ravivastuse põhjust tuleb otsida (vt lõigud 4.2 ja 5.1).
Kroonilise neerupuudulikkusega patsiente, keda ravitakse subkutaanse alfaepoetiiniga, tuleb regulaarselt jälgida efektiivsuse vähenemise suhtes, mis tähendab, et epoetiin alfa puudumine või ravivastuse vähenemine patsientidel, kes varem ravile allusid. Seda nähtust iseloomustab püsiv hemoglobiinisisalduse langus võrreldes alfaepoetiini annuse suurenemisega (vt lõik 4.8).
Mõnedel patsientidel, keda ravitakse alfaepoetiiniga pikemate annustamisintervallidega (rohkem kui üks kord nädalas), ei pruugi hemoglobiinisisaldus püsida piisav (vt lõik 5.1) ja võib vajada annuse suurendamist. Hemoglobiini taset tuleb regulaarselt jälgida.
Hemodialüüsi saavatel patsientidel on esinenud veresoonte ligipääsu tromboosi, eriti patsientidel, kellel on kalduvus hüpotensioonile ja kellel on arteriovenoossete fistulite tüsistused (nt stenoos, aneurüsmid jne). Nendel patsientidel on soovitatav veresoonte juurdepääsu ennetav kontroll ja tromboosi profülaktika koos atsetüülsalitsüülhappe manustamisega.
Üksikjuhtudel on täheldatud hüperkaleemiat, kuigi põhjuslikku seost ei ole kindlaks tehtud. Kroonilise neerupuudulikkusega patsientidel tuleb seerumi elektrolüüte jälgida. Kui täheldatakse kõrgenenud (või tõusvat) kaaliumisisaldust seerumis, tuleb lisaks hüperkaleemia asjakohasele ravile kaaluda alfaepoetiinravi katkestamist kuni seerumi kaaliumisisalduse korrigeerimiseni.
Hemodialüüsi ajal on sageli vaja hepariini annust suurendada hematokriti väärtuse suurenemise tõttu. Kui hepariini annuste kohandamine ei ole optimaalne, võib tekkida dialüsaatori oklusioon. Seni kättesaadavate andmete põhjal ei kiirenda aneemia korrigeerimine alfaepoetiiniga kroonilise neerupuudulikkusega täiskasvanud patsientidel, kes ei saa veel dialüüsi, neerupuudulikkuse progresseerumist.
Keemiaravist põhjustatud aneemiaga patsientide ravi
Vähktõvega patsiente, kes saavad alfaepoetiini, tuleb regulaarselt mõõta hemoglobiini taset, kuni saavutatakse stabiilne tase ja seejärel perioodiliselt mõõta.
Erütropoetiinid on kasvufaktorid, mis stimuleerivad sisuliselt punaste vereliblede tootmist. Erütropoetiini retseptoreid saab ekspresseerida mitmesuguste vähirakkude pinnal. Nagu kõigi kasvufaktorite puhul, on ka teoreetiline mure, et erütropoetiinid võivad stimuleerida kasvaja kasvu.
Mõnedes kontrollitud kliinilistes uuringutes ei ole näidatud, et erütropoetiinid parandaksid kasvajaga seotud aneemiaga patsientidel üldist elulemust ega vähendaksid kasvaja progresseerumise riski.
Kontrollitud kliinilistes uuringutes on alfaepoetiini ja teiste erütropoeesi stimuleerivate ainete (ESA) kasutamine näidanud:
• vähenenud lokoregionaalne kontroll kaugelearenenud pea- ja kaelavähiga patsientidel, kes saavad kiiritusravi, kui seda manustatakse hemoglobiini taseme saavutamiseks üle 14 g / dl (8,7 mmol / l);
• üldine elulemus ja haiguse progresseerumisest tingitud suremuse suurenemine 4 kuu pärast metastaatilise rinnavähiga patsientidel, kes saavad keemiaravi, kui seda manustatakse hemoglobiinitaseme saavutamiseks vahemikus 12–14 g / dl (7,5–8,7 mmol / l);
• suurenenud suremuse risk, kui seda manustatakse hemoglobiinitaseme 12 g / dl (7,5 mmol / l) saavutamiseks; aktiivse neoplaasiaga patsientidel, kes ei saa keemia- ja / või kiiritusravi. Ravi erütropoeesi stimuleerivate ainetega (ESA -d) ei ole selles patsientide populatsioonis näidustatud.
Eespool öeldut silmas pidades tuleks vähktõvega patsientide aneemia ravis teatud kliinilistes olukordades eelistada vereülekannet. Rekombinantse erütropoetiini manustamise otsus peab põhinema kasu ja riski hindamisel, kaasates patsiendi individuaalselt. peab hindama oma konkreetset kliinilist konteksti. Selle hindamise käigus tuleb arvesse võtta vähktüüpi ja selle progresseerumist; aneemia aste; eeldatav eluiga; keskkond, kus patsienti ravitakse; patsiendi eelistused (vt lõik 5.1).
Keemiaravi saavatel vähipatsientidel tuleb alfa-epoetiinravi sobivuse hindamisel hoolikalt kaaluda 2-3-nädalast intervalli manustamise ja ESA-indutseeritud punaste vereliblede ilmumise vahel (transfusiooniohtlikud patsiendid).
Täiskasvanud patsiendid, kes kandideerivad kirurgilisteks sekkumisteks, mis on osa autoloogsetest vereloovutusprogrammidest
Tuleb järgida kõiki hoiatusi ja erilisi ettevaatusabinõusid, mis on seotud autoloogse vereloovutusprogrammiga, eriti tavapärase mahu asendamisega.
Patsiendid, kes kandideerivad suuremahuliseks plaaniliseks ortopeediliseks operatsiooniks
Enne operatsiooni tuleb alati järgida häid verejuhtimise tavasid.
Patsiendid, kes on plaanilise suure ortopeedilise kirurgia kandidaadid, peaksid saama piisavat tromboosivastast profülaktikat, kuna operatsioonil olevatel patsientidel, eriti neil, kellel on kardiovaskulaarsed häired, võivad tekkida trombootilised ja vaskulaarsed sündmused. Lisaks tuleb ettevaatusabinõusid rakendada patsientidel, kellel on eelsoodumus. süvaveenide tromboosi (DVT) tekkimist. Lisaks ei saa välistada operaatoreid patsientidel, kelle hemoglobiini algväärtus on> 13 g / dl, võimalusega, et ravi alfaepoetiiniga võib suurendada tromboosijärgsete / vaskulaarsete sündmuste riski. . Seetõttu ei tohi alfaepoetiini kasutada patsientidel, kelle hemoglobiini algväärtus on> 13 g / dl.
04.5 Koostoimed teiste ravimitega ja muud koostoimed
Puuduvad tõendid selle kohta, et ravi alfaepoetiiniga muudaks teiste ravimite metabolismi. Erütropoeesi vähendavad ravimid võivad vähendada reaktsiooni alfaepoetiinile.
Kuna tsüklosporiin seondub punaste verelibledega, võib selle ravimiga esineda koostoime.
Samaaegse manustamise korral tuleb tsüklosporiini sisaldust veres jälgida ja annust kohandada vastavalt hematokriti suurenemisele.
G-CSF-i, GM-CSF-i ja alfaepoetiini vahel puuduvad in vitro koostoimed hematoloogilise diferentseerumise või proliferatsiooni osas in vitro kasvaja biopsia proovidest.
Metastaatilise rinnavähiga täiskasvanud naispatsientidel ei avaldanud alfaepoetiini 40 000 RÜ / ml subkutaanne manustamine koos trastuzumabi 6 mg / kg trastuzumabi farmakokineetikat.
04.6 Rasedus ja imetamine
Rasedus
Puuduvad piisavad ja hästi kontrollitud uuringud rasedate naiste kohta. Loomkatsed on näidanud reproduktiivtoksilisust (vt lõik 5.3). Sellest tulenevalt tohib alfaepoetiini raseduse ajal kasutada ainult juhul, kui oodatav kasu kaalub üles võimaliku ohu lootele. Alfaepoetiini ei soovitata kasutada rasedatel, kes on autoloogse vereloovutusprogrammis osalevad operatsioonikandidaadid.
Toitmisaeg
Ei ole teada, kas eksogeenne alfaepoetiin eritub inimese rinnapiima. Alfaepoetiini tuleb imetavatel naistel kasutada ettevaatusega.Otsus rinnaga toitmise jätkamise / lõpetamise või alfaepoetiinravi jätkamise / lõpetamise kohta tuleb teha, arvestades rinnaga toitmise kasu imikule ja alfaepoetiinravi kasulikkust naisele.
Alfaepoetiini kasutamine ei ole soovitatav imetavatele naistele, kes kandideerivad operatsioonile ja osalevad autoloogse vereloovutusprogrammis.
Viljakus
Puuduvad uuringud, mis hindaksid alfaepoetiini võimalikku mõju meeste või naiste viljakusele.
04.7 Mõju autojuhtimise ja masinate käsitsemise võimele
Uuringuid autojuhtimise ja masinate käsitsemise võime kohta ei ole läbi viidud.
04.8 Kõrvaltoimed
Ohutusprofiili kokkuvõte
Kõige sagedasem kõrvaltoime alfa-epoetiinravi ajal on annusest sõltuv vererõhu tõus või olemasoleva hüpertensiooni süvenemine.
Vererõhu suundumust on soovitatav jälgida eriti ravi alguses (vt lõik 4.4).
Kõige sagedasemad kõrvaltoimed, mis esinesid alfaepoetiini kliinilistes uuringutes, on kõhulahtisus, iiveldus, oksendamine, palavik ja peavalu. Gripilaadsed sümptomid võivad ilmneda valdavalt ravi alguses.
Annuste vahemiku pikendamise kliinilistes uuringutes neerupuudulikkusega täiskasvanud patsientidel, kes ei saa veel dialüüsi, on teatatud hingamisteede ummistusest, sealhulgas ülemiste hingamisteede ummistustest, ninakinnisusest ja nina-neelupõletikust.
ESA saanud patsientidel on täheldatud vaskulaarsete trombootiliste sündmuste (TVE) esinemissageduse suurenemist (vt lõik 4.4).
Kõrvaltoimete tabel
Kokku 3262 patsiendist 23 randomiseeritud, topeltpimedas, platseebo- või standardraviga kontrollitud kliinilises uuringus hinnati EPREXi üldist ohutusprofiili 1 922 aneemiaga patsiendil. Neljas kroonilise neerupuudulikkuse uuringus osales 228 ICR-ga patsienti, keda raviti alfaepoetiiniga (2 uuringut enne dialüüsi [N = 131 ICR-ga kokku puutunud patsienti] ja 2 dialüüsi (N = 97 ICR-ga kokku puutunud patsienti)); 1404 vähktõvega patsienti, kes puutusid kokku 16 uuringus keemiaravi põhjustatud aneemia kohta; 147 patsienti, kes olid eksponeeritud kahes uuringus autoloogse vere loovutamise eel, ja 213 patsienti, kes olid eksponeeritud ühes uuringus perioperatiivsel perioodil. Ravimi kõrvaltoimetest teatati ≥ 1% Nendes kliinilistes uuringutes on alfaepoetiin näidatud allolevas tabelis.
Erinevate esinemissageduste kohta kehtivad järgmised määratlused: väga sage (≥ 1/10), sage (≥ 1/100 kuni
Valitud kõrvaltoimete kirjeldus
On teatatud ülitundlikkusreaktsioonidest, sealhulgas lööbe (sh urtikaaria) juhtudest, anafülaktilistest reaktsioonidest ja angioödeemist.
Ravi ajal alfaepoetiiniga on esinenud entsefalopaatia ja krampidega hüpertensiivseid kriise, mis nõudsid kohest arstiabi ja intensiivset arstiabi, isegi patsientidel, kellel on varem normaalne või madal vererõhk. Võimaliku hoiatusmärgina tuleb erilist tähelepanu pöörata migreenitaolistele hammustustele (vt lõik 4.4).
Väga harva on teatatud antikehade vahendatud puhtast punaliblede aplaasiast
Hemodialüüsi saavatel kroonilise neerupuudulikkusega lastel
Kliinilistes uuringutes ja turuletulekujärgsel perioodil on hemodialüüsi saavatel kroonilise neerupuudulikkusega lastel kokkupuude piiratud. Selles populatsioonis ei ole teatatud lastel esinevatest spetsiifilistest kõrvaltoimetest ega põhihaigusele tüüpilistest kõrvaltoimetest.
Arvatavatest kõrvaltoimetest teatamine
Pärast ravimi müügiloa väljastamist tekkinud arvatavatest kõrvaltoimetest teatamine on oluline, kuna see võimaldab pidevalt jälgida ravimi kasu ja riski suhet. Tervishoiutöötajatel palutakse teavitada kõigist võimalikest kõrvaltoimetest riikliku teavitussüsteemi kaudu. "Aadress http: //www.agenziafarmaco.gov.it/it/responsabili.
04.9 Üleannustamine
Epoetiin alfa terapeutiline piir on väga lai. Alfaepoetiini üleannustamine võib avaldada mõju, mis pikendab hormooni farmakoloogilist toimet. Kui leitakse liiga kõrge hemoglobiinisisaldus, võib teha flebotoomia.
Täiendavat toetavat ravi tuleb osutada vastavalt patsiendi seisundile.
05.0 FARMAKOLOOGILISED OMADUSED
05.1 Farmakodünaamilised omadused
Farmakoterapeutiline rühm: aneemiavastased ravimid, ATC-kood: B03XA01.
Toimemehhanism
Erütropoetiin (EPO) on glükoproteiinhormoon, mida toodab peamiselt neer vastuseks hüpoksiale ja mis on punaste vereliblede (RBC) tootmise peamine regulaator. "EPO osaleb erütroidide arengu kõigis faasides ja selle peamine toime on erütroidi prekursorite tasemel. Pärast seda, kui EPO seondub oma retseptoriga rakupinnal, aktiveerib see signaaliülekande rajad, mis häirivad" apoptoosi ja stimuleerivad erütroidrakkude proliferatsiooni. Rekombinantne hiina hamstri munasarjarakkudes väljendatud inimese erütropoetiinil (alfaepoetiinil) on 165 aminohappe järjestus, mis on identne inimese uriini EPO omaga; kaks on funktsionaalsete testide põhjal eristamatud. Erütropoetiini näiv molekulmass on 32 000–40 000 daltonid.
Erütropoetiin on kasvufaktor, mis stimuleerib peamiselt erütrotsüütide tootmist.Erütropoetiini retseptoreid saab ekspresseerida mitmesuguste vähirakkude pinnal.
Farmakodünaamilised toimed
Terved vabatahtlikud
Pärast alfaepoetiini üksikannuste manustamist (20 000 kuni 160 000 RÜ subkutaanselt) täheldati annusest sõltuvat vastust uuritud farmakodünaamiliste markerite, sealhulgas retikulotsüütide, punaste vereliblede ja hemoglobiini suhtes. Retikulotsüütide protsendi muutuste korral täheldati piigi ja tagasi algtasemele kindlaksmääratud kontsentratsiooni-ajaprofiili. Erütrotsüütide ja hemoglobiini puhul täheldati vähem määratletud profiili. Üldiselt suurenesid kõik farmakodünaamilised markerid lineaarselt, kui annused saavutasid maksimaalse ravivastuse maksimaalse annuse juures.
Täiendavates farmakodünaamilistes uuringutes uuriti 40 000 RÜ üks kord nädalas, võrreldes 150 RÜ / kg 3 korda nädalas. Vaatamata erinevustele kontsentratsiooni-aja profiilides, oli farmakodünaamiline vastus (mõõdetuna retikulotsüütide, hemoglobiini ja punaste vereliblede muutuste protsentuaalse muutuse järgi) nende skeemide puhul sarnane. Täiendavates uuringutes võrreldi alfaepoetiini 40 000 RÜ raviskeemi üks kord nädalas kahe nädala tagant manustatavate annustega vahemikus 80 000 kuni 120 000 RÜ subkutaanselt. Üldiselt, nende tervete isikute farmakodünaamiliste uuringute tulemuste põhjal, tundub 40 000 RÜ üks kord nädalas manustatav raviskeem punaste vereliblede tootmisel efektiivsem kui kahenädalane raviskeem, hoolimata retikulotsüütide tootmise sarnasusest. Kord nädalas ja kord nädalas.
Krooniline neerupuudulikkus
On näidatud, et alfaepoetiin stimuleerib erütropoeesi kroonilise neerupuudulikkusega aneemilistel patsientidel, sealhulgas dialüüsi saavatel ja dialüüsieelsetel patsientidel.Esimene tõend epoetiin alfa ravivastuse kohta on retikulotsüütide arvu suurenemine 10 päeva jooksul, millele järgneb punaste vereliblede, hemoglobiini ja hematokriti arvu suurenemine, tavaliselt 2-6 nädala jooksul. Hemoglobiinivastus varieerub patsientide vahel ning seda võivad mõjutada raualadestused ja kaasnevad meditsiinilised probleemid.
Keemiaravi põhjustatud aneemia
On näidatud, et epoetiin alfa, mida manustatakse 3 korda nädalas või üks kord nädalas, suurendab keemiaravi saavatel aneemiavähiga patsientidel hemoglobiini ja vähendab vereülekande vajadust pärast esimest ravikuud.
Uuringus, milles võrreldi annustamisskeeme 150 RÜ / kg 3 korda nädalas ja 40 000 RÜ üks kord nädalas tervetel isikutel ja aneemilistel vähihaigetel, olid retikulotsüütide, hemoglobiini ja punaste vereliblede üldise muutuse ajalised profiilid sarnased kaks annustamisskeemi tervetel ja aneemilistel vähihaigetel. Vastavate farmakodünaamiliste parameetrite AUC -d olid 150 RÜ / kg 3 korda nädalas ja 40 000 RÜ üks kord nädalas annustamisskeemide puhul sarnased nii tervetel kui ka aneemilistel vähihaigetel.
Täiskasvanud kirurgilised patsiendid autoloogse annetusprogrammi raames
On näidatud, et alfaepoetiin stimuleerib punaste vereliblede tootmist, et suurendada autoloogse vere kogumist ja piirata hemoglobiinisisalduse langust täiskasvanud patsientidel, kellele plaanitakse teha suur plaaniline operatsioon ja kelle puhul ei eeldata täielikku perioperatiivset eelsalvestust. Suurimat toimet täheldati madala hemoglobiinisisaldusega patsientidel (≤ 13 g / dl).
Täiskasvanud patsientide ravi plaanilise ortopeedilise operatsiooni jaoks
Patsientidel, kellele on plaanis teha suur plaaniline ortopeediline operatsioon ja hemoglobiini eeltöötlus> 10 kuni ≤ 13 g / dl, on näidatud, et alfaepoetiin vähendab allogeensete vereülekannete saamise riski ja kiirendab erütroidide taastumist (suurenenud hemoglobiinisisaldus, hematokrit ja retikulotsüütide arv).
Kliiniline efektiivsus ja ohutus
Krooniline neerupuudulikkus
Alfaepoetiini on kliinilistes uuringutes hinnatud aneemiaga täiskasvanud patsientidel, kellel on CRF, sealhulgas hemodialüüsi- ja dialüüsieelsed patsiendid, et ravida aneemiat ja hoida hematokriti kontsentratsioonivahemikus 30 ... 36%.
Kliinilistes uuringutes, kus algannused olid 50 ... 150 RÜ / kg kolm korda nädalas, reageeris ligikaudu 95% patsientidest kliiniliselt olulise hematokriti tõusuga. Pärast ligikaudu kahekuulist ravi tehti peaaegu kõik patsiendid vereülekannet. -Sõltumatu. saavutati hematokriti sihtmärk, kohandati iga patsiendi jaoks säilitusannus.
Kolmes suures kliinilises uuringus täiskasvanud dialüüsi saavatel patsientidel oli keskmine säilitusannus, mis oli vajalik hematokriti säilitamiseks vahemikus 30–36%, ligikaudu 75 RÜ / kg 3 korda nädalas.
Topeltpimedas, mitmekeskuselises, platseebokontrollitud uuringus hemodialüüsi saavatel CRF-ga patsientide elukvaliteedil täheldati kliiniliselt ja statistiliselt olulist paranemist alfaepoetiiniga ravitud patsientidel võrreldes platseebo rühmaga, mõõtes väsimust, füüsilisi sümptomeid, suhteid ja depressioon (neeruhaiguste küsimustik) pärast kuuekuulist ravi. Alfaepoetiinirühma patsiendid kaasati avatud laiendatud uuringusse, mis näitas, et nende elukvaliteet paranes veel 12 kuud.
Neerupuudulikkusega täiskasvanud patsiendid, kes ei saa veel dialüüsi
Kliinilistes uuringutes, milles osalesid CRF -ga patsiendid, kes ei saanud dialüüsi ja mida raviti alfaepoetiiniga, oli ravi keskmine kestus ligi viis kuud. Need patsiendid reageerisid alfaepoetiinravile sarnaselt dialüüsi saavatel patsientidele. CRF -ga patsientidel, kes ei saanud dialüüsi, ilmnes annusest sõltuvus ja hematokriti pidev tõus, kui alfaepoetiini manustati nii intravenoosselt kui ka subkutaanselt. Sarnaseid hematokriti kasvumäärasid täheldati ka alfaepoetiini manustamisel mõlemale. Lisaks alfaepoetiini annused 75 ... 150 RÜ / kg nädalas on näidatud, et hematokrit jääb 36–38% tasemele kuni kuueks kuuks.
Kahes EPREXi pikema annustamisintervalli uuringus (3 korda nädalas, üks kord nädalas, üks kord iga kahe nädala tagant ja kord nelja nädala jooksul) ei säilinud mõned pikema annustamisintervalliga patsiendid piisavat hemoglobiinisisaldust ja vastasid kehtestatud ärajätmise kriteeriumidele (0% üks kord nädalas, 3,7% kord 2 nädala jooksul ja 3,3% kord 4 nädala jooksul).
Prospektiivses randomiseeritud uuringus (CHOIR) hinnati 1432 kroonilise neerupuudulikkusega aneemilist patsienti, kes ei saanud dialüüsi. Patsientidele määrati ravi alfaepoetiiniga, mille eesmärk oli säilitada hemoglobiinisisaldus 13,5 g / dl (üle soovitatud hemoglobiini taseme) või 11,3 g / dl. Suur kardiovaskulaarne sündmus (surm, müokardiinfarkt, insult või haiglaravi südame paispuudulikkuse tõttu) , esines 125 (18%) 715 patsiendi seas kõrgema hemoglobiinirühmaga võrreldes 97 (14%) madalama hemoglobiinirühma 717 patsiendi seas (riski protsent [HR] 1,3, 95%CI: 1,0, 1,7, p = 0,03).
Kroonilise neerupuudulikkusega patsientidel (dialüüsi- ja dialüüsivälistel patsientidel, diabeetikutel ja mitte-diabeetikutel) viidi läbi ESA kliiniliste uuringute kumulatiivsed retrospektiivsed analüüsid. Olenemata patsiendi suhkurtõve või dialüüsi staatusest täheldati suundumust suurenenud suremuse, kardiovaskulaarsete ja tserebrovaskulaarsete sündmuste riski suurenemisele, mis on seotud ESA suuremate kumulatiivsete annustega (vt lõigud 4.2 ja 4.4).
Keemiaravi põhjustatud aneemiaga patsientide ravi
Alfaepoetiini on hinnatud kliinilistes uuringutes täiskasvanud aneemiaga vähihaigetel, kellel on lümfoidne ja soliidne kasvaja, ning patsientidel, kes kasutavad erinevaid keemiaravi raviskeeme, sealhulgas plaatina- ja plaatinaravita. Nendes uuringutes tõestati, et epoetiin alfa, mida manustati 3 korda nädalas ja üks kord nädalas, suurendas aneemiaga patsientidel hemoglobiini ja vähendas vereülekande vajadust pärast esimest ravikuud. Mõnes uuringus järgnes topeltpimedale faasile avatud faas, mille jooksul kõik patsiendid said alfaepoetiini ja täheldati toime säilimist.
Olemasolevad andmed viitavad sellele, et pahaloomuliste hematoloogiliste kasvajate ja soliidtuumoritega patsiendid reageerivad alfaepoetiinravile samaväärselt ning patsiendid, kellel on luuüdi infiltratsioon või mitte, reageerivad alfaepoetiinravile samaväärselt. Keemiaravi uuringutes oli võrreldav keemiaravi intensiivsus alfaepoetiin ja platseebo rühmades sarnane pindala neutrofiilide aja kõvera all patsientidel, keda raviti alfaepoetiiniga ja platseeboga, samuti sama osa patsientidega ravitud rühmades. alfaepoetiini ja platseebot saanud rühmade puhul, kelle neutrofiilide absoluutarv langes alla 1000 ja 500 rakku / mcL
Prospektiivses, topeltpimedas, randomiseeritud ja platseebokontrollitud uuringus, milles osales 375 mitte-müeloidse kasvajaga aneemiat põdevat patsienti, kes said plaatinapõhist keemiaravi, vähenes oluliselt aneemiaga seotud sümptomid (nt asteenia, väsimus ja vererõhu langus) aktiivsus), mõõdetuna järgmiste hindamisskaaladega: vähiteraapia-aneemia funktsionaalse hindamise üldine skaala (FACT-An); FAKT-Väsimusskaala ja vähi lineaarne analoogskaala (CLAS).
Kaks teist randomiseeritud ja platseebokontrolliga uuringut, mis viidi läbi väiksema arvu patsientidega, ei näidanud elukvaliteedi parameetrite paranemist vastavalt EORTC-QLQ-C30 ja CLAS skaalale.
Ellujäämist ja kasvaja progresseerumist uuriti viies suures kontrollitud uuringus, milles osales kokku 2833 patsienti, sealhulgas neli topeltpimedat platseebokontrolliga ja ühte avatud uuringut. Uuringutes osalesid nii keemiaravi saanud patsiendid (kaks uuringut) kui ka patsiendid, kellel ESA -de kasutamine ei olnud näidustatud: aneemiaga vähiga patsiendid, kes ei saa keemiaravi, ja pea- ja kaelavähiga patsiendid, kes saavad kiiritusravi. Soovitud kiiritusravi kontsentratsioonitase. Hemoglobiin kahes uuringutes oli> 13 g / dl; ülejäänud kolmes uuringus oli see 12 ... 14 g / dl. Avatud uuringus ei erinenud elulemus rekombinantse inimese erütropoetiiniga ravitud patsientide ja kontrollrühmade vahel. Neljas kontrollitud uuringus"ohumäär üldise elulemuse puhul jäi see vahemikku 1,25–2,47 kontrollide kasuks. Need uuringud näitasid seletamatult statistiliselt olulist suremuse suurenemist vähi aneemiaga patsientidel, keda raviti rekombinantse inimese erütropoetiiniga, võrreldes kontrollidega.Inimese rekombinantse erütropoetiiniga ravitud patsientide üldist elulemust võrreldes kontrolliga ei saanud rahuldavalt seletada tromboosi ja sellega seotud tüsistuste esinemissageduse erinevusega.
Patsienditaseme analüüs viidi läbi ka üle 13 900 vähihaige (keemia-, raadio-, radiokeemia- või mitteravi), kes osalesid 53 kontrollitud kliinilises uuringus erinevate epoetiinidega. Üldise elulemuse andmete metaanalüüs näitas täpse ohu suhte hinnangul 1,06 kontrollrühma kasuks (95% CI: 1,00, 1,12; 53 uuringut ja 13933 patsienti), samas kui vähihaigetel, kes said keemiaravi, oli üldine elulemus riskisuhe, oli see 1,04 (95% CI: 0,97, 1,11; 38 uuringut ja 10441 patsienti). Lisaks näitavad metaanalüüsid järjekindlalt trombembooliliste sündmuste suhtelise riski olulist suurenemist vähihaigetel, kes saavad rekombinantseid inimese erütropoetiini (vt lõik 4.4).
Autoloogne eeltootmise programm
Platseebokontrollitud topeltuuringus hinnati alfaepoetiini toimet autoloogse vere loovutamise hõlbustamiseks patsientidel, kellel oli madal hematokrit (≤ 39% ja kellel puudus ilmne rauapuudusest tingitud aneemia). Pimestatud 204 patsiendil ja ühel -pime platseebokontrollitud uuring, milles osales 55 patsienti.
Topeltpimedas uuringus raviti patsiente alfa-epoetiiniga 600 RÜ / kg või platseeboga intravenoosselt üks kord päevas iga 3 või 4 päeva järel 3 nädala jooksul (kokku 6 annust). Keskmiselt suutsid alfaepoetiiniga ravitud patsiendid eelnevalt hoiustada oluliselt rohkem vereühikuid (4,5 ühikut) kui platseebot saanud patsiendid (3,0 ühikut).
Üksikpimedas uuringus raviti patsiente alfa-epoetiiniga 300 RÜ / kg või 600 RÜ / kg või platseeboga intravenoosselt üks kord päevas iga 3 või 4 päeva järel 3 nädala jooksul (kokku 6 annust). Alfaepoetiiniga ravitud patsiendid suutsid platseeboga (2,9 ühikut) võrreldes eelnevalt ka olulisi täiendavaid vereühikuid (alfaepoetiin 300 RÜ / kg = 4,4 ühikut; alfaepoetiin 600 RÜ / kg = 4,7 ühikut) eelnevalt hoiustada.
Alfaepoetiinravi vähendas allogeense verega kokkupuutumise riski 50% võrreldes patsientidega, keda ei ravitud alfaepoetiiniga.
Suur plaaniline ortopeediline kirurgia
Epoetiin alfa (300 RÜ / kg või 100 RÜ / kg) mõju allogeensete vereülekannete toimele hinnati topeltpimedas platseebo-kontrollitud kliinilises uuringus rauapuudulikkusega täiskasvanud patsientidel, kes ootasid operatsiooni. Epoetiin alfa manustati subkutaanselt 10 päeva enne operatsiooni, operatsiooni päeval ja neli päeva pärast operatsiooni. Patsiendid klassifitseeriti nende hemoglobiini algtaseme järgi (≤ 10 g / dl,> 10 kuni ≤ 13 g / dl ja> 13 g / dl).
Alfaepoetiin 300 RÜ / kg vähendas oluliselt allogeensete vereülekannete riski patsientidel, kelle hemoglobiin oli enne ravi> 10 kuni ≤ 13 g / dl. Vereülekannet vajas 16% patsientidest, keda raviti 300 RÜ / kg alfaepoetiiniga, 23% alfaepoetiiniga 100 RÜ / kg ja 45% platseeboga.
Avatud paralleelrühma uuring rauapuudulikkusega täiskasvanud isikutel, kelle ravieelne hemoglobiin oli ≥ 10 kuni ≤ 13 g / dl ja kes ootasid puusa- või põlveliigese ortopeedilist operatsiooni, võrreldi ravi alfaepoetiiniga 300 RÜ / kg subkutaanselt 10 päeva enne operatsiooni, operatsiooni päeval ja neli päeva pärast operatsiooni, ravi alfaepoetiiniga 600 RÜ / kg subkutaanselt üks kord nädalas 3 nädala jooksul enne operatsiooni ja operatsiooni päeval.
Eeltöötlusest enne operatsiooni oli hemoglobiini keskmine tõus nädalas 600 RÜ / kg (1,44 g / dl) rühmas kahekordne kui 300 RÜ / kg ööpäevases rühmas (0,73 g / dl). Keskmine hemoglobiinitase oli mõlemas ravigrupis kogu operatsioonijärgse perioodi jooksul sarnane.
Mõlemas ravigrupis täheldatud erütropoeetiline reaktsioon tõi kaasa sarnased vereülekande määrad (16% rühmas 600 RÜ / kg nädalas ja 20% 300 RÜ / kg päevas)
Lapsed
Krooniline neerupuudulikkus
Alfaepoetiini hinnati avatud, randomiseeritud, avatud annuste vahemiku 52-nädalases kliinilises uuringus hemodialüüsi saavatel CRF-iga lastel. Uuringusse kaasatud patsientide keskmine vanus oli 11,6 aastat (vahemikus 0,5 kuni 20,1 aastat).
Epoetiin alfa manustati dialüüsijärgselt intravenoosselt 75 RÜ / kg nädalas 2 või 3 jagatud annusena, tiitrides 75 RÜ / kg nädalas 4-nädalaste intervallidega (kuni 300 RÜ / kg nädalas), 1 g / dl / kuus hemoglobiini tõusu saavutamiseks. Soovitud hemoglobiini tase oli 9,6 kuni 11,2 g / dl. 81 % patsientidest saavutas hemoglobiini sihttaseme. Keskmine sihtkohta kulunud aeg oli 11 nädalat, keskmine doos sihtkohta oli 150 RÜ / kg nädalas. Eesmärgi saavutanud patsientidest tegi seda 90% annustamisskeemi 3 korda nädalas.
Pärast 52 nädala möödumist jäi uuringusse 57% patsientidest, kes said keskmist annust 200 RÜ / kg nädalas.
05.2 Farmakokineetilised omadused
Imendumine
Pärast subkutaanset manustamist saavutab alfaepoetiinitase seerumis maksimumi 12 ... 18 tundi pärast manustamist. Pärast korduvate 600 RÜ / kg annuste manustamist subkutaanselt ei täheldatud kumulatsiooni.
Subkutaanselt süstitud alfaepoetiini absoluutne biosaadavus on tervetel isikutel ligikaudu 20%.
Levitamine
Keskmine jaotusruumala on 49,3 ml / kg pärast 50 ja 100 RÜ / kg intravenoosset manustamist tervetel isikutel. Pärast alfaepoetiini intravenoosset manustamist kroonilise neerupuudulikkusega isikutele oli jaotusruumala vahemikus 57–107 ml / kg pärast ühekordset manustamist (12 RÜ / kg) kuni 42–64 ml / kg pärast korduva annuse manustamist (48 ... 192 RÜ) / kg) vastavalt. Järelikult on jaotusruumala veidi suurem kui plasma maht.
Elimineerimine
Epoetiin alfa poolväärtusaeg pärast mitmeannuselist intravenoosset manustamist on tervetel isikutel ligikaudu 4 tundi. Poolväärtusaeg pärast subkutaanset manustamist on tervetel isikutel hinnanguliselt ligikaudu 24 tundi.
Keskmine CL / F väärtus 150 RÜ / kg kohta 3 korda nädalas ja 40 000 RÜ üks kord nädalas oli tervetel isikutel vastavalt 31,2 ja 12,6 ml / h / kg. Keskmine CL / F väärtus 150 RÜ / kg 3 korda nädalas ja 40 000 RÜ üks kord nädalas raviskeemide korral oli aneemilistel vähihaigetel vastavalt 45,8 ja 11,3 ml / h / kg. Enamikul tsüklilist keemiaravi saanud aneemilistest vähihaigetest oli CL / F madalam pärast subkutaanset annust 40 000 RÜ üks kord nädalas ja 150 RÜ / kg 3 korda nädalas, võrreldes tervete isikute väärtustega.
Lineaarsus / mittelineaarsus
Tervetel isikutel täheldati alfaepoetiinisisalduse annuses proportsionaalset suurenemist pärast 150 ja 300 RÜ / kg intravenoosset manustamist 3 korda nädalas. Alfaepoetiini ühekordsed subkutaansed annused 300 ... 2400 RÜ / kg andsid lineaarse seose keskmise C ja annuse ning keskmise AUC ja annuse vahel. Vahel täheldati pöördvõrdelist seost kliirensilmne ja annus tervetel isikutel.
Uuringutes, kus uuriti annuste vahelise intervalli pikenemist (40 000 RÜ üks kord nädalas ja 80 000, 100 000 ja 120 000 RÜ iga kahe nädala tagant), täheldati lineaarset, kuid annusega mitteseotud proportsionaalset seost keskmise Cmax ja annuse el "Keskmine AUC ja annus tasakaalukontsentratsiooni korral .
Farmakokineetiline / farmakodünaamiline suhe
Epoetiin alfa avaldab annusest sõltuvat toimet hematoloogilistele parameetritele, mis ei sõltu manustamisviisist.
Lapsed
Kroonilise neerupuudulikkusega lastel on teatatud poolväärtusajast ligikaudu 6,2-8,7 tundi pärast alfaepoetiini korduvat intravenoosset manustamist. Epoetiin alfa farmakokineetiline profiil lastel ja noorukitel näib olevat sarnane täiskasvanutega.
Neerupuudulikkus
Kroonilise neerupuudulikkusega patsientidel on alfaepoetiini poolväärtusaeg intravenoosselt manustatuna veidi pikem, ligikaudu 5 tundi, võrreldes tervete isikutega.
05.3 Prekliinilised ohutusandmed
Korduvate annuste toksikoloogilistes uuringutes koertel ja rottidel, kuid mitte ahvidel, seostati alfaepoetiinravi luuüdi fibroosi subkliinilise seisundiga. Luuüdi fibroos on kroonilise neerupuudulikkuse teadaolev komplikatsioon inimestel ja võib olla seotud sekundaarse hüperparatüreoidismiga või olla põhjustatud tundmatutest teguritest.Uuringus, milles osales 3 aastat alfaepoetiiniga ravitud hemodialüüsi saavatel patsientidel, ei olnud luuüdi fibroosi esinemissagedus suurem kui kontrolldialüüsi saanud patsientide rühmas, keda ei ravitud alfaepoetiiniga.
Epoetiin alfa ei kutsu esile geenimutatsioone bakterites (Amesi test), kromosoomide aberratsiooni imetajate rakkudes, mikrotuumasid hiirtel ega geenimutatsioone HGPRT lookuses.
Pikaajalisi kantserogeensusuuringuid ei ole läbi viidud. Andmete põhjal kirjanduses vastuolulised tulemused in vitro näitavad, et erütropoetiinidel võib olla kasvaja proliferatsioonis oma roll, kuid see on kliinilises praktikas ebakindel.
Inimese luuüdi rakkude rakukultuurides stimuleerib alfaepoetiin spetsiifiliselt erütropoeesi ega hõlma leukopoeesi Alfaepoetiin tsütotoksilist toimet luuüdi rakkudele ei ole täheldatud.
Loomkatsetes on näidatud, et alfaepoetiin vähendab loote kehakaalu, aeglustab luustumist ja suurendab loote suremust, kui seda manustatakse iganädalastes annustes, mis on ligikaudu 20 korda suuremad kui soovitatud nädalane annus inimestel. Neid muutusi peetakse ema kehakaalu vähenemise tõttu sekundaarseteks ja nende olulisus inimestele terapeutiliste annuste kasutamisel ei ole teada.
06.0 FARMATSEUTILINE TEAVE
06.1 Abiained
Polüsorbaat 80
Glütsiin
Süstevesi.
Ühealuseline naatriumfosfaatdihüdraat
Kahealuseline naatriumfosfaatdihüdraat
Naatriumkloriid
06.2 Sobimatus
Sobivusuuringute puudumise tõttu ei tohi ravimit teiste ravimitega segada.
06.3 Kehtivusaeg
18 kuud.
06.4 Säilitamise eritingimused
Hoida külmkapis (2 ° C ... 8 ° C). See temperatuurivahemik peab olema tagatud kuni patsiendile manustamiseni.
Hoida originaalpakendis, et kaitsta toodet valguse eest.
Mitte külmutada ega loksutada.
Ambulatoorseks kasutamiseks võib ravimit külmkapist välja võtta ilma asendamata maksimaalselt 3 päeva jooksul temperatuuril, mis ei ületa 25 ° C. Kui ravimit ei ole selle perioodi lõpus kasutatud, tuleb see hävitada.
06.5 Vahetu pakendi olemus ja pakendi sisu
0,3 ml (3000 RÜ) süstelahus eeltäidetud süstlas (I tüüpi klaas), millel on kolb (teflonkattega kumm) ja korpusega nõel (polüpropüleenkattega kumm) ja süstla külge kinnitatud nõelakaitseseade (polükarbonaat) - pakk 1.
0,4 ml (4000 RÜ) eeltäidetud süstlas (I tüüpi klaas), millel on kolb (teflonkattega kumm) ja korpusega nõel (polüpropüleenkattega kumm) ja süstla külge kinnitatud nõelakaitse (polükarbonaat)-pakend 1.
0,5 ml (5000 RÜ) süstelahus eeltäidetud süstlas (I tüüpi klaas), millel on kolb (teflonkattega kumm) ja korpusega nõel (polüpropüleenkattega kumm) ja süstla külge kinnitatud nõelakaitseseade (polükarbonaat) - pakk 1.
0,6 ml (6000 RÜ) süstelahus eeltäidetud süstlas (I tüüpi klaas) koos kolviga (teflonkattega kumm) ja korpusega nõel (polüpropüleenkattega kumm) ja süstla külge kinnitatud nõelakaitse (polükarbonaat) - pakk 1.
0,8 ml (7000 RÜ) süstelahus eeltäidetud süstlas (I tüüpi klaas), millel on kolb (teflonkattega kumm) ja korpusega nõel (polüpropüleenkattega kumm) ja süstla külge kinnitatud nõelakaitse (polükarbonaat) - pakk 1.
1,0 ml (10 000 RÜ) süstelahus eeltäidetud süstlas (I tüüpi klaas), millel on kolb (teflonkattega kumm) ja korpusega nõel (polüpropüleenkattega kumm) ja süstla külge kinnitatud nõelakaitseseade (polükarbonaat) - pakk 1.
06.6 Kasutamis- ja käsitsemisjuhised
Toodet ei tohi kasutada ja see tuleb ära visata:
• Kui tihend on katki;
• kui lahus on värviline või osakeste juuresolekul;
• Kui külmumine on toimunud või seda kahtlustatakse;
• Kui tekib külmiku rike.
Ühekordselt kasutatav toode. Pärast soovimatu lahuse koguse süstlast eemaldamist ärge manustage süstla kohta rohkem kui ühte annust. Vt pakendi infolehe lõiku 3. Kuidas EPREXi (süstimisjuhised) kasutada.
Eeltäidetud süstlad on varustatud nõela ohutusseadmega PROTECS nõela ohutusseadmega. Pakendi infoleht sisaldab kogu teavet turvaseadmega eeltäidetud süstalde kasutamise ja käsitsemise kohta. PROTECS nõel.
Kasutamata ravim ja sellest tekkinud jäätmed tuleb hävitada vastavalt kohalikele eeskirjadele.
07.0 MÜÜGILOA HOIDJA
Janssen -Cilag SpA, M. Buonarroti kaudu, 23 - 20093 Cologno Monzese (MI)
08.0 MÜÜGILOA NUMBER
027015167 - "10 000 RÜ / ML süstelahus eeltäidetud süstlas" 1 3000 RÜ / 0,3 ml süstal
027015179 - "10 000 RÜ / ML süstelahus eeltäidetud süstlas" 1 4000 RÜ / 0,4 ml süstal
027015231 - "10 000 RÜ / ML süstelahus eeltäidetud süstlas" 1 5000 RÜ / 0,5 ml süstal
027015243 - "10 000 RÜ / ML süstelahus eeltäidetud süstlas" 1 6000 RÜ / 0,6 ml süstal
027015268 - "10 000 RÜ / ML süstelahus eeltäidetud süstlas" 1 süstal 8000 RÜ / 0,8 ml
027015181 - "10 000 RÜ / ML süstelahus süstlis" 1 10 000 RÜ / 1 ml süstal
09.0 MÜÜGILOA VÕI UUENDAMISE KUUPÄEV
Mai 1989
AIC uuendamine: 4. august 2008
10.0 TEKSTI LÄBIVAATAMISE KUUPÄEV
08/2015