Toimeained: Raltegraviir
ISENTRESS 400 mg õhukese polümeerikattega tabletid
Isentressi pakendi infolehed on saadaval järgmistes pakendisuurustes:- ISENTRESS 400 mg õhukese polümeerikattega tabletid
- ISENTRESS 100 mg närimistabletid
- ISENTRESS 25 mg närimistabletid
- ISENTRESS 100 mg graanulid suukaudse suspensiooni jaoks
Näidustused Miks kasutatakse Isentressi? Milleks see mõeldud on?
Mis on Isentres
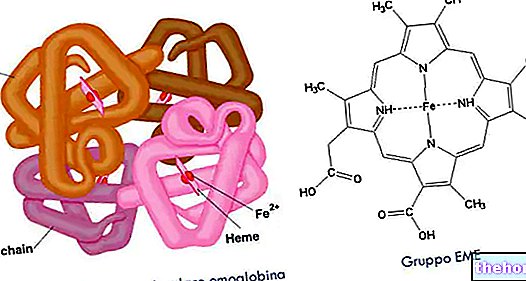
Isentress sisaldab toimeainena raltegraviiri. Isentress on viirusevastane ravim, mis toimib inimese immuunpuudulikkuse viiruse (HIV) vastu. See on viirus, mis põhjustab omandatud immuunpuudulikkuse sündroomi (AIDS).
Kuidas Isentress toimib
Viirus toodab ensüümi, mida nimetatakse HIV integraasiks. See aitab viirusel paljuneda tema keha rakkudes. Isentress peatab selle ensüümi aktiivsuse. Kui seda kasutatakse koos teiste ravimitega, võib Isentress vähendada HIV -i sisaldust teie veres (seda nimetatakse "viiruse koormuseks") ja suurendada teie CD4 -rakkude (teatud tüüpi valgete vereliblede) arvu. mängib olulist rolli terve immuunsüsteemi säilitamisel, et aidata võidelda infektsioonidega).
HIV -i hulga vähendamine veres võib parandada teie immuunsüsteemi toimimist. See tähendab, et teie keha saab infektsiooniga paremini võidelda.
Isentress ei pruugi kõigil patsientidel seda toimet avaldada.
Isentress ei ravi HIV -nakkust.
Millal Isentressi kasutada?
Isentressi kasutatakse HIV-nakkusega täiskasvanute, noorukite, laste ja imikute raviks alates 4. nädalast. Arst on teile määranud Isentressi, mis aitab hoida teie HIV -nakkust kontrolli all.
Vastunäidustused, kui Isentressi ei tohi kasutada
Ärge võtke Isentressi
Kui olete raltegraviiri või selle ravimi mis tahes koostisosa (de) suhtes allergiline.
Ettevaatusabinõud kasutamisel Mida on vaja teada enne Isentressi võtmist
Enne Isentressi võtmist pidage nõu oma arsti, apteekri või meditsiiniõega.
Pidage meeles, et Isentress ei ole HIV-nakkuse ravim. See tähendab, et võite jätkata nakkuste või muude HIV-iga seotud haiguste saamist. Jätkake selle ravimi võtmise ajal regulaarselt arsti külastamist.
Vaimse tervise probleemid
Rääkige oma arstile, kui teil on varem esinenud depressiooni või psühhiaatrilisi haigusi.Mõnedel seda ravimit kasutavatel patsientidel on teatatud depressioonist, sealhulgas enesetapumõtetest ja -käitumisest, eriti depressiooni või psühhiaatriliste haiguste all kannatavatel patsientidel.
Probleemid luudega
Mõnedel kombineeritud retroviirusevastast ravi saavatel patsientidel võib tekkida luuhaigus, mida nimetatakse osteonekroosiks (luu surm luu verevarustuse puudumise tõttu). Kombineeritud retroviirusevastase ravi kestus, kortikosteroidide kasutamine, alkoholi tarbimine, tugev immuunsüsteemi aktiivsuse langus, kõrgem kehamassiindeks võivad muu hulgas olla mitmed selle haiguse tekke riskifaktorid. Osteonekroosi tunnusteks on jäikus, valud liigestes (eriti puusas, põlves ja õlas) ning liikumisraskused. Kui märkate mõnda neist sümptomitest, võtke ühendust oma arstiga.
Maksaprobleemid
Rääkige oma arstile, apteekrile või meditsiiniõele, kui teil on varem esinenud maksaprobleeme, sealhulgas B- või C -hepatiit. Enne selle ravimi võtmise üle otsustamist võib arst hinnata teie maksahaiguse raskust.
HIV levik teistele
HIV -nakkus levib vere- või seksuaalse kontakti kaudu HIV -nakkusega inimesega. Selle ravimi võtmise ajal saate HIV -i edasi anda, kuigi retroviirusevastase ravi mõju vähendab riski. Arutage oma arstiga vajalikke ettevaatusabinõusid, et vältida nakkuse edastamine teistele inimestele.
Infektsioonid
Informeerige otsekohe oma arsti, apteekrit või meditsiiniõde, kui märkate infektsiooni sümptomeid, nagu palavik ja / või iiveldus. Mõnel kaugelearenenud HIV-nakkusega patsiendil, kellel on olnud oportunistlikud infektsioonid, kohe pärast ravi alustamist HIV-i põletikulised nähud ja sümptomid võib esineda varasemaid infektsioone ja need sümptomid arvatakse olevat tingitud organismi immuunvastuse paranemisest, mis võimaldab tal võidelda infektsioonidega, mis võisid ilmneda ilma selgete sümptomiteta.
Lisaks oportunistlikele infektsioonidele võivad tekkida ka autoimmuunhäired (seisund, mis tekib siis, kui immuunsüsteem ründab tervet kehakude) pärast HIV -nakkuse raviks kasutatavate ravimite võtmise alustamist. Autoimmuunhäired võivad tekkida mitu kuud pärast ravi algust. Kui märkate infektsiooni sümptomeid või muid sümptomeid, nagu lihasnõrkus, esmane nõrkus kätes ja jalgades, mis liiguvad keha pagasiruumi, südamepekslemine, värisemine või hüperaktiivsus, rääkige sellest pöörduge viivitamatult oma arsti poole.
Lihasprobleemid
Võtke otsekohe ühendust oma arsti, apteekri või meditsiiniõega, kui teil tekib selle ravimi võtmise ajal seletamatu lihasvalu, hellus või nõrkus.
Nahaprobleemid
Lööbe tekkimisel võtke kohe ühendust oma arstiga. Mõnedel seda ravimit kasutavatel patsientidel on teatatud tõsistest, eluohtlikest nahareaktsioonidest ja allergilistest reaktsioonidest.
Lapsed ja noorukid
Isentressi ei tohi kasutada alla 4 nädala vanustel imikutel.
Koostoimed Millised ravimid või toidud võivad muuta Isentressi toimet
Muud ravimid ja Isentress
Teatage oma arstile või apteekrile, kui te kasutate, olete hiljuti kasutanud või kavatsete kasutada mis tahes muid ravimeid ilma retseptita.
Isentress võib suhelda teiste ravimitega. Teatage oma arstile, apteekrile või meditsiiniõele, kui te võtate või olete hiljuti võtnud või kavatsete võtta
- antatsiidid. Isentressi ei soovitata võtta koos mõne antatsiidiga (alumiiniumi ja / või magneesiumi sisaldavate ravimitega). Rääkige oma arstiga teiste antatsiidide kohta, mida saate võtta.
- rifampitsiin (ravim, mida kasutatakse teatud infektsioonide, näiteks tuberkuloosi raviks), kuna see võib vähendada Isentressi taset. Teie arst võib kaaluda Isentressi annuse suurendamist, kui te võtate rifampitsiini.
Hoiatused Oluline on teada, et:
Rasedus ja imetamine
Kui te olete rase, imetate või arvate end olevat rase või kavatsete rasestuda, pidage enne selle ravimi kasutamist nõu oma arsti või apteekriga.
- Isentressi ei soovitata raseduse ajal kasutada, kuna seda ei ole rasedatel uuritud.
- HIV -nakkusega naised ei tohi oma lapsi rinnaga toita, sest nad võivad HIV -nakkuse saada rinnapiima kaudu.
Küsige oma arstilt, milline on parim viis lapse toitmiseks. Kui olete rase või toidate last rinnaga, pidage enne ravimi kasutamist nõu oma arsti, apteekri või meditsiiniõega.
Autojuhtimine ja masinatega töötamine
Ärge kasutage masinaid, ärge juhtige autot ega sõitke jalgrattaga, kui teil tekib pärast selle ravimi võtmist pearinglus.
Isentress õhukese polümeerikattega tabletid sisaldavad laktoosi
Kui arst on teile öelnud, et te ei talu teatud suhkruid, võtke enne selle ravimi kasutamist ühendust oma arstiga.
Annus, manustamisviis ja aeg Kuidas Isentressi kasutada: Annustamine
Võtke seda ravimit alati täpselt nii, nagu arst, apteeker või meditsiiniõde on teile rääkinud. Kui te ei ole milleski kindel, pidage nõu oma arsti, apteekri või meditsiiniõega. Isentressi tuleb kasutada koos teiste HIV -ravimitega.
- On väga oluline, et te võtaksite seda ravimit täpselt vastavalt juhistele.
Kui palju võtta
Täiskasvanud
Soovitatav annus on üks tablett (400 mg) suu kaudu kaks korda päevas.
- Ärge muutke annust ega lõpetage selle ravimi võtmist ilma oma arsti, apteekri või meditsiiniõega nõu pidamata.
Kasutamine lastel ja noorukitel
Isentressi soovitatav annus on 400 mg suu kaudu kaks korda päevas noorukitele ja lastele, kes kaaluvad vähemalt 25 kg.
Isentress on saadaval ka närimistablettidena lastele, kes kaaluvad vähemalt 11 kg, ja graanulitena suukaudseks suspensiooniks imikutele ja lastele alates 4 nädalast ning kaaluga vähemalt 3 kg ja alla 20 kg.
- Ärge muutke 400 mg tabletti suukaudse suspensiooni närimistabletiks või graanuliteks, enne kui olete oma arsti, apteekri või meditsiiniõega nõu pidanud.
Tablette ei soovitata närida, purustada ega poolitada, sest see võib muuta ravimi taset organismis. Seda ravimit võib võtta koos toiduga või ilma.
Kui te unustate Isentressi võtta
- Kui te unustate annuse võtmata, võtke see niipea, kui see teile meenub.
- Kui aga on käes järgmise annuse võtmise aeg, jätke unustatud annus vahele ja minge tagasi tavapärase skeemi juurde.
- Ärge võtke kahekordset annust, kui annus jäi eelmisel korral võtmata.
Kui te lõpetate Isentressi võtmise
On oluline, et te võtaksite Isentressi täpselt nii, nagu arst on teile määranud. Ärge lõpetage ravi, sest:
- On väga oluline, et te võtaksite kõiki oma HIV -ravimeid nii, nagu ette nähtud ja õigel kellaajal. See võimaldab teie ravimitel paremini toimida. See vähendab ka võimalust, et teie ravimid ei suuda enam HIV -iga võidelda (ka mida nimetatakse "ravimiresistentsuseks").
- Kui teie Isentressi varud hakkavad vähenema, küsige oma arstilt või apteekrilt rohkem. Seda seetõttu, et on väga oluline, et te ei jääks ilma ravimita kasvõi lühiajaliselt, viiruste sisaldus veres võib suureneda. See võib tähendada, et HIV -viirus hakkab Isentressi suhtes resistentsust arendama ja seda on raskem ravida.
Kui teil on lisaküsimusi selle ravimi kasutamise kohta, pidage nõu oma arsti, apteekri või meditsiiniõega.
Üleannustamine Mida teha, kui olete võtnud Isentressi liiga palju?
Ärge võtke rohkem tablette, kui arst on määranud. Kui te võtate liiga palju tablette, võtke ühendust oma arstiga
Kõrvaltoimed Millised on Isentressi kõrvaltoimed
Nagu kõik ravimid, võib ka Isentress põhjustada kõrvaltoimeid, kuigi kõigil neid ei teki.
Tõsised kõrvaltoimed - need on aeg -ajalt (võivad esineda kuni 1 inimesel 100 -st)
Pöörduge kohe oma arsti poole, kui märkate mõnda järgmistest:
- herpesinfektsioonid, sealhulgas vöötohatis
- aneemia, sealhulgas rauapuudusest tingitud vorm
- infektsiooni või põletiku tunnused ja sümptomid
- psüühikahäire
- enesetapukatse või -katse
- mao põletik
- maksapõletik
- maksapuudulikkus
- allergiline nahalööve
- teatud tüüpi neeruprobleemid
- võtta ravimeid soovitatust suuremas koguses
Pöörduge kohe oma arsti poole, kui märkate mõnda ülaltoodud kõrvaltoimetest.
Sage: võivad tekkida kuni 1 inimesel 10 -st
- vähenenud söögiisu
- unehäired; unistuste sisu muutmine; õudusunenäod; ebanormaalne käitumine; sügavat kurbust ja seda, et pole väärt
- pearinglus; peavalu
- tasakaalu kaotuse tunne
- turse; kõhuvalu; kõhulahtisus; liigne gaas maos või sooltes; iiveldus; oksendamine; seedehäired; röhitsemine
- teatud tüüpi lööve (sagedamini, kui seda kasutatakse koos darunaviiriga)
- väsimus; ebatavaline väsimus või nõrkus; palavik
- maksaensüümide aktiivsuse tõus veres; valgete vereliblede muutus; suurenenud vere rasvasisaldus; süljenäärmete või kõhunäärme sekreteeritavate ensüümide taseme tõus
Aeg -ajalt: järgnev võib mõjutada kuni 1 inimest 100 -st
- juuksejuurte infektsioon; mõju; viiruste põhjustatud nahainfektsioon; oksendamine või kõhulahtisus nakkusetekitaja tõttu; ülemiste hingamisteede infektsioon; lümfisõlmede abstsess
- tüügas
- valu lümfisõlmedes; madal valgete vereliblede arv, mis võitlevad infektsioonidega; paistes näärmed kaelas, kaenlaalustes ja kubemes
- allergiline reaktsioon
- suurenenud söögiisu; diabeet; suurenenud kolesterooli ja lipiidide sisaldus veres; kõrge veresuhkru tase; liigne janu; tõsine kehakaalu langus; kõrge rasvasisaldus (nt kolesterool ja triglütseriidid) veres; häiritud keharasv
- ärevuse tunne; segadustunne; depressiivne meeleolu; meeleolu muutused; paanikahoog
- mälukaotus; närvi kokkusurumisest tingitud valu käes; tähelepanuhäired; peapööritus pärast kiireid kehaasendi muutusi; muutunud maitse; suurenenud unisus; energiapuudus; unustus, migreen; tundlikkuse kaotus; käte ja / või jalgade tuimus või nõrkus; kipitus; unisus; pingepeavalu värisemine halb une kvaliteet
- nägemishäired
- helin, susin, vilistamine, helin või muu püsiv müra kõrvades
- südamepekslemine; aeglased südamelöögid; kiire või ebaregulaarne südametegevus
- kuumahood; kõrge vererõhk
- karm, terav või väsinud hääl; ninaverejooks; ninakinnisus
- valu ülakõhus; ebamugavustunne pärasooles; kõhukinnisus; suukuivus; kõrvetised; valulik neelamine; kõhunäärme põletik; haavand või haav maos või ülaosas verejooks pärakust; ebamugavustunne maos; igemepõletik; turses, punane, valulik keel
- rasva kogunemine maksa
- vinnid; ebanormaalne juuste väljalangemine või hõrenemine; naha punetus; ebanormaalne keharasva jaotus, mis võib hõlmata rasvade kadumist jalgadelt, kätelt ja näolt ning suurenenud rasva kogust kõhus; liigne higistamine; öine higistamine; naha paksenemine ja sügelus korduva kriimustamise tõttu; nahakahjustus; kuiv nahk
- liigesevalu, valulik liigesehaigus; seljavalu; luu- / lihasvalu; lihaste hellus või nõrkus; kaelavalu; valu kätes või jalgades; kõõluste põletik; mineraalide hulga vähenemine luudes
- neerukivid; urineerimine öösel; neeru tsüst
- erektsioonihäired; rindade suurenemine meestel; menopausi sümptomid
- ebamugavustunne rinnus; külmavärinad; näo turse; närvilisus; üldine halb enesetunne; kaela mass; käte, pahkluude või jalgade turse; valutama
- valgete vereliblede arvu vähenemine; vereliistakute (teatud tüüpi rakk, mis soodustab hüübimist) vähenemine; vereanalüüsid, mis näitavad neerufunktsiooni langust; kõrge veresuhkru tase; lihaste ensüümide sisalduse suurenemine veres; suhkru olemasolu uriinis; punaste vereliblede olemasolu uriinis; kaalutõus; vöökoha suurenemine; vere valkude (albumiini) vähenemine; suurenenud vere hüübimisaeg.
Täiendavad kõrvaltoimed lastel ja noorukitel
- hüperaktiivsus
Isentress -ravi ajal on teatatud lihasvalu, hellusest või nõrkusest.
Kliinilistes uuringutes täheldati Isentressi saanud patsientidel vähki sama sagedusega kui patsientidel, kes said muid HIV-vastaseid ravimeid, mis ei sisaldanud Isentressi.
Kõrvaltoimetest teatamine
Kui teil tekib ükskõik milline kõrvaltoime, pidage nõu oma arsti, apteekri või meditsiiniõega. Kõrvaltoime võib olla ka selline, mida selles infolehes ei ole nimetatud. Kõrvaltoimetest võite ka ise teavitada riikliku teavitussüsteemi kaudu. Lisateavet selle ravimi ohutuse kohta .
Aegumine ja säilitamine
- Hoidke seda ravimit laste eest varjatud ja kättesaamatus kohas.
- Ärge võtke seda ravimit pärast kõlblikkusaega, mis on märgitud pudelil pärast „Kõlblik kuni“. Kõlblikkusaeg viitab selle kuu viimasele päevale.
- See ravimpreparaat ei vaja säilitamisel eritingimusi.
Ärge visake ravimeid kanalisatsiooni ega olmejäätmete hulka. Küsige oma apteekrilt, kuidas visata ära ravimeid, mida te enam ei kasuta. See aitab kaitsta keskkonda.
Muu info
Mida Isentress sisaldab
Toimeaine on raltegraviir. Üks õhukese polümeerikattega tablett sisaldab 400 mg raltegraviiri (kaaliumina).
Abiained on: laktoosmonohüdraat, mikrokristalne tselluloos, veevaba kahealuseline kaltsiumfosfaat, hüpromelloos 2208, poloksameer 407, naatriumstearüülfumaraat ja magneesiumstearaat. Lisaks sisaldab kate järgmisi abiaineid: polüvinüülalkohol, titaandioksiid, polüetüleenglükool 3350, talk, punane raudoksiid ja must raudoksiid.
Kuidas Isentress välja näeb ja pakendi sisu
Õhukese polümeerikattega tablett on ovaalne, roosa, ühele küljele on pressitud "227". Saadaval on kaks pakendi suurust: 1 pudel 60 tabletiga ja 3 pudelit 60 tabletiga. D.
Kõik pakendi suurused ei pruugi olla müügil.
Allika pakendi infoleht: AIFA (Itaalia ravimiamet). Sisu avaldati jaanuaris 2016. Esitatud teave ei pruugi olla ajakohane.
Kõige ajakohasemale versioonile juurdepääsu saamiseks on soovitatav külastada AIFA (Itaalia ravimiamet) veebisaiti. Vastutusest loobumine ja kasulik teave.
01.0 RAVIMPREPARAADI NIMETUS
ISENTRESS 400 mg tabletid, mis on kaetud kilega
02.0 KVALITATIIVNE JA KVANTITATIIVNE KOOSTIS
Üks õhukese polümeerikattega tablett sisaldab 400 mg raltegraviiri (kaaliumina).
Teadaolevat toimet omav abiaine:
Üks tablett sisaldab 26,06 mg laktoosi (monohüdraadina).
Abiainete täielik loetelu vt lõik 6.1.
03.0 RAVIMVORM
Õhukese polümeerikattega tablett.
Roosa, ovaalne tablett, mille ühele küljele on pressitud "227".
04.0 KLIINILINE TEAVE
04.1 Näidustused
ISENTRESS on näidustatud kombinatsioonis teiste retroviirusevastaste ravimitega inimese immuunpuudulikkuse viiruse (HIV-1) infektsiooni raviks täiskasvanutel, noorukitel, lastel ja imikutel alates 4. nädalast (vt lõigud 4.2, 4.4, 5.1 ja 5.2).
04.2 Annustamine ja manustamisviis
Ravi peab alustama HIV -nakkuse ravis kogenud arst.
Annustamine
ISENTRESSi tuleb kasutada kombinatsioonis muu aktiivse retroviirusevastase raviga (ART) (vt lõigud 4.4 ja 5.1).
Täiskasvanud
Soovitatav annus on 400 mg (üks tablett) kaks korda päevas.
Lapsed ja noorukid
Vähemalt 25 kg kaaluvatel inimestel on soovitatav annus 400 mg (üks tablett) kaks korda päevas. Isikutel, kes ei suuda tabletti alla neelata, kaaluge närimistableti kasutamist.
ISENTRESS on saadaval ka närimistablettidena lastele, kelle kehakaal on vähemalt 11 kg, ja graanulite kujul suukaudseks suspensiooniks imikutele ja lastele alates 4. nädalast kehakaaluga vähemalt 3 kg ja alla 20 kg. Lisateavet annustamise kohta leiate Euroopa närimistablettide ja suukaudse suspensiooni granuleeritud ravimvormide Euroopa ravimi omaduste kokkuvõtetest.
Närimistableti maksimaalne annus on 300 mg kaks korda päevas. Kuna ravimvormid ei ole bioekvivalentsed, ei tohi 400 mg tabletti asendada närimistableti või suukaudse suspensiooni graanulitega (vt lõik 5.2). Närimistablette ja suukaudse suspensiooni graanuleid ei ole uuritud noorukitel (12 ... 18 aastat) ega HIV-nakkusega täiskasvanutel.
Eakad kodanikud
Raltegraviiri kasutamise kohta eakatel on vähe teavet (vt lõik 5.2). Seetõttu tuleb ISENTRESSi selles populatsioonis kasutada ettevaatusega.
Neerukahjustus
Neerukahjustusega patsientidel ei ole annuse kohandamine vajalik (vt lõik 5.2).
Maksakahjustus
Kerge kuni mõõduka maksakahjustusega patsientidel ei ole annuse kohandamine vajalik. Raltegraviiri ohutus ja efektiivsus raske maksahaigusega patsientidel ei ole tõestatud, seetõttu tuleb ISENTRESSi kasutada raske maksakahjustusega patsientidel ettevaatlikult (vt lõigud 4.4 ja 5.2).
Lapsed
Raltegraviiri ohutus ja efektiivsus alla 4 nädala vanustel imikutel ei ole veel tõestatud. Andmed puuduvad.
Manustamisviis
Suukaudseks kasutamiseks.
ISENTRESS 400 mg tablette võib manustada koos toiduga või ilma.
Tablette ei tohi närida, purustada ega poolitada farmakokineetilise profiili eeldatavate muutuste tõttu.
04.3 Vastunäidustused
Ülitundlikkus toimeaine või lõigus 6.1 loetletud mis tahes abiainete suhtes.
04.4 Erihoiatused ja asjakohased ettevaatusabinõud kasutamisel
Patsiente tuleb hoiatada, et praegune retroviirusevastane ravi ei ravi HIV -i ja ei ole tõestatud, et see takistab HIV -i edasikandumist teistele inimestele vere kaudu. Kuigi viirusevastane ravi tõhus viiruse pärssimine vähendab märkimisväärselt sugulisel teel levimise riski, jääkriski ei saa välistada. Tuleb võtta ettevaatusabinõusid, et vältida levikut vastavalt riiklikele juhistele.
Üldiselt täheldati raltegraviiri farmakokineetikas märkimisväärset individuaalset ja individuaalset varieeruvust (vt lõigud 4.5 ja 5.2).
Raltegraviiril on suhteliselt madal resistentsuse geneetiline barjäär. Seetõttu tuleb võimaluse korral manustada raltegraviiri koos kahe teise aktiivse retroviirusevastase ravimiga, et minimeerida viroloogilise ebaõnnestumise ja resistentsuse tekkimise võimalust (vt lõik 5.1).
AastalïLisaks ravile piirduvad kliiniliste uuringute andmed raltegraviiri kasutamise kohta kombinatsioonis kahe nukleotiidse pöördtranskriptaasi inhibiitoriga (emtritsitabiin ja tenofoviirdisoproksiilfumaraat).
Depressioon
On teatatud depressioonist, sealhulgas enesetapumõtetest ja -käitumisest, eriti patsientidel, kellel on depressioon või psühhiaatriline haigus. Ettevaatlik tuleb olla patsientidel, kellel on depressioon või psühhiaatriline haigus.
Maksakahjustus
Raltegraviiri ohutus ja efektiivsus raske maksahaigusega patsientidel ei ole tõestatud, seetõttu tuleb ISENTRESSi kasutada raske maksakahjustusega patsientidel ettevaatlikult (vt lõigud 4.2 ja 5.2).
Patsientidel, kellel on juba esinenud maksakahjustus, sealhulgas kroonilise hepatiidiga patsientidel, esineb kombineeritud retroviirusevastase ravi ajal sagedamini maksafunktsiooni häireid ja neid tuleb jälgida nagu tavaliselt. Kui sellistel patsientidel täheldatakse maksahaiguse süvenemist, tuleb kaaluda ravi katkestamist või lõpetamist.
Kroonilise B- või C-hepatiidiga patsientidel, keda ravitakse kombineeritud retroviirusevastase raviga, on suurem risk tõsiste ja eluohtlike maksa kõrvaltoimete tekkeks.
Osteonekroos
Kuigi etioloogia arvatakse olevat multifaktoriaalne (sh kortikosteroidide kasutamine, alkoholi tarbimine, raske immunosupressioon, kõrgem kehamassiindeks), on teatatud osteonekroosi juhtudest, eriti kaugelearenenud HIV-haigusega ja / või pikaajalise retroviirusevastase raviga patsientidel Patsientidele tuleb soovitada pöörduda arsti poole, kui neil tekivad liigesevalu ja -valu, liigesejäikus või liikumisraskused.
Immuunsüsteemi reaktivatsiooni sündroom
HIV-nakkusega patsientidel, kellel on raske immuunpuudulikkus kombineeritud retroviirusevastase ravi (CART) alustamise ajal, võib tekkida põletikuline reaktsioon asümptomaatilistele või allesjäänud oportunistlikele patogeenidele ja põhjustada tõsiseid kliinilisi seisundeid või sümptomite süvenemist. Tavaliselt on selliseid reaktsioone täheldatud esimestel nädalatel või kuudel pärast kombineeritud retroviirusevastase ravi (CART) alustamist. Selle olulised näited on tsütomegaloviiruse retiniit, generaliseerunud ja / või fokaalsed mükobakteriaalsed infektsioonid ja kopsupõletik Pneumocystis jiroveci (varem tuntud kui Pneumocystis carinii). Kõiki põletikulisi sümptomeid tuleb hinnata ja vajadusel alustada ravi.
Autoimmuunhäirete (nt Gravesi tõbi) esinemisest on teatatud ka immuunsuse taasaktiveerimise kontekstis; registreeritud aeg alguseni on siiski varieeruvam ja need sündmused võivad ilmneda mitu kuud pärast ravi algust.
Antatsiidid
ISENTRESSi samaaegne manustamine koos alumiiniumi ja magneesiumi sisaldavate antatsiididega põhjustas raltegraviiri taseme langust plasmas. ISENTRESSi ei soovitata kasutada koos alumiiniumi ja / või magneesiumi sisaldavate antatsiididega (vt lõik 4.5).
Rifampitsiin
Olge ettevaatlik, kui manustate ISENTRESSi koos tugevate uridiin-difosfor-glükuronosüültransferaasi (UGT) 1A1 indutseerijatega (nt rifampitsiin). Rifampitsiin vähendab raltegraviiri taset plasmas; mõju raltegraviiri efektiivsusele ei ole teada. Kui aga rifampitsiini samaaegset manustamist ei saa vältida, võib kaaluda ISENTRESSi annuse kahekordistamist täiskasvanutel. Puuduvad andmed ISENTRESSi ja rifampitsiini samaaegse manustamise kohta alla 18 -aastastel patsientidel. vanuses (vt lõik 4.5).
Müopaatia ja rabdomüolüüs
On teatatud müopaatiast ja rabdomüolüüsist. Kasutada ettevaatusega patsientidel, kellel on varem esinenud müopaatiat või rabdomüolüüsi või kellel on eelsoodumus, sealhulgas muid nende seisunditega seotud ravimeid (vt lõik 4.8).
Rasked naha- ja ülitundlikkusreaktsioonid
ISENTRESSi saanud patsientidel on teatatud tõsistest, eluohtlikest ja surmavatest nahareaktsioonidest, enamikul juhtudel samaaegselt teiste nende reaktsioonidega seotud ravimitega. Nende hulka kuuluvad Stevensi-Johnsoni sündroomi ja toksilise epidermaalse nekrolüüsi juhtumid. Samuti on teatatud ülitundlikkusreaktsioonidest, mida iseloomustab lööve, süsteemsed sümptomid ja mõnikord elundite talitlushäired, sealhulgas maksapuudulikkus. Lõpetage viivitamatult ravi ISENTRESSi ja teiste kahtlustatavate ainetega, kui tekivad raskete nahareaktsioonide või ülitundlikkusreaktsioonide nähud või sümptomid (sealhulgas, kuid mitte ainult, tugev nahalööve või lööve, millega kaasneb palavik, üldine halb enesetunne, väsimus, lihas- või liigesevalu, villid). , suu kahjustused, konjunktiviit, näoturse, hepatiit, eosinofiilia, angioödeem). Kliinilist seisundit, sealhulgas maksa aminotransferaasi, tuleb jälgida ja alustada sobivat ravi. ISENTRESS-i või muude kahtlustatavate ainetega ravi katkestamine pärast raske lööbe tekkimist võib põhjustada eluohtliku reaktsiooni.
Lööve
Lööve tekkis sagedamini ravi saanud ISENTRESSi ja darunaviiri sisaldavaid raviskeeme saanud patsientidel kui patsientidel, kes said ISENTRESSi ilma darunaviirita või darunaviiri ilma ISENTRESSita (vt lõik 4.8).
Laktoos
ISENTRESS õhukese polümeerikattega tabletid sisaldavad laktoosi. Patsiendid, kellel on harvaesinev pärilik galaktoositalumatus, Lappi laktaasi puudulikkus või glükoosi-galaktoosi imendumishäire, ei tohi seda ravimit võtta.
04.5 Koostoimed teiste ravimitega ja muud koostoimed
Haridus in vitro näitavad, et raltegraviir ei ole tsütokroom P450 (CYP) ensüümide substraat, ei inhibeeri ensüüme CYP1A2, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6 või CYP3A, ei indutseeri CYP3A4 ega pärsi P-põhist transporti. raltegraviir ei muuda nende ravimite farmakokineetikat, mis on nende ensüümide või P-glükoproteiini substraadid.
Uuringute põhjal in vitro Ja in vivo, raltegraviir elimineeritakse peamiselt UGT1A1 vahendatud glükuronidatsiooni raja kaudu.
Kuigi uuringud in vitro näitavad, et raltegraviir ei ole UDP glükuronosüültransferaasi (UGT) 1A1 ja 2B7 inhibiitor, on kliiniline uuring näidanud, et võib tekkida osaline UGT1A1 inhibeerimine in vivo põhineb täheldatud mõjul bilirubiini glükuronidatsioonile. Ravimite koostoimete puhul ei tundu selle toime ulatus siiski kliiniliselt oluline.
Täheldati raltegraviiri farmakokineetika märkimisväärset individuaalset ja individuaalset varieeruvust. Järgnev teave ravimite koostoime kohta põhineb geomeetrilistel keskmistel väärtustel; toimet üksikule patsiendile ei saa täpselt ennustada.
Raltegraviiri mõju teiste ravimite farmakokineetikale
Koostoimeuuringutes ei avaldanud raltegraviir kliiniliselt olulist mõju etraviriini, maraviroki, tenofoviiri, hormonaalsete rasestumisvastaste vahendite, metadooni, midasolaami ega bocepreviiri farmakokineetikale.
Mõnedes uuringutes põhjustas ISENTRESSi ja darunaviiri samaaegne manustamine darunaviiri plasmakontsentratsiooni mõõduka languse; selle toime mehhanism on teadmata. Raltegraviiri mõju darunaviiri plasmakontsentratsioonidele ei tundu siiski olevat kliiniliselt oluline.
Teiste ainete mõju raltegraviiri farmakokineetikale
Kuna raltegraviir metaboliseerub peamiselt UGT1A1 kaudu, tuleb olla ettevaatlik, kui ISENTRESSi manustatakse koos tugevate UGT1A1 indutseerijatega (nt rifampitsiin). Rifampitsiin vähendab raltegraviiri taset plasmas; mõju raltegraviiri efektiivsusele ei ole teada. Kui aga rifampitsiini samaaegset manustamist ei saa vältida, võib kaaluda ISENTRESSi annuse kahekordistamist täiskasvanutel. Puuduvad andmed ISENTRESSi ja rifampitsiini samaaegse manustamise kohta alla 18 -aastased (vt lõik 4.4). Teiste tugevalt ravimeid metaboliseerivate ensüümide indutseerijate, nagu fenütoiin ja fenobarbitaal, mõju UGT1A1 -le ei ole teada. Vähem tugevad indutseerijad (nt efavirens, nevirapiin, etraviriin, rifabutiin, glükokortikoidid, St. ürt, pioglitasoon) võib kasutada koos ISENTRESSi soovitatud annusega.
ISENTRESSi manustamine koos teiste ravimitega, mis teadaolevalt on tugevad UGT1A1 inhibiitorid (nt atasanaviir), võib suurendada raltegraviiri taset plasmas. Vähem tugevad UGT1A1 inhibiitorid (nt indinaviir, sakvinaviir) võivad samuti suurendada raltegraviiri taset plasmas, kuid vähemal määral kui atasanaviir. Lisaks võib tenofoviir suurendada raltegraviiri taset plasmas, kuid selle toimemehhanism ei ole teada (vt tabel 1). Kliinilistes uuringutes kasutas märkimisväärne osa patsiente optimeeritud raviskeemide hulgast atasanaviiri ja / või tenofoviiri, mis mõlemad suurendavad raltegraviiri taset plasmas. Atasanaviiri ja / või tenofoviiri kasutavate patsientide ohutusprofiil oli üldiselt sarnane patsientide ohutusprofiilile, kes neid ravimeid ei saanud ja seetõttu ei ole annuse kohandamine vajalik.
ISENTRESSi samaaegne manustamine kahevalentseid metallkatioone sisaldavate antatsiididega võib vähendada raltegraviiri imendumist kelaatimise teel, mille tulemuseks on raltegraviiri plasmakontsentratsiooni vähenemine. Seetõttu ei soovitata ISENTRESSi kasutada koos alumiiniumi ja / või magneesiumi sisaldavate antatsiididega. ISENTRESSi manustamine koos kaltsiumkarbonaati sisaldava antatsiidiga vähendas raltegraviiri taset plasmas; seda koostoimet ei peeta siiski kliiniliselt oluliseks. Seega, kui ISENTRESSi manustatakse koos kaltsiumkarbonaati sisaldavate antatsiididega, ei ole annuse kohandamine vajalik.
ISENTRESSi samaaegne manustamine koos teiste mao pH taset tõstvate ainetega (nt omeprasool ja famotidiin) võib suurendada raltegraviiri imendumist ja suurendada raltegraviiri taset plasmas (vt tabel 1). III faasi uuringutes olid prootonpumba inhibiitoreid või H2 antagoniste kasutavate patsientide alarühma ohutusprofiilid võrreldavad nendega, kes neid antatsiide ei võtnud. Seetõttu ei ole prootonpumba inhibiitorite või H2 antagonistide kasutamisel annuse kohandamine vajalik.
Kõik koostoimeuuringud viidi läbi täiskasvanutel.
Tabel 1
Farmakokineetilise koostoime andmed
04.6 Rasedus ja imetamine
Rasedus
Raltegraviiri kasutamise kohta rasedatel ei ole piisavalt andmeid. Loomkatsed on näidanud reproduktiivtoksilisust (vt lõik 5.3). Võimalik risk inimestele ei ole teada. ISENTRESSi ei tohi raseduse ajal kasutada.
Rasedusregister koos retroviirusevastaste ravimitega
Et jälgida raseduse ajal tahtmatult ISENTRESS-iga ravitud patsientide ema-loote tulemusi, loodi retroviirusevastaseid ravimeid kasutavate patsientide rasedusregister. Arstidel soovitatakse patsiendid sellesse registrisse registreerida.
Üldjuhul, kui otsustatakse retroviirusevastaste ravimite kasutamist rasedate naiste HIV -nakkuse raviks ja sellest tulenevalt HIV -i vertikaalse ülekandumise riski vähendamiseks vastsündinutele, tuleb üldjuhul arvesse võtta nii loomade andmeid kui ka kliinilist kogemust rasedatel naistel. et iseloomustada ohutust lootele.
Toitmisaeg
Ei ole teada, kas raltegraviir eritub rinnapiima. Raltegraviir eritub siiski imetavate rottide piima. Rottidel oli ema annuses 600 mg / kg ööpäevas toimeaine keskmine kontsentratsioon piimas ligikaudu 3 korda suurem kui emasplasmas. Imetamine ei ole ISENTRESS-ravi ajal soovitatav.Üldreeglina soovitatakse HIV-nakkusega emadel HIV-i edasikandumise vältimiseks oma lapsi rinnaga toita.
Viljakus
Isaste ja emaste rottide annustes kuni 600 mg / kg ööpäevas ei täheldatud toimet fertiilsusele, mille tulemuseks oli kokkupuude 3 korda suurem kui soovitatud annuse korral inimestel.
04.7 Mõju autojuhtimise ja masinate käsitsemise võimele
Ravi ajal sh ISENTRESSiga on mõnedel patsientidel teatatud pearinglusest. Pearinglus võib mõjutada mõnede patsientide autojuhtimise ja masinate käsitsemise võimet (vt lõik 4.8).
04.8 Kõrvaltoimed
Ohutusprofiili kokkuvõte
ISENTRESSi ohutusprofiil põhines kahe III faasi kliinilise uuringu kombineeritud ohutusandmetel, kus osalesid ravi saanud täiskasvanud patsiendid ja üks III faasi kliiniline uuring täiskasvanud patsientidel.ïlähen ravile. Kõige sagedamini teatatud kõrvaltoimed ravi ajal olid peavalu ja iiveldus, mida esines 5% või rohkem. Kõige sagedamini teatatud tõsine kõrvaltoime oli immuunsüsteemi taastamise sündroom.
Kahes randomiseeritud kliinilises uuringus kasutati kahes randomiseeritud kliinilises uuringus soovitatud annust 400 mg kaks korda ööpäevas koos optimeeritud taustraviga (OBT) 462 patsiendil, võrreldes 237 patsiendiga, kes said platseebot koos OBT-ga. Topeltpimedas ravi ajal oli kogu jälgimisperiood 708 patsiendiaastat ISENTRESS 400 mg kaks korda päevas saanud rühmas ja 244 patsiendiaastat platseeborühmas.
Varem ravi mittesaanud patsientidel kasutati mitmekeskuselises randomiseeritud topeltpimedas aktiivkontrollitud kliinilises uuringus 281 patsiendil soovitatavat annust 400 mg kaks korda ööpäevas koos fikseeritud annusega 200 mg (+) 245 mg emtritsitabiini 282 patsienti, kes võtsid efavirensi (EFV) 600 mg (enne magamaminekut) kombinatsioonis emtritsitabiini (+) tenofoviiriga. Topeltpimedas ravi ajal oli kogu jälgimisperiood 1104 patsiendiaastat rühmas, kes sai ISENTRESS 400 mg kaks korda ööpäevas, ja 1036 patsiendiaastat rühmas, kes sai enne magamaminekut 600 mg efavirensi.
Ravi saanud patsientide koondanalüüsis katkestati kõrvaltoimete tõttu ravi katkestamine 3,9% ISENTRESS + OBT-ravi saanud patsientidel ja 4,6% platseebot + OBT-d saanud patsientidel. Kõrvaltoimete tõttu katkestati ravi varem mittesaanud patsientidel 5,0% ISENTRESS + emtritsitabiin ( +) tenofoviiri saanud patsientidel ja 10,0% efavirensi + emtritsitabiini ( +) tenofoviiri saanud patsientidel.
Kõrvaltoimete tabel
Allpool on loetletud organsüsteemi klasside kaupa kõrvaltoimed, mida uurijad peavad põhjuslikult ISENTRESSiga seostatavaks (üksi või koos teiste ART -dega). Esinemissagedused on määratletud kui tavalised (≥ 1/100,
Valitud kõrvaltoimete kirjeldus
Varem kogenud ja varem ravi mittesaanud patsientidel, kes alustasid ISENTRESSi kasutamist koos teiste retroviirusevastaste ravimitega, on teatatud vähijuhtudest. Spetsiifiliste pahaloomuliste kasvajate tüübid ja esinemissagedused olid need, mida oodati raske immuunpuudulikkusega populatsioonis. Nendes uuringutes oli vähktõve tekkimise oht sarnane nii ISENTRESS kui ka võrdlusrühmades.
ISENTRESS-iga ravitud isikutel on täheldatud 2. – 4. Astme muutusi kreatiinkinaasi laboratoorsetes väärtustes. On teatatud müopaatiast ja rabdomüolüüsist. Kasutage ettevaatusega patsientidel, kellel on varem olnud müopaatia või rabdomüolüüs või kellel on eelsoodumus, sealhulgas muud nende seisunditega seotud ravimid (vt lõik 4.4).
Osteonekroosi juhtudest on teatatud peamiselt patsientidel, kellel on üldiselt teadaolevad riskitegurid, kaugelearenenud HIV-haigus või kes on pikka aega saanud kombineeritud retroviirusevastast ravi (CART). Esinemissagedus on teadmata (vt lõik 4.4).
HIV-nakkusega patsientidel, kellel on raske immuunpuudulikkus kombineeritud retroviirusevastase ravi (CART) alustamise ajal, võib tekkida põletikuline reaktsioon asümptomaatilistele või allesjäänud oportunistlikele infektsioonidele. Samuti on teatatud autoimmuunhäiretest (nt Gravesi tõbi): registreeritud aeg alguseni on siiski varieeruvam ja need sündmused võivad ilmneda isegi mitu kuud pärast ravi alustamist (vt lõik 4.4).
Kõigi järgmiste kliiniliste kõrvaltoimete puhul on esinenud vähemalt üks raske juhtum: suguelundite herpes, aneemia, immuunsüsteemi taastamise sündroom, depressioon, psüühikahäired, enesetapukatse, gastriit, hepatiit, neerupuudulikkus, juhuslik üleannustamine.
Kliinilistes uuringutes ravi saanud patsientidega täheldati löövet sõltumata põhjuslikkusest sagedamini ISENTRESSi ja darunaviiri sisaldavate raviskeemide puhul kui ISENTRESSi sisaldavate raviskeemide korral ilma darunaviiri või darunaviiri ilma ISENTRESSita. Kokkupuutega kohandatud lööbe esinemissagedus (kõikidest põhjuslikest põhjustest) oli vastavalt 10,9, 4,2 ja 3,8 100 patsiendiaasta kohta (PYR); ja ravimiga seotud lööbe korral vastavalt 2,4, 1,1 ja 2,3 100 patsiendiaasta kohta. Kliinilistes uuringutes täheldatud lööbed olid kerge kuni mõõduka raskusega ega põhjustanud haigusi. Ravi katkestamine (vt lõik 4.4).
Patsiendid, kes on samaaegselt nakatunud B- ja / või C-hepatiidi viirusega
III faasi uuringutes osalesid ravi saanud patsiendid (N = 114/699 või 16%; HBV = 6%, HCV = 9%, HBV + HCV = 1%) ja varem ravi mittesaanud patsiendid (N = 34/563 või 6%) ; HBV = 4%, HCV = 2%, HBV + HCV = 0,2%) koos aktiivse kroonilise (kuid mitte ägeda) B- ja / või C-hepatiidi kaasinfektsiooniga kaasati uuringusse, eeldusel, et maksafunktsiooni testid ei ületanud normi ülemist piiri rohkem kui 5 korda. Üldiselt oli ISENTRESSi ohutusprofiil B- ja / või C-hepatiidi viirusega samaaegselt nakatunud patsientidel sarnane B-hepatiidi ja / või või C-hepatiidi viiruse kaasinfektsioon, kuigi ASAT ja ALAT kõrvalekallete esinemissagedus oli mõlemas ravirühmas B-hepatiidi ja / või hepatiitiviirusega samaaegselt nakatunud alarühmas suhteliselt kõrgem. või suurem kui ASAT, ALT või bil laboratoorsed väärtused Üldist irubiini, mis viitab algtaseme halvenemisele, esines vastavalt 29%, 34% ja 13% ISENTRESS-iga ravitud kaasinfektsiooniga isikutest, võrreldes 11%, 10% ja 9% -ga kõigist teistest ISENTRESS-iga ravitud isikutest. 240 nädala jooksul esinesid varem ravi mittesaanud patsientidel II astme või suuremad laboratoorsed muutused ASAT, ALAT või üldbilirubiinis, mis viitavad astme halvenemisele võrreldes algtasemega, vastavalt 22%, 44% ja 17% patsientidest. ravitud ISENTRESSiga võrreldes 13%, 13% ja 5% kõigist teistest ISENTRESSiga ravitud isikutest.
Turuletulekujärgse järelevalve käigus tuvastati järgmised kõrvaltoimed, kuid neid ei teatatud ravimiga seotud III faasi randomiseeritud kontrollitud kliinilistes uuringutes (protokollid 018, 019 ja 021): trombotsütopeenia, enesetapumõtted, enesetapukäitumine (eriti patsientidel, kellel on varem esinenud psühhiaatrilisi haigusi), maksapuudulikkus, Stevensi Johnsoni sündroom, eosinofiilia ja süsteemsete sümptomitega ravimilööve (DRESS), rabdomüolüüs.
Lapsed
Lapsed ja noorukid vanuses 2 kuni 18 aastat
IMPAACT P1066 puhul on raltegraviiri koos teiste retroviirusevastaste ravimitega uuritud 126 HIV-1 nakkusega lapsel ja noorukil vanuses 2 kuni 18 aastat, kellel on retroviirusevastane ravi (vt lõigud 5.1 ja 5.2). 126 patsiendist 96 said soovitatud annuse ISENTRESSist.
Nendel 96 lapsel ja noorukil oli ravimiga seotud kõrvaltoimete esinemissagedus, tüüp ja raskus kuni 48. nädalani võrreldav täiskasvanutega.
Ühel patsiendil esines psühhomotoorne hüperaktiivsus, ebanormaalne käitumine ja unetus, 3. astme ravimiga seotud kliinilised kõrvaltoimed; ühel patsiendil oli raske 2. astme ravimiga seotud allergiline lööve.
Ühel patsiendil olid ravimiga seotud laboratoorsed kõrvalekalded, 4. astme AST ja 3. astme ALAT, mida peeti raskeks.
Imikud ja lapsed vanuses 4 nädalat kuni alla 2 aasta
IMPAACT P1066 uuringus uuriti raltegraviiri kombinatsioonis teiste retroviirusevastaste ravimitega ka 26 HIV-1 nakatunud imikul ja vähemalt 4-nädalase ja alla 2-aastase lapsega (vt lõigud 5.1 ja 5.2).
Nendel 26 imikul ja lapsel oli ravimiga seotud kõrvaltoimete sagedus, tüüp ja raskus kuni 48. nädalani võrreldav täiskasvanutega.
Ühel patsiendil tekkis raske 3. astme ravimiga seotud allergiline lööve, mille tõttu ravi katkestati.
Arvatavatest kõrvaltoimetest teatamine
Pärast ravimi müügiloa väljastamist tekkivatest arvatavatest kõrvaltoimetest teatamine on oluline, kuna see võimaldab pidevalt jälgida ravimi kasu ja riski suhet. Tervishoiutöötajatel palutakse teavitada kõigist võimalikest kõrvaltoimetest Itaalia Ravimiameti kaudu. , veebisait: http://www.agenziafarmaco.gov.it/it/responsabili.
04.9 Üleannustamine
ISENTRESSi üleannustamise ravi kohta spetsiifiline teave puudub.
Üleannustamise korral on mõistlik kasutada ühiseid toetavaid meetmeid, nt. eemaldage imendumata aine seedetraktist, jälgige patsienti kliiniliselt (sh EKG jälg) ja vajadusel alustage toetavat ravi. Tuleb märkida, et raltegraviir esineb kliiniliseks kasutamiseks kaaliumisoolana.Raltegraviiri dialüüsitavus ei ole teada.
05.0 FARMAKOLOOGILISED OMADUSED
05.1 Farmakodünaamilised omadused
Farmakoterapeutiline rühm: viirusevastased ained süsteemseks kasutamiseks, muud viirusevastased ained, ATC -kood: J05AX08.
Toimemehhanism
Raltegraviir on selle toime inhibiitor ahela ülekanne integraas on aktiivne inimese immuunpuudulikkuse viiruse (HIV-1) vastu. Raltegraviir pärsib viiruse replikatsiooniks vajaliku HIV -i kodeeritud ensüümi integraasi katalüütilist aktiivsust. Integraasi pärssimine takistab HIV -genoomi kovalentset sisestamist või integreerumist peremeesraku genoomi. HIV, mis ei suuda integreeruda, ei saa esile kutsuda uute nakkushaiguste teket viirusosakesed, seetõttu takistab integratsiooni pärssimine viirusnakkuse levikut.
Viirusevastane toime in vitro
Raltegraviir kontsentratsioonis 31 ± 20 nM põhjustas HIV-1 replikatsiooni 95% -lise inhibeerimise (IC95) (võrreldes viirusega nakatunud, ravimata kultuuriga) inimese T-lümfoidrakkude kultuurides, mis olid nakatunud kohandatud HIV rakuliini H9IIIB variandiga -1. Lisaks inhibeeris raltegraviir viiruse replikatsiooni kultiveeritud mitogeeni aktiveeritud inimese perifeerse vere mononukleaarsetes rakkudes, mis olid nakatunud mitmete esmaste HIV-1 kliiniliste isolaatidega, sealhulgas isolaadid viiest mitte-alatüübist. B ja isolaadid, mis olid resistentsed pöördtranskriptaasi inhibiitorite ja proteaasi inhibiitorite suhtes. Infektsiooni ühe tsükli testis pärssis raltegraviir 23 HIV isolaadi nakatumist, mis esindasid 5 mitte-B alatüüpi ja 5 ringlevat rekombinantset vormi, mille IC50 oli varieeruv 5 ... 12 nM.
Vastupidavus
Enamikul raltegraviirile reageerimata patsientidest eraldatud viirustel oli raltegraviiri suhtes kõrge resistentsus, viidates kahe või enama mutatsiooni esinemisele. Enamikul oli võtmemutatsioon aminohappel 155 (N155 modifitseeritud H -ks), aminohappel 148 (Q148 modifitseeritud H -ks, K -ks või R -ks) või aminohappes 143 (Y143 modifitseeritud H -ks, C -ks või R -ks) koos ühe või mitme täiendava mutatsiooniga integraasi mutatsioonid (nt L74M, E92Q, T97A, E138A / K, G140A / S, V151I, G163R, S230R). Põhimutatsioonid vähendavad viiruse vastuvõtlikkust raltegraviirile ja muude mutatsioonide lisamine vähendab veelgi raltegraviiri tundlikkust. Tegurid, mis vähendasid resistentsuse tekkimise tõenäosust, olid madalam algviiruse koormus ja teiste aktiivsete retroviirusevastaste ainete kasutamine. Mutatsioonid, mis põhjustavad resistentsust raltegraviiri suhtes, annavad tavaliselt resistentsuse ka aktiivsuse inhibiitorile ahela ülekanne Aminohappe 143 mutatsioonid annavad suurema resistentsuse raltegraviiri suhtes kui elvitegraviir ja E92Q mutatsioon annab suurema resistentsuse elvitegraviiri suhtes kui raltegraviir. Viirustel, millel on aminohappe 148 mutatsioon koos ühe või mitme mutatsiooniga, mis põhjustavad resistentsuse raltegraviiri suhtes, võib olla ka kliiniliselt oluline resistentsus dolutegraviiri suhtes.
Kliiniline kogemus
Tõendid ISENTRESSi efektiivsuse kohta põhinesid kahe 96-nädalase randomiseeritud topeltpimedas platseebokontrollitud kliinilise uuringu (BENCHMRK 1 ja BENCHMRK 2, protokollid 018 ja 019) andmete analüüsil HIV-1 retroviirusevastase raviga nakatunud täiskasvanud patsientidel. 240-nädalase randomiseeritud topeltpimedas aktiivkontrollitud uuringu (STARTMRK, protokoll 021) kogemuste ja andmete analüüs, milles osalesid HIV-1 nakatunud täiskasvanud patsiendid, kes ei olnud varem saanud retroviirusevastast ravi.
Tõhusus
Ravi kogemusega täiskasvanud patsiendid
ISENTRESS 400 mg kaks korda päevas ohutust ja retroviirusevastast toimet võrreldes platseeboga kombinatsioonis optimeeritud taustraviga (OBT) hinnati BENCHMRK 1 ja BENCHMRK 2 (multitsentrilised, randomiseeritud, topeltpimedad, platseebokontrollitud uuringud) abil HIV-nakatunud patsientidel. 16 -aastased või vanemad patsiendid, kellel on dokumenteeritud resistentsus vähemalt ühe ravimi suhtes kõigist kolmest retroviirusevastase ravi klassist (NRTI, NNRTI, PI). Enne randomiseerimist määras teadlane OBT ravi, samuti genotüübi ja fenotüübi viiruse resistentsuse testide algtasemel.
Patsientide demograafilised andmed (sugu, vanus ja rass) ja algtaseme näitajad olid võrreldavad kahe ISENTRESS 400 mg kaks korda ööpäevas ja platseebot saanud rühma vahel. Patsientidel oli eelnev kokkupuude keskmiselt 12 retroviirusevastase raviga, keskmiselt 10 aastat. OBT -s kasutati keskmiselt 4 ART -d.
Analüüsi tulemused 48 nädala ja 96 nädala pärast
Tabelis 2 on näidatud patsientide püsivad tulemused (48. ja 96. nädalal), keda raviti ISENTRESSi soovitatud annusega 400 mg kaks korda ööpäevas.
Tabel 2
Efektiivsuse tulemused 48. ja 96. nädalal
† Ebaõnnestumist loetakse ebaõnnestunuks: patsiendid, kes lõpetasid ravi enneaegselt, registreeriti hiljem ebaõnnestununa. On teatatud patsientide protsendist, kes reageerisid ravile 95% usaldusintervalliga.
Progn Prognoosiliste tegurite analüüsis kasutati lähenemist viroloogilise ebaõnnestumise korral kanna edasi algtaseme ülekandeprotsentide puhul.
§ Genotüüpse tundlikkuse skoor (GSS) määratleti kui suukaudsete ART -de koguarv optimeeritud taustteraapias (OBT), mille suhtes "patsiendi viirusisolaat näitas genotüübilise resistentsuse testi põhjal genotüüpilist tundlikkust. L" enfuvirtiidi kasutamine OBT -seadetes enfuvirtiidi mittesaanud patsientidel loeti aktiivseks OBT -ravimiks. Sarnaselt loeti darunaviiri kasutamine OBT tingimustes varem darunaviiri mittesaanud patsientidel aktiivseks OBT -ravimiks.
Raltegraviir sai HIV RNA viroloogilised vastused (kasutades meetodit Not Completed = Failure)
Üleminek raltegraviirile
SWITCHMRK uuringutes 1 ja 2 (protokollid 032 ja 033) hinnati HIV-nakkusega patsiente, kes said supressiivset ravi (HIV RNA sõelumine; stabiilne raviskeem> 3 kuud) koos lopinaviiriga 200 mg (+) ritonaviiri 50 mg 2 tabletti kaks korda päevas pluss vähemalt 2 pöördnukleosiidi transkriptaasi inhibiitorid ja randomiseeritud 1: 1, et jätkata lopinaviiri (+) ritonaviiri 2 tabletiga kaks korda päevas (vastavalt n = 174 ja n = 178) või asendada lopinaviir (+) ritonaviir 400 mg raltegraviiriga kaks korda päevas (n = 174 ja n = 176). Patsiente, kellel on varem esinenud viroloogilist ebaõnnestumist, ei välistatud ja varasemate retroviirusevastaste ravimite arv ei olnud piiratud.
Need uuringud viidi lõpule pärast esmast efektiivsusanalüüsi 24. nädalal, kuna need ei näidanud raltegraviiri mittealamatust lopinaviiri (+) ritonaviiriga. Mõlemas 24. nädala uuringus püsis HIV RNA supressioon alla 50 koopia / ml 84,4% raltegraviiri rühma patsientidest võrreldes 90,6% -ga lopinaviiri (+) ritonaviiri rühma patsientidest (kasutades lähenemisviisi Not Completed = Failure). Raltegraviiri ja kahe teise toimeaine manustamise vajaduse kohta vt lõik 4.4.
Ravi mittesaanud täiskasvanud patsiendid
STARTMRK (mitmekeskuseline, randomiseeritud, topeltpime, aktiivselt kontrollitud uuring) hindas ISENTRESS 400 mg kaks korda ööpäevas võetud ohutusprofiili ja retroviirusevastast toimet võrreldes raviga 600 mg efavirensiga enne magamaminekut kombinatsioonis emtritsitabiini (+) tenofoviiriga. varem ravi mittesaanud HIV-nakkusega patsiendid, kelle HIV RNA oli> 5000 koopiat / ml. Randomiseerimine kihistati HIV RNA tasemega (≤50 000 koopiat / ml ja> 50 000 koopiat / ml) ja B- või C-hepatiidi testiga (positiivne või negatiivne).
Patsientide demograafilised andmed (sugu, vanus ja rass) ja algtaseme näitajad olid võrreldavad ISENTRESS 400 mg kaks korda päevas rühmas ja 600 mg efavirensi enne magamaminekut.
Analüüsi tulemused 48 nädala ja 240 nädala pärast
Võrreldes esmase efektiivsuse tulemusnäitajaga, HIV -RNA väärtuste saavutanud patsientide osakaal (%)
Tabel 3
Efektiivsuse tulemused 48. ja 240. nädalal
† Ebaõnnestumist loetakse ebaõnnestunuks: Patsiente, kes lõpetasid ravi enneaegselt, loeti ebaõnnestunuks. On teatatud patsientide protsendist, kes reageerisid ravile 95% usaldusintervalliga.
Progn Prognoosiliste tegurite analüüsis kasutati lähenemist viroloogilise ebaõnnestumise korral kanna edasi algtaseme ülekandeprotsentide puhul.
Märkused: Analüüs põhineb kõigil olemasolevatel andmetel.
ISENTRESSi ja efavirensi manustati koos emtritsitabiini (+) tenofoviiriga.
Lapsed
Lapsed ja noorukid vanuses 2 kuni 18 aastat
IMPAACT P1066 on mitmekeskuseline avatud I / II faasi uuring, milles hinnatakse raltegraviiri farmakokineetilist profiili, ohutust, taluvust ja efektiivsust HIV-nakkusega lastel. Sellesse uuringusse kaasati 126 last ja noorukit vanuses 2 kuni 18 aastat. ravikogemus. Patsiendid kihistati vanuse järgi, kaasates esmalt noorukid ja seejärel nooremad lapsed. Patsiendid said kas 400 mg tabletivormi (6 ... 18 -aastased) või närimistabletivormi (2 kuni alla 12 -aastased) Raltegraviiri manustati optimeeritud taustrežiimiga.
Esialgne etapp annuse leidmine see hõlmas intensiivset farmakokineetilist hindamist. Annuse valik põhines raltegraviiri plasmakontsentratsiooni ja minimaalse kontsentratsiooni saavutamisel, mis oli sarnane täiskasvanutega, ning vastuvõetava lühiajalise ohutusprofiiliga. Pärast annuse valimist kaasati täiendavaid patsiente ohutuse, taluvuse ja efektiivsuse pikaajaliseks hindamiseks. 126 patsienti, 96 said ISENTRESSi soovitatud annuse (vt lõik 4.2).
Tabel 4
IMPAACTi uuringu P1066 (2 ... 18 -aastased) algtaseme omadused ja efektiivsuse tulemused 24. ja 48. nädalal
Imikud ja lapsed vanuses 4 nädalat kuni alla 2 aasta
IMPAACT P1066 uuringus osalesid HIV-nakkusega imikud ja vähemalt 4-nädalased kuni alla 2-aastased lapsed, keda varem raviti profülaktilise retroviirusevastase raviga, et vältida emalt lapsele ülekandumist (PMTCT) ja / või kombineeritud retroviirusevastast ravi. Raltegraviiri manustati suukaudse suspensiooni graanulite kujul, sõltumata toidutarbimisest, koos optimeeritud taustraviga, mis sisaldas lopinaviiri ja ritonaviiri kahel kolmandikul patsientidest.
Tabel 5
Algtaseme omadused ja efektiivsuse tulemused IMPAACT P1066 24. ja 48. nädalal (4 nädalat kuni alla 2 aasta)
* Ühel patsiendil oli asendis 155 mutatsioon.
Euroopa Ravimiamet on edasi lükanud kohustuse esitada ISENTRESSiga läbi viidud uuringute tulemused laste ühe või mitme alarühma kohta inimese immuunpuudulikkuse viirusinfektsiooni korral (teavet laste kasutamise kohta vt lõik 4.2).
05.2 Farmakokineetilised omadused
Imendumine
Raltegraviir imendub kiiresti, Tmax on ligikaudu 3 tundi pärast annuse manustamist, nagu on näidatud tervetel vabatahtlikel, kes on võtnud tühja kõhuga raltegraviiri ühekordse suukaudse annuse. Raltegraviiri AUC ja Cmax suurendavad annust proportsionaalselt ühe perioodi jooksul vahemik annus 100 mg kuni 1600 mg. C12 h suureneb proportsionaalselt annusega vahemikus a vahemik annust vahemikus 100 mg kuni 800 mg ja suureneb veidi vähem kui annusega proportsionaalne suurendamine annusevahemikus 100 mg kuni 1600 mg.
Kaks korda päevas manustatava ravimvormi korral saavutatakse farmakokineetika tasakaalu seisund kiiresti, ligikaudu esimese 2 ravipäeva jooksul. AUC ja Cmax kuhjuvad vähe või üldse mitte, samas kui C12 h on kumulatsioon väike.Raltegraviiri absoluutne biosaadavus ei ole kindlaks tehtud.
ISENTRESSi võib võtta koos toiduga või ilma. Efektiivsuse ja ohutuse pilootuuringutes HIV -positiivsetel patsientidel manustati raltegraviiri koos toiduga või ilma. Raltegraviiri mitme annuse manustamine pärast mõõduka rasvasisaldusega einet ei muutnud AUC -d kliiniliselt olulisel määral, 13% suurenes tühja kõhuga võrreldes. Raltegraviiri C12 h oli 66% kõrgem ja Cmax 5% kõrgem pärast mõõduka rasvasisaldusega sööki kui tühja kõhuga. Raltegraviiri manustamine pärast rasvarikast sööki suurendas AUC ja Cmax ligikaudu 2 korda ja suurendas C12 h 4,1 korda. Raltegraviiri manustamine pärast madala rasvasisaldusega sööki vähendas AUC ja Cmax vastavalt 46% ja 52%; C12h jäi praktiliselt muutumatuks. Näib, et toit suurendab tühja kõhuga võrreldes farmakokineetilist varieeruvust.
Üldiselt täheldati raltegraviiri farmakokineetikas märkimisväärset varieeruvust. BENCHMRK 1 ja 2 täheldatud C12 h puhul on üksikisikute varieeruvuse variatsioonikordaja (CV) 212%, samas kui indiviidisisese varieeruvuse CV on 122%.Varieeruvuse allikad võivad hõlmata erinevusi toidu ja ravimite samaaegsel tarbimisel.
Levitamine
Raltegraviir seondub ligikaudu 83% ulatuses inimese plasmavalkudega vahemik kontsentratsioon 2 kuni 10 mcM.
Raltegraviir läbis rottidel kergesti platsenta, kuid ei tunginud ajusse tuvastatavates kogustes.
Kahes uuringus HIV-1 nakatunud patsientidega, kes said 400 mg raltegraviiri kaks korda päevas, tuvastati raltegraviir hõlpsalt tserebrospinaalvedelikus. Esimeses uuringus (n = 18) oli CSF -i keskmine kontsentratsioon 5,8% (vahemik 1 kuni 53,5%) plasmakontsentratsioonist. Teises uuringus (n = 16) oli CSF -i keskmine kontsentratsioon 3% (vahemik 1 kuni 61%) plasmakontsentratsioonist. Need keskmised proportsioonid on ligikaudu 3 ... 6 korda madalamad kui raltegraviiri vaba fraktsioon plasmas.
Biotransformatsioon ja eritumine
Raltegraviiri näiv terminaalne poolväärtusaeg on ligikaudu 9 tundi lühema faasiga? Poolväärtusaeg (ligikaudu 1 tund) moodustab suurema osa AUC-st. Pärast radioaktiivselt märgistatud raltegraviiri suukaudse annuse manustamist on ligikaudu 51% ja 32% annus eritus vastavalt väljaheitega ja uriiniga. Väljaheites oli ainult raltegraviiri, millest enamik pärineb tõenäoliselt sapiga erituva raltegraviir-glükuroniidi hüdrolüüsist, nagu on täheldatud prekliinilistes uuringutes. Kaks komponenti, raltegraviir ja raltegraviir-glükuroniid, tuvastati uriinis vastavalt ligikaudu 9% ja 23% annusest. Peamine tsirkuleeriv üksus oli raltegraviir ja see moodustas umbes 70% kogu radioaktiivsusest; ülejäänud plasmas tuvastatud radioaktiivsust esindas raltegraviir-glükuroniid. Uuringud, milles kasutati keemiliste inhibiitorite ja cDNA-ga ekspresseeritud UDP-glükuronosüültransferaasi (UGT) selektiivseid isovorme, näitavad, et UGT1A1 on peamine raltegraviir-glükuroniidi moodustumise eest vastutav ensüüm. See näitab, et raltegraviiri kliirensi esmane mehhanism inimestel on UGT1A1-vahendatud glükuronidatsioon .
UGT1A1 polümorfism
Võrreldes 30 katsealust, kellel oli * 28 / * 28 genotüüp, ja 27 metsiktüüpi genotüübiga isikut, oli AUC geomeetriliste keskmiste suhe (90% CI) 1,41 (0,96–2,09) ja geomeetriliste keskmiste suhe C12 h 1,91 (1,43-2,55). UGT1A1 aktiivsusega isikutel ei peeta annuse kohandamist geneetilise polümorfismi tõttu vajalikuks.
Spetsiaalsed populatsioonid
Lapsed
Preparaatide võrdlusuuringu põhjal tervetel täiskasvanud vabatahtlikel on närimistabletil ja suukaudse suspensiooni graanulitel suurem suukaudne biosaadavus kui 400 mg tabletil. Selles uuringus põhjustas närimistableti manustamine koos suure rasvasisaldusega toiduga AUC keskmiselt 6%, Cmax vähenes 62% ja C12h suurenes võrreldes tühja kõhuga manustamisega. Närimistableti manustamine koos rasvarikka einega ei mõjuta raltegraviiri farmakokineetikat kliiniliselt olulisel viisil ja närimistableti võib manustada olenemata söögist. Toidu mõju suukaudse suspensiooni preparaadi graanulitele ei ole uuritud.
Tabelis 6 on toodud 400 mg tableti, närimistableti ja suukaudse suspensiooni graanulite farmakokineetilised parameetrid kehakaalu alusel.
Tabel 6
IMPAACT P1066 raltegraviriini farmakokineetilised parameetrid pärast lõigus 4.2 loetletud annuste manustamist
Raltegraviiri farmakokineetikat alla 4 nädala vanustel imikutel ei ole kindlaks tehtud.
Eakad kodanikud
Vanusel ei olnud kliiniliselt olulist mõju raltegraviiri farmakokineetikale vahemik vanusest (19–71 aastat, piiratud arv katsealuseid üle 65 -aastased).
Sugu, rass ja KMI
Täiskasvanutel ei leitud soost, rassist või kehamassiindeksist (KMI) tingitud kliiniliselt olulisi farmakokineetilisi erinevusi.
Neerukahjustus
Muutumatu ravimi neerukliirens moodustab väikese osa eliminatsiooniteest. Täiskasvanutel ei esinenud kliiniliselt olulisi erinevusi raske neerukahjustusega patsientide ja tervete isikute farmakokineetikas (vt lõik 4.2). Kuna ei ole teada, mil määral saab raltegraviiri dialüüsida, tuleb enne dialüüsi seanssi vältida.
Maksakahjustus
Raltegraviir eritub maksas peamiselt glükuronisatsiooni teel. Täiskasvanutel ei esinenud kliiniliselt olulisi erinevusi mõõduka maksakahjustusega patsientide ja tervete isikute farmakokineetikas. Raske maksakahjustuse mõju raltegraviiri farmakokineetikale ei ole uuritud (vt lõigud 4.2 ja 4.4).
05.3 Prekliinilised ohutusandmed
Mittekliinilised toksikoloogilised uuringud, sealhulgas konventsionaalsed farmakoloogilise ohutuse, korduvtoksilisuse, genotoksilisuse, embrüo-loote toksilisuse ja alaealiste toksilisuse uuringud raltegraviiriga, viidi läbi hiirtel, rottidel, koertel ja küülikutel. Mõju, kui kokkupuute tase ületab piisavalt kliinilist ekspositsiooni, ei viita inimesele erilisele ohule.
Mutageensus
(Amesi) mikroobide mutageneesi testides ei leitud tõendeid mutageensuse ja genotoksilisuse kohta. in vitro, aluselise elueerimise testides in vitro DNA lagundamiseks ja kromosomaalsete aberratsioonide uuringutes in vitro Ja in vivo.
Kantserogeensus
Raltegraviiri kartsinogeensusuuring hiirtel ei näidanud kantserogeenset toimet. Suurimate annuste korral, 400 mg / kg / päevas naistel ja 250 mg / kg / päevas isastel, oli süsteemne ekspositsioon sarnane kliinilise annusega 400 mg kaks korda ööpäevas. Rottidel tuvastati need. Kasvajad (lame rakuline kartsinoom) nina / ninaneelu annustes 300 ja 600 mg / kg / päevas naistel ja 300 mg / kg / päevas meestel. Need kasvajad võivad olla tingitud ravimi sadestumisest ja / või aspiratsioonist limaskesta tasemele nina / ninaneelu membraan sondiannuse manustamisel ja sellele järgnev krooniline ärritus ja põletik; Süsteemne kokkupuude NOAEL -iga oli sarnane kliinilise annusega 400 mg kaks korda ööpäevas. Tavalised genotoksilisuse uuringud mutageensuse ja klastogeensuse hindamiseks olid negatiivsed.
Embrüo-loote toksilisus
Embrüo-loote toksilisuse uuringutes rottidel ja küülikutel ei olnud raltegraviir teratogeenne. Emade vastsündinutel rottidel, kelle raltegraviiri ekspositsioon oli ligikaudu 4,4 korda suurem kui inimesel 400 mg kaks korda ööpäevas, täheldati AUC0-24 tunni põhjal kerget ribide arvu suurenemist. Arengut mõjutavaid toimeid ei täheldatud, kui ekspositsioon oli 3,4 korda suurem kui inimesel, kellele manustati 400 mg kaks korda ööpäevas, arvutades AUC0-24 h (vt lõik 4.6). Sarnaseid andmeid ei täheldatud küülikutel.
06.0 FARMATSEUTILINE TEAVE
06.1 Abiained
Tableti sees
• Mikrokristalne tselluloos
• Laktoosmonohüdraat
• Veevaba kahealuseline kaltsiumfosfaat
• Hüpromelloos 2208
• Poloksameer 407
• Naatriumstearüülfumaraat
• magneesiumstearaat
Tableti kate
• polüvinüülalkohol
• Titaan dioksiid
• Polüetüleenglükool 3350
• Talk
• Punane raudoksiid
• Must raudoksiid
06.2 Sobimatus
Ei ole asjakohane.
06.3 Kehtivusaeg
30 kuud
06.4 Säilitamise eritingimused
See ravim ei vaja säilitamisel eritingimusi.
06.5 Vahetu pakendi olemus ja pakendi sisu
Lastekindla polüpropüleenist korgiga suure tihedusega polüetüleenist (HDPE) pudelid.
Saadaval on kaks pakendi suurust: 1 pudel 60 tabletiga ja 3 pudelit 60 tabletiga.
Kõik pakendi suurused ei pruugi olla müügil.
06.6 Kasutamis- ja käsitsemisjuhised
Hävitamiseks ei ole erijuhiseid.
07.0 MÜÜGILOA HOIDJA
Merck Sharp & Dohme Limited
Hertford Road, Hoddesdon
Hertfordshire EN11 9BU
Ühendkuningriik
08.0 MÜÜGILOA NUMBER
EL/1/07/436/001
EL/1/07/436/002
038312017
038312029
09.0 MÜÜGILOA VÕI UUENDAMISE KUUPÄEV
Müügiloa esmase väljastamise kuupäev: 20. detsember 2007
Viimase uuendamise kuupäev: 14. mai 2014
10.0 TEKSTI LÄBIVAATAMISE KUUPÄEV
14. november 2016