Toimeained: trimetoprim, sulfametoksasool
Bactrim 160 mg + 800 mg lahustuvad tabletid
Bactrimi pakendi infolehed on saadaval järgmistes pakendisuurustes:- Bactrim 160 mg + 800 mg lahustuvad tabletid
- Bactrim 160 mg + 800 mg tabletid, Bactrim 80 mg / 5 ml + 400 mg / 5 ml suukaudne suspensioon
- Bactrim 80 mg + 400 mg tabletid
Bactrim 40 mg / 5 ml + 200 mg / 5 ml suukaudne suspensioon
Miks Bactrimit kasutatakse? Milleks see mõeldud on?
Bactrim kuulub bakteritsiidsete keemiaravi ravimite kategooriasse.
Näidustused
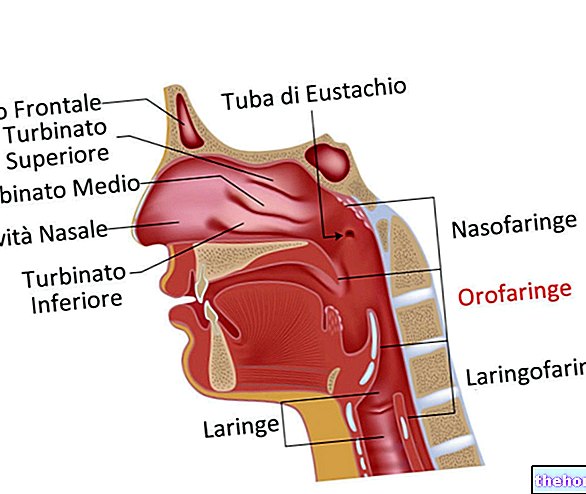
Hingamisteede infektsioonid: sinusiit, keskkõrvapõletik, äge bronhiit, kopsupõletik (ka Pneumocystis carinii tõttu), ägenemised kroonilise bronhiidi või bronhiektaasi korral.
Neeru- ja kuseteede infektsioonid: püeliit, tsüstiit, prostatiit, uretriit, krooniliste kuseteede infektsioonide ägenemised.
Suguelundite infektsioonid sealhulgas gonokoki uretriit.
Seedesüsteemi infektsioonid: Shigella, Salmonella typhi ja paratyphi nakkused ja muud enteriitid tundlikest mikroobidest
Vastunäidustused Kui Bactrim'i ei tohi kasutada
Teadaolev ülitundlikkus sulfoonamiidide ja / või trimetoprimi või ravimi ükskõik millise abiaine suhtes.
Raske neerupuudulikkus koos asoteemiaga; maksa parenhüümi rasked kahjustused; vere düskraasia.
Alla kahe kuu vanused lapsed.
Raseduse ja imetamise ajal, et vältida ohtu, et ebaõnnestumine ravimi eemaldamisel ema kehast ja vastavalt piima sattumine võib põhjustada vastsündinute ikterust.
Glükoos-6-fosfaatdehüdrogenaasi puudulikkus
Bactrim'i ei tohi manustada koos dofetiliidiga (vt lõik "Koostoimed").
Ettevaatusabinõud kasutamisel Mida on vaja teada enne Bactrim'i võtmist
Raseduse ajal, väga varases lapsepõlves ja eakatel patsientidel tuleb ravimit kasutada ainult tõelise vajaduse korral ja arsti otsese järelevalve all.
Bactrimi kasutamisel on teatatud eluohtlikest nahalöövetest (Stevensi-Johnsoni sündroom, toksiline epidermaalne nekrolüüs) DRESS (ravimilööve koos eosinofiilia ja süsteemsete sümptomitega); need tekivad esialgu ümmarguste punaste laikude või ümmarguste laikudena, mis sageli kaasnevad villid pagasiruumi keskosas.
Täiendavad märgid on suu, kurgu, nina, suguelundite haavandid ja konjunktiviit (punased ja tursed silmad).
Nende eluohtlike löövetega kaasnevad sageli gripilaadsed sümptomid. Lööve võib areneda laialt levinud villide ja naha koorumisega.
Suurim tõsiste nahareaktsioonide oht esineb esimestel ravinädalatel.
Kui tekib Stevensi-Johnsoni sündroom või toksiline epidermaalne nekrolüüs, ei tohi Bactrim’i koos Bactrim’iga kasutada.
Kui teil tekib nahalööve või need nahasümptomid, lõpetage Bactrim'i võtmine, pöörduge kiiresti arsti poole ja öelge neile, et te võtate seda ravimit.
Eriti ettevaatlik tuleb olla neeru- või maksapuudulikkusega ning folaadi puudulikkusega või raske allergiaga patsientide ravimisel.
Ravi ajal, eriti pikaajalisel perioodil, on soovitatav perioodiliselt kontrollida maksa- ja neerufunktsiooni ning vereanalüüse.
Toodet ei tohi kasutada A-rühma ß-hemolüütilise streptokoki põhjustatud infektsioonide (farüngiit jt) korral.
Rasedus ja imetamine
Bactrim on raseduse ja rinnaga toitmise ajal vastunäidustatud.
Koostoimed Millised ravimid või toidud võivad Bactrimi toimet muuta
Teatage oma arstile või apteekrile, kui te kasutate või olete hiljuti kasutanud mingeid muid ravimeid, isegi ilma retseptita.
Kaudseid antikoagulante saavatel patsientidel on teatatud Bactrim'i põhjustatud protrombiiniaja pikenemisest. Seetõttu tuleb seda koostoimet meeles pidada, kui Bactrim määratakse patsientidele, kes saavad juba antikoagulantravi; lisaks tuleb uuesti kontrollida vere hüübimisnäitajaid.
Pärast trimetoprim-sulfametoksasooli ja amantadiini samaaegset kasutamist on teatatud toksilisest deliiriumist.
On tõendeid selle kohta, et trimetoprim võib neerutranspordi süsteemi pärssimise tõttu interakteeruda dofetiliidiga. Trimetoprim 160 mg kombinatsioonis 800 mg sulfametoksasooliga kaks korda ööpäevas samaaegselt 500 mg dofetiliidiga kaks korda päevas nelja päeva jooksul suurendas kontsentratsiooni-aja kõvera (AUC) alune pindala ja maksimaalse kontsentratsiooni (Cmax) suurenemine 93% võrra. Dofetiliid võib põhjustada tõsiseid vatsakeste arütmiaid, mis on seotud QT -intervalli pikenemisega, sealhulgas torsades de pointes, mis on otseselt seotud dofetiliidi plasmakontsentratsiooniga. Dofetiliidi ja trimetoprimi samaaegne manustamine on vastunäidustatud.
Hoiatused Oluline on teada, et:
Löövete ilmnemisel tuleb ravi Bactrim'iga kohe lõpetada.
Võimalikud on asümptomaatilised muutused foolhappe metabolismis, kuigi need on pöörduvad foliinhappega.
Pikaajalise ravi ajal Bactrimiga on soovitatav regulaarselt kontrollida vere valemit ja uriini.
Annustamine ja kasutusviis Kuidas Bactrim'i kasutada: Annustamine
Täiskasvanud ja üle 12 -aastased lapsed:
Tavaline annus: 1 lahustuv tablett 2 korda päevas, hommikul ja õhtul pärast sööki.
Minimaalne annus ja annus pikaajalise ravi korral (üle 15 päeva): ½ lahustuvat tabletti 2 korda päevas.
Maksimaalne annus (eriti rasketel juhtudel): 1½ lahustuvat tabletti kaks korda päevas. Ägedate infektsioonide korral tuleb Bactrim 160 mg + 800 mg lahustuvaid tablette manustada vähemalt 5 päeva või seni, kuni patsient on 2 päeva jooksul sümptomitest vabanenud.
Lastel vanuses 2 kuud kuni 12 aastat on soovitatav kasutada siirupit vastavalt annusele, mis on märgitud vastava pakendi infolehel.
Kuidas kasutada: Tabletid lahustuvad või õigemini hajuvad kiiresti vees või muudes vesilahustes; sel viisil saadakse vastuvõetava maitsega ja kergesti joodav jook.
Üleannustamine Mida teha, kui olete Bactrim'i üleannustanud?
Teoreetiliselt on võimalik: kristallide ilmumine uriini, oliguuria või anuuria; iiveldus, oksendamine, kõhulahtisus, peavalu, pearinglus.
Mürgistuse korral tuleb sõltuvalt sümptomitest ette näha: maoloputus, piisav vedeliku tarbimine, et kiirendada neerude kaudu eritumist, hemodialüüs, verevalemi kontroll ja selle muutumise korral 6–12 mg folinaadi manustamine. jalgpallist.
Ravimi ülemäärase annuse juhusliku võtmise korral teavitage sellest kohe oma arsti või minge lähimasse haiglasse
Kõrvaltoimed Millised on Bactrimi kõrvaltoimed
Nagu kõik ravimid, võib ka see põhjustada kõrvaltoimeid, kuigi kõigil neid ei teki.
Kasutatakse järgmisi standardsageduskategooriaid: väga sage (≥ 1/10); sage (≥ 1/100 e
Trimetoprim -sulfametoksasooliga ravitud patsientide üldpopulatsioonis teatatud kõrvaltoimed
Infektsioonid ja infestatsioonid
Väga harv
On teatatud seeninfektsioonidest nagu kandidoos.
Vere ja lümfisüsteemi häired
Haruldane
Paljud täheldatud hematoloogilised muutused olid kerged, asümptomaatilised ja ravi katkestamisel pöörduvad. Kõige sagedamini täheldatud muutused olid leukopeenia, granulotsütopeenia ja trombotsütopeenia.
Väga harv
Võib esineda agranulotsütoos, aneemia (megaloblastne, hemolüütiline / autoimmuunne, aplastiline), pantsütopeenia, methemoglobineemia, eosinofiilia (seotud DRESSiga), hüpoprotrombineemia, folaatide metabolismi muutused.
Immuunsüsteemi häired
Väga harv
On teatatud ülitundlikkusreaktsioonidest. Nagu kõigi teiste ravimite puhul, võivad allergilised reaktsioonid, sealhulgas ristreaktsioonid, tekkida patsientidel, kes on ülitundlikud ühe komponendi suhtes: näiteks üldised naha- ja limaskestareaktsioonid, urtikaaria, eksfoliatiivne dermatiit, palavik, angioneurootiline ödeem, anafülaktoidsed reaktsioonid, seerumihaigus, DRESS (ravimilööve eosinofiilia ja süsteemsete sümptomitega), interstitsiaalne kopsupõletik.
On teatatud kopsuinfiltraatide juhtudest, näiteks eosinofiilse või allergilise alveoliidi korral. Need võivad ilmneda selliste sümptomitena nagu köha või hingamisraskused. Kui sellised sümptomid ilmnevad või süvenevad ootamatult, tuleb patsient uuesti läbi vaadata ja kaaluda Bactrim-ravi katkestamist. Lisaks on teatatud nodosa periarteriidi ja allergilise müokardiidi juhtudest.
Ainevahetus- ja toitumishäired
Väga harv
TM manustamine suurtes annustes, nagu Pneumocystis carinii kopsupõletiku korral, põhjustab paljudel patsientidel progresseeruvat, kuid pöörduvat seerumi kaaliumi kontsentratsiooni tõusu. Isegi soovitatud annuste korral võib TM põhjustada hüperkaleemiat, kui seda manustatakse patsientidele, kellel on kaaliumi metabolismi häire, neerupuudulikkus või keda ravitakse hüperkaleemiat põhjustavate ravimitega. Nendel patsientidel on soovitatav jälgida seerumi kaaliumisisaldust.
On teatatud hüponatreemia juhtudest. TM-SMZ-ga ravitud mitte-diabeediga patsientidel on tavaliselt teatatud hüpoglükeemia juhtudest, tavaliselt mõne päeva pärast. Eriti ohustatud on patsiendid, kellel on vähenenud neerufunktsioon, maksahaigus või alatoitumus või keda ravitakse suurte TM-SMZ annustega.
Psühhiaatrilised häired
Väga harv
Kirjeldatud on üksikuid hallutsinatsioonijuhte.
Närvisüsteemi häired
Väga harv
Neuropaatia (sealhulgas perifeerne neuriit ja paresteesia), uveiit. On teatatud aseptilisest meningiidist või meningeaalsele sarnastele sümptomitele, ataksiale, krampidele, tinnitusele, pearinglusele, peavalule, vaimsele depressioonile, unetusele ja asteeniale.
Seedetrakti häired
levinud
Iiveldus (koos oksendamisega või ilma)
Haruldane
Stomatiit, glossiit, kõhulahtisus
Väga harv
Kõhuvalu, pseudomembranoosne koliit. On teatatud ägeda pankreatiidi juhtudest; Paljud patsiendid kannatavad tõsiste haiguste, sealhulgas AIDSi all.
Maksa ja sapiteede häired
Väga harv
Kirjeldatud on transaminaaside ja bilirubiini taseme tõusu, hepatiiti, kolestaasi, maksanekroosi, sagenenud sapijuha sündroomi üksikuid juhtumeid, ikterust
Naha ja nahaaluskoe kahjustused
levinud
Kirjeldatud on mitmeid nahareaktsioone; need on tavaliselt kerged ja pärast ravi katkestamist kiiresti pöörduvad.
Väga harv
Nagu paljud teised sulfoonamiidi sisaldavad ravimid, on ka Bactrim seotud valgustundlikkusega. Teatatud on eluohtlikest nahalöövetest (Stevensi-Johnsoni sündroom, toksiline epidermaalne nekrolüüs), DRESSist (eosinofiilia ja süsteemsete sümptomitega ravimilööve) (vt lõik "Ettevaatusabinõud kasutamisel").
Lihas -skeleti, sidekoe ja luude kahjustused
Väga harv
On teatatud artralgia ja müalgia juhtudest ning üksikutest rabdomüolüüsi juhtudest.
Neerude ja kuseteede häired
Väga harv
On teatatud neerufunktsiooni kahjustuse juhtudest, interstitsiaalsest nefriidist, vere uurea lämmastiku (BUN) taseme tõusust, albuminuuriast, hematuuriast, kreatiniini taseme tõusust ja kristalluuriast. Sulfoonamiidid, sealhulgas Bactrim, võivad esile kutsuda diureesi suurenemist, eriti südameödeemiga patsientidel.
Üldised häired ja manustamiskoha reaktsioonid
Bactrim perfusiooni intravenoosne infusioon on aeg -ajalt põhjustanud kohalikke kõrvaltoimeid kerge kuni mõõduka veenivalu ja flebiidi kujul.
TM-SMZ ohutus HIV-positiivsetel patsientidel
Võimalike kõrvaltoimete spektri poolest on HIV-positiivne patsientide populatsioon sarnane üldpopulatsiooniga. Igal juhul võivad mõned kõrvaltoimed esineda sagedamini ja erineva kliinilise pildiga.
Need erinevused puudutavad järgmisi klasse:
Vere ja lümfisüsteemi häired
Väga tavaline
Leukopeenia, granulotsütopeenia ja trombotsütopeenia.
Ainevahetus- ja toitumishäired
Väga tavaline
Hüperkaleemia. Aeg -ajalt Hüponatreemia, hüpoglükeemia.
Seedetrakti häired
Väga tavaline
Anoreksia, iiveldus koos oksendamisega või ilma, kõhulahtisus. Maksa ja sapiteede häired Transaminaaside aktiivsuse tõus.
Naha ja nahaaluskoe kahjustused
Väga tavaline
Makulopapulaarne lööve, millega tavaliselt kaasneb sügelus.
Üldised häired ja manustamiskoha reaktsioonid
Väga tavaline
Palavik, millega tavaliselt kaasnevad makulopapulaarsed lööbed.
Pakendi infolehel olevate juhiste järgimine vähendab kõrvaltoimete riski. Kui ükskõik milline kõrvaltoimetest muutub tõsiseks või kui te märkate mõnda kõrvaltoimet, mida selles infolehes ei ole nimetatud, palun rääkige sellest oma arstile või apteekrile.
Aegumine ja säilitamine
Aegumine: vaadake pakendile trükitud aegumiskuupäeva. Kõlblikkusaeg viitab puutumata pakendis olevale tootele, mis on õigesti hoitud. Hoiatus: ärge kasutage ravimit pärast kõlblikkusaega, mis on märgitud pakendil
Ravimeid ei tohi ära visata kanalisatsiooni kaudu ega koos majapidamisprügiga. Küsige oma apteekrilt, kuidas visata ära ravimeid, mida te enam ei kasuta. See aitab kaitsta keskkonda.
Koostis
Bactrim 160 mg + 800 mg lahustuvad tabletid: üks lahustuv tablett sisaldab 800 mg sulfametoksasooli ja 160 mg trimetoprimi.
Abiained: mikrokristalne tselluloos, naatriumtärklisglükolaat, naatriumdioctüülsulfosuktsinaat, sahhariin, magneesiumstearaat, maisitärklis.
Ravimvorm ja pakend
Bactrim 160 mg + 800 mg lahustuvad tabletid: 16 lahustuvat tabletti.
Allika pakendi infoleht: AIFA (Itaalia ravimiamet). Sisu avaldati jaanuaris 2016. Esitatud teave ei pruugi olla ajakohane.
Kõige ajakohasemale versioonile juurdepääsu saamiseks on soovitatav külastada AIFA (Itaalia ravimiamet) veebisaiti. Vastutusest loobumine ja kasulik teave.
01.0 RAVIMPREPARAADI NIMETUS
BACTRIM
02.0 KVALITATIIVNE JA KVANTITATIIVNE KOOSTIS
Bactrim on seos sulfoonamiidi derivaadi, sulfametoksasooli (SMZ) ja diaminopürimidiinidest saadud kemoterapeutilise ravimi, trimetoprimi (TM) vahekorras 5: 1.
Bactrim 80 mg + 400 mg tabletid. Üks tablett sisaldab: sulfametoksasooli 400 mg, trimetoprim 80 mg.
Bactrim 160 mg + 800 mg tabletid. Üks tablett sisaldab: sulfametoksasooli 800 mg, trimetoprim 160 mg.
Bactrim 160 mg + 800 mg lahustuvad tabletid. Üks tablett sisaldab: sulfametoksasooli 800 mg, trimetoprim 160 mg.
Bactrim 40 mg / 5 ml + 200 mg / 5 ml suukaudne suspensioon. 100 ml sisaldab: sulfametoksasooli 4 g, trimetoprimi 0,8 g. 5 ml suukaudset suspensiooni (üks lusikas) sisaldab 200 mg SMZ ja 40 mg TM.
Bactrim 80 mg / 5 ml + 400 mg / 5 ml suukaudne suspensioon. 100 ml sisaldab: sulfametoksasooli 8 g, trimetoprimi 1,6 g. 5 ml suukaudset suspensiooni (üks lusikas) sisaldab 400 mg SMZ ja 80 mg TM.
Abiained vt lõik 6.1.
03.0 RAVIMVORM
Bactrim on saadaval tablettide, lahustuvate tablettide ja suukaudse suspensiooni kujul.
04.0 KLIINILINE TEAVE
04.1 Näidustused
Hingamisteede infektsioonid: sinusiit, keskkõrvapõletik, äge bronhiit, kopsupõletik (ka Pneumocystis carinii tõttu), ägenemised kroonilise bronhiidi või bronhiektaasi korral.
Neeru- ja kuseteede infektsioonid: püeliit, tsüstiit, prostatiit, uretriit, krooniliste kuseteede infektsioonide ägenemised.
Suguelundite infektsioonid, sealhulgas gonokokiline uretriit.
Seedesüsteemi infektsioonid: Shigella, Salmonella typhi ja paratyphi nakkused ja muud tundlike mikroobide enteriit.
04.2 Annustamine ja manustamisviis
Ägedate infektsioonide korral tuleb Bactrim'i manustada vähemalt 5 päeva või kuni patsient on 2 päeva jooksul sümptomitest vabanenud.
• Laste annus vastab ligikaudu 6 mg TM / kg päevas.
• Raskete infektsioonide korral tuleb annust suurendada 50%.
• Pikaajalise säilitusravi korral (üle 15 päeva) tuleks seda vähendada 50%.
Kuidas kasutada
Suukaudne suspensioon: enne kasutamist loksutada hoolikalt.
Bactrim 160 mg + 800 mg lahustuvad tabletid lahustuvad või õigemini lahustuvad kiiresti vees või muudes vesilahustes; sel viisil saadakse vastuvõetava maitsega ja kergesti joodav jook.
04.3 Vastunäidustused
Teadaolev ülitundlikkus sulfoonamiidide ja / või trimetoprimi või ravimi ükskõik millise abiaine suhtes. Raske neerupuudulikkus koos asoteemiaga; maksa parenhüümi rasked kahjustused; vere düskraasia.
Alla kahe kuu vanused lapsed.
Raseduse ja imetamise ajal, et vältida riski, et ravimi ebaõnnestumine ema kehast ja vastavalt piima sattumine võib põhjustada vastsündinute ikterust. Glükoos-6-fosfaatdehüdrogenaasi puudulikkus.
Bactrim'i ei tohi manustada koos dofetiliidiga (vt lõik 4.5).
04.4 Erihoiatused ja asjakohased ettevaatusabinõud kasutamisel
Raseduse ajal, väga varases lapsepõlves ja eakatel patsientidel tuleb ravimit kasutada ainult tõelise vajaduse korral ja arsti otsese järelevalve all.
Bactrimi kasutamisel on teatatud järgmistest eluohtlikest nahareaktsioonidest: Stevensi-Johnsoni sündroom (SJS) ja toksiline epidermaalne nekrolüüs (TEN), DRESS (ravimilööve koos eosinofiilia ja süsteemsete sümptomitega). Patsiente tuleb teavitada. Märgid ja sümptomid ja hoolikalt jälgida nahareaktsioone. Suurim risk SJS -i ja TEN -i tekkeks on esimestel ravinädalatel.
Kui tekivad SJS -i ja TEN -i sümptomid või nähud (nt progresseeruv nahalööve, millega sageli kaasnevad villid või limaskesta kahjustused), tuleb Bactrim -ravi katkestada.
SJS -i ja TEN -i juhtimise parimad tulemused saavutatakse varajase diagnoosimise ja ravi kohese katkestamisega mis tahes kahtlustatava ravimiga. Varajane katkestamine on seotud parema prognoosiga.
Kui patsiendil on Bactrim'i kasutamisel tekkinud SJS ja TEN, ei tohi Bactrimit sellel patsiendil enam kasutada.
Eriti ettevaatlik tuleb olla neeru- või maksapuudulikkusega ning folaadi puudulikkusega või raske allergiaga patsientide ravimisel.
Ravi ajal, eriti pikaajalisel perioodil, on soovitatav perioodiliselt kontrollida maksa- ja neerufunktsiooni ning vereanalüüse.
Toodet ei tohi kasutada A-rühma β-hemolüütilise streptokoki põhjustatud infektsioonide (farüngiit jt) korral.
Löövete ilmnemisel tuleb ravi Bactrim'iga kohe lõpetada.
Võimalikud on asümptomaatilised muutused foolhappe metabolismis, kuigi need on pöörduvad foliinhappega.
Pikaajalise ravi ajal Bactrimiga on soovitatav regulaarselt kontrollida vere valemit ja uriini.
Suukaudne suspensioon sisaldab sorbitooli: patsiendid, kellel on harvaesinev pärilik fruktoositalumatus, ei tohi seda ravimit võtta.
04.5 Koostoimed teiste ravimitega ja muud koostoimed
Kaudseid antikoagulante saavatel patsientidel on teatatud Bactrim'i põhjustatud protrombiiniaja pikenemisest. Seetõttu tuleb seda koostoimet meeles pidada, kui Bactrim määratakse patsientidele, kes saavad juba antikoagulantravi; lisaks tuleb uuesti kontrollida vere hüübimisnäitajaid.
Pärast TM-SMZ ja amantadiini samaaegset kasutamist on teatatud toksilisest deliiriumist.
On tõendeid selle kohta, et TM võib neerutranspordi süsteemi pärssimise tõttu interakteeruda dofetiliidiga. Trimetoprim 160 mg kombinatsioonis 800 mg sulfametoksasooliga kaks korda ööpäevas samaaegselt 500 mg dofetiliidiga kaks korda päevas, nelja päeva jooksul, suurendas kontsentratsiooni-aja kõvera (AUC) alune pindala ja maksimaalse kontsentratsiooni (Cmax) suurenemine 93% võrra. Dofetiliid võib põhjustada tõsiseid vatsakeste arütmiaid, mis on seotud QT -intervalli pikenemisega, sealhulgas torsades de pointes, mis on otseselt seotud dofetiliidi plasmakontsentratsiooniga. Dofetiliidi ja trimetoprimi samaaegne manustamine on vastunäidustatud.
04.6 Rasedus ja imetamine
Bactrim on vastunäidustatud raseduse ja imetamise ajal.
04.7 Mõju autojuhtimise ja masinate käsitsemise võimele
Ravimi mõju nendele võimetele ei ole teatatud ega oodata.
04.8 Kõrvaltoimed
Kasutatakse järgmisi standardsageduskategooriaid: väga sage (≥ 1/10); sage (≥ 1/100 e
TM-SMZ-ga ravitud patsientide üldpopulatsioonis teatatud kõrvaltoimed
Infektsioonid ja infestatsioonid
Väga harv: on teatatud seeninfektsioonidest nagu kandidoos.
Vere ja lümfisüsteemi häired
Haruldane: Paljud täheldatud hematoloogilised muutused olid kerged, asümptomaatilised ja ravi katkestamisel pöörduvad. Kõige sagedamini täheldatud muutused olid leukopeenia, granulotsütopeenia ja trombotsütopeenia.
Väga harv: võivad esineda agranulotsütoos, aneemia (megaloblastne, hemolüütiline / autoimmuunne, aplastiline), pantsütopeenia, methemoglobineemia, eosinofiilia (seotud DRESSiga), hüpoprotrombineemia, folaatide metabolismi muutused.
Immuunsüsteemi häired
Väga harv: on teatatud ülitundlikkusreaktsioonidest. Nagu kõigi teiste ravimite puhul, võivad allergilised reaktsioonid, sealhulgas ristreaktsioonid, tekkida patsientidel, kes on ülitundlikud ühe komponendi suhtes: näiteks üldised naha- ja limaskestareaktsioonid, urtikaaria, eksfoliatiivne dermatiit, palavik, angioneurootiline ödeem, anafülaktoidsed reaktsioonid, seerumihaigus, DRESS (ravimilööve eosinofiilia ja süsteemsete sümptomitega), interstitsiaalne kopsupõletik.
On teatatud kopsuinfiltraatide juhtudest, näiteks eosinofiilse või allergilise alveoliidi korral. Need võivad ilmneda selliste sümptomitena nagu köha või hingamisraskused. Kui sellised sümptomid ilmnevad või süvenevad ootamatult, tuleb patsient uuesti läbi vaadata ja kaaluda Bactrim-ravi katkestamist.
Lisaks on teatatud nodosa periarteriidi ja allergilise müokardiidi juhtudest.
Ainevahetus- ja toitumishäired
Väga harv: TM manustamine suurtes annustes, nagu Pneumocystis carinii kopsupõletiku korral, põhjustab paljudel patsientidel progresseeruvat, kuid pöörduvat seerumi kaaliumi kontsentratsiooni tõusu. Isegi soovitatud annuste korral võib TM põhjustada hüperkaleemiat, kui seda manustatakse patsientidele, kellel on kaaliumi metabolismi häire, neerupuudulikkus või keda ravitakse hüperkaleemiat põhjustavate ravimitega. Nendel patsientidel on soovitatav jälgida seerumi kaaliumisisaldust.
On teatatud hüponatreemia juhtudest. TM-SMZ-ga ravitud mitte-diabeediga patsientidel on tavaliselt teatatud hüpoglükeemia juhtudest, tavaliselt mõne päeva pärast. Eriti ohustatud on patsiendid, kellel on vähenenud neerufunktsioon, maksahaigus või alatoitumus või keda ravitakse suurte TM-SMZ annustega.
Psühhiaatrilised häired
Väga harv: on kirjeldatud üksikuid hallutsinatsioonijuhte.
Närvisüsteemi häired
Väga harv: neuropaatia (sh perifeerne neuriit ja paresteesia), uveiit. On teatatud aseptilisest meningiidist või meningeaalsele sarnastele sümptomitele, ataksiale, krampidele, tinnitusele, pearinglusele, peavalule, vaimsele depressioonile, unetusele ja asteeniale.
Seedetrakti häired
levinudiiveldus (koos oksendamisega või ilma)
Haruldane: stomatiit, glossiit, kõhulahtisus.
Väga harv: kõhuvalu, pseudomembranoosne koliit.
On teatatud ägeda pankreatiidi juhtudest; Paljud patsiendid kannatavad tõsiste haiguste, sealhulgas AIDSi all.
Maksa ja sapiteede häired
Väga harv: on kirjeldatud transaminaaside ja bilirubiini taseme tõusu, hepatiiti, kolestaasi, maksanekroosi, üksikuid haigestunud sapiteede sündroomi, ikterust.
Naha ja nahaaluskoe kahjustused
levinud: on kirjeldatud mitmeid nahareaktsioone; need on tavaliselt kerged ja pärast ravi katkestamist kiiresti pöörduvad.
Väga harv: nagu paljud teised sulfoonamiidi sisaldavad ravimid, on Bactrim olnud seotud valgustundlikkusega.
Teatatud on tõsistest naha kõrvaltoimetest, nagu Stevensi-Johnsoni sündroom (SJS) ja toksiline epidermaalne nekrolüüs (TEN), DRESS (ravimilööve koos eosinofiilia ja süsteemsete sümptomitega) (vt lõik 4.4).
Multiformne erüteem, purpur ja Henoch-Schoenleini purpur.
Lihas -skeleti, sidekoe ja luude kahjustused
Väga harv: On teatatud artralgia ja müalgia juhtudest ning üksikutest rabdomüolüüsi juhtudest.
Neerude ja kuseteede häired
Väga harv: On teatatud neerufunktsiooni kahjustuse juhtudest, interstitsiaalsest nefriidist, kõrgenenud vere uurea lämmastikust (BUN), albuminuuriast, hematuuriast, kreatiniini taseme tõusust ja kristalluuriast. Sulfoonamiidid, sealhulgas Bactrim, võivad esile kutsuda diureesi suurenemist, eriti südameödeemiga patsientidel.
Üldised häired ja manustamiskoha reaktsioonid
Bactrim perfusiooni intravenoosne infusioon on aeg -ajalt põhjustanud kohalikke kõrvaltoimeid kerge kuni mõõduka veenivalu ja flebiidi kujul.
TM-SMZ ohutus HIV-positiivsetel patsientidel
Võimalike kõrvaltoimete spektri poolest on HIV-positiivne patsientide populatsioon sarnane üldpopulatsiooniga. Igal juhul võivad mõned kõrvaltoimed esineda sagedamini ja erineva kliinilise pildiga.
Need erinevused puudutavad järgmisi klasse:
Vere ja lümfisüsteemi häired
Väga tavaline: leukopeenia, granulotsütopeenia ja trombotsütopeenia.
Ainevahetus- ja toitumishäired
Väga tavaline: hüperkaleemia.
Aeg -ajalt: hüponatreemia, hüpoglükeemia.
Seedetrakti häired
Väga tavaline: isutus, iiveldus koos oksendamisega või ilma, kõhulahtisus.
Maksa ja sapiteede häired
Transaminaaside aktiivsuse tõus.
Naha ja nahaaluskoe kahjustused
Väga tavaline: makulopapulaarne lööve, millega tavaliselt kaasneb sügelus.
Üldised häired ja manustamiskoha reaktsioonid
Väga tavaline: palavik, millega tavaliselt kaasnevad makulopapulaarsed pursked.
04.9 Üleannustamine
Teoreetiliselt on võimalik: kristallide ilmumine uriini, oliguuria või anuuria; iiveldus, oksendamine, kõhulahtisus, peavalu, pearinglus.
Mürgistuse korral tuleb sõltuvalt sümptomitest ette näha: maoloputus, piisav vedeliku tarbimine, et kiirendada neerude kaudu eritumist, hemodialüüs, verevalemi kontroll ja selle muutumise korral 6–12 mg folinaadi manustamine. jalgpallist.
05.0 FARMAKOLOOGILISED OMADUSED
05.1 Farmakodünaamilised omadused
Farmakoterapeutiline rühm: antibakteriaalne süsteemseks kasutamiseks.
ATC -kood: J01EE01.
Bactrim on näide sünergistest kahe aine vahelise täiustamisega. See seos toob kaasa suurema farmakoloogilise toime kui üksikute komponentide individuaalne toime, kuna need toimivad samaaegselt kahel järjestikusel bakteriaalse metabolismi punktis.
Nagu kõik sulfoonamiidi toimega ained, konkureerib SMZ ka p-aminobensoehappe bakterite omastamisega, pärssides seega foolhappe sünteesi; sekkudes eranditult bakteriaalsesse protsessi, ei kahjusta see inimese rakke.
TM toimib järgmisel ensümaatilisel etapil, blokeerides bakteriaalse dihüdrofool-reduktaasi ja tõhustades seeläbi eelmise inhibeerimise toimet. TM-i afiinsus selle bakteriaalse ensüümi suhtes on vähemalt 10 000 korda suurem kui inimese rakuensüümil: selle blokeeriv toime on seega valikuline.
Kahe aine poolt juhitava kahekordse järjestikuse ploki tagajärjel on nende seostamise tulemus ülitundlik, millel on bakteritsiidne toime.
Bactrimi toime spekter on väga lai ja sisaldab arvukalt Gram + ja Gram-mikroobe, näiteks streptokokke (A-rühma β-hemolüütilise streptokoki põhjustatud infektsioonide korral ei ole terapeutiline toime alati rahuldav), stafülokokid, pneumokokid, meningokokid, gonokokid, Bordetella, salmonellae, Klebsiella / Aerobacter, shigellae ja koolera vibrio.
Bactrim toimib ka teatud mikroobidele, mida on raske rünnata: Haemophilus influenzae, Escherichia coli, Proteus mirabilis ja Proteus vulgaris.
05.2 Farmakokineetilised omadused
Bactrimi kahe komponendi imendumine ja vere kineetika kattuvad rahuldavalt. Mõlemad ravimid imenduvad soolestikus väga kiiresti ja jaotuvad kudedesse, levides röga, sülje, trahheobronhiaalsete sekretsioonide, vesivedeliku, tserebrospinaalvedeliku, tupe sekretsiooni, sünoviaalvedeliku ja eesnäärme kaudu. .
Nii trimetoprimi kui ka sulfametoksasooli poolväärtusaeg plasmas on ligikaudu 12 tundi ja need erituvad suures koguses uriiniga.
05.3 Prekliinilised ohutusandmed
Suukaudne LD50 hiirtel on 4200 mg / kg.
06.0 FARMATSEUTILINE TEAVE
06.1 Abiained
Bactrim 80 mg + 400 mg tabletid
povidoon, naatriumtärklisglükolaat, magneesiumstearaat, naatriumdioktüülsulfosuktsinaat.
Bactrim 160 mg + 800 mg tabletid
povidoon K30, magneesiumstearaat, naatriumdokusaat, naatriumtärklisglükolaat.
Bactrim 160 mg + 800 mg lahustuvad tabletid
mikrokristalne tselluloos, naatriumtärklisglükolaat, naatriumdioktüülsulfosuktsinaat, sahhariin, magneesiumstearaat, maisitärklis.
Bactrim 40 mg / 5 ml + 200 mg / 5 ml suukaudne suspensioon
70% kristalliseerumatu sorbitool, mikrokristalne tselluloos, naatriumkarboksümetüültselluloos, metüülparahüdroksübensoaat, propüülparahüdroksübensoaat, naatriumsahhariin, polüsorbaat 80, ammooniumglütsürritsinaat, karamellimaitse, banaanimaitse, vanilje maitse, glütserool, alkohol, naatriumedetaat, puhastatud vesi
Bactrim 80 mg / 5 ml + 400 mg / 5 ml suukaudne suspensioon
mikrokristalne tselluloos, naatriumkarboksümetüültselluloos, metüülparahüdroksübensoaat, propüülparahüdroksübensoaat, 70% mittekristalliseeruv sorbitool, sahhariin, polüsorbaat 80, ammooniumglütsürritsinaat, karamellimaitse, banaanimaitse, vanilje maitse, alkohol, glütserool, naatriumedetaat, puhastatud vesi
06.2 Sobimatus
Praeguseks ei ole teada konkreetseid vastuolusid.
06.3 Kehtivusaeg
Avamata pakendi aegumiskuupäev: 5 aastat.
06.4 Säilitamise eritingimused
Säilitamise erinõuded puuduvad.
06.5 Vahetu pakendi iseloomustus ja pakendi sisu
Tabletid
Blisterpakendid, mis on valmistatud termovormitud plastmaterjalist koos alumiiniumlindiga.
Lahustuvad tabletid, suukaudne suspensioon
Pudelid tumedast klaasist (merevaigukollane), keeratava korgiga termoplastilisest materjalist.
Erinevad mahutid on pakendilehega (ja kahe suukaudse suspensiooni pakendi plastikust mõõtetopsiga) kaasas vastavas pappkarbis.
06.6 Kasutamis- ja käsitsemisjuhised
Suukaudne suspensioon: enne kasutamist loksutada hoolikalt.
07.0 MÜÜGILOA HOIDJA
Roche S.p.A. - Piazza Durante 11 - 20131 Milano
08.0 MÜÜGILOA NUMBER
"80 mg + 400 mg tabletid" 20 tabletti AIC nr 021978010
"160 mg + 800 mg tabletid" 16 tabletti AIC nr 021978046
"40 mg / 5 ml + 200 mg / 5 ml suukaudne suspensioon" 1 pudel 100 ml AIC nr 021978059
"80 mg / 5 ml + 400 mg / 5 ml suukaudne suspensioon" 1 pudel 100 ml AIC nr 021978061
"160 mg + 800 mg lahustuvaid tablette" 16 lahustuvat tabletti AIC nr 021978097
09.0 MÜÜGILOA VÕI UUENDAMISE KUUPÄEV
Uuendamine: juuni 2010
10.0 TEKSTI LÄBIVAATAMISE KUUPÄEV
Juuni 2013