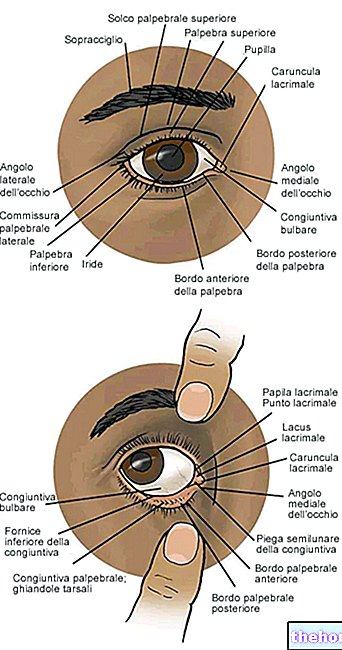
Määratlus
Ensüümid on taime- ja loomarakkudes toodetud valgud, mis toimivad katalüsaatoritena, kiirendades bioloogilisi reaktsioone ilma neid muutmata.
Ensüümid töötavad, kombineerides neid konkreetse ainega, muutes selle teiseks aineks; klassikalisi näiteid toovad süljes, maos, kõhunäärmes ja peensooles esinevad seedeensüümid, mis täidavad seedimisel olulist funktsiooni ja aitavad lagundada toidu põhikomponentideks, mida organism saab seejärel imenduda ja kasutada, töödelda teiste ensüümide või eritub jäätmetena.
Igal ensüümil on spetsiifiline roll: see, mis lagundab näiteks rasvu, ei mõjuta valke ega süsivesikuid. Ensüümid on organismi heaolu jaoks hädavajalikud. Isegi ühe ensüümi puudus võib põhjustada tõsiseid häireid. Tuntud näide on fenüülketonuuria (PKU), haigus, mida iseloomustab võimetus asendada olulisi aminohappeid. fenüülalaniin, mille kogunemine võib põhjustada füüsilisi deformatsioone ja vaimuhaigusi.
Biokeemiline uuring
Ensüümid on teatud valgud, millel on bioloogilised katalüsaatorid, st neil on võime lõhkuda reaktsiooni aktiveerimisenergia (Eatt), muutes selle rada nii, et kineetiliselt aeglane protsess oleks kiirem.
Ensüümid suurendavad termodünaamiliselt võimalike reaktsioonide kineetikat ja erinevalt katalüsaatoritest on nad enam -vähem spetsiifilised: seetõttu on neil substraadi spetsiifilisus.
Ensüüm ei osale reaktsiooni stöhhiomeetrias: selleks peab lõplik katalüütiline koht olema identse lähtekohaga.
Katalüütilises tegevuses on peaaegu alati aeglane faas, mis määrab protsessi kiiruse.
Ensüümidest rääkides ei ole õige rääkida tasakaalureaktsioonidest, vaid selle asemel püsiseisund (olek, milles teatud metaboliit moodustub ja seda tarbitakse pidevalt, hoides selle kontsentratsiooni aja jooksul peaaegu konstantsena). Ühe ensüümi poolt katalüüsitud reaktsiooni produkt on tavaliselt ise järgneva reaktsiooni reagent, mida katalüüsib teine ensüüm jne.
Ensüümide poolt katalüüsitavad protsessid koosnevad tavaliselt reaktsioonijärjestustest.
Ensüümi (E) katalüüsitud üldise reaktsiooni võib kokku võtta järgmiselt:

E on ensüüm
S on substraat;
ES tähistab ensüümi ja substraadi vahelist addukti;
P on toode;
K on reaktsiooni kiiruskonstant.
Geneeriline ensüüm (E) kombineerub substraadiga (S), moodustades addukti (ES) kiiruskonstandiga K1; see võib dissotsieeruda tagasi kiiruseks E + S kiiruskonstandiga K2 või (kui "elab" piisavalt kaua) ) võib kiiruskonstandiga K3 edasi liikuda P -vormini.
Produkt (P) võib omakorda ensüümiga rekombineeruda ja addukti reformida kiiruskonstandiga K4.
Kui ensüüm ja substraat on segatud, on murdosa ajast, mil kahe liigi kohtumine pole veel toimunud: see tähendab, et ensüümi ja substraadi vahel on äärmiselt lühike ajavahemik (mis sõltub reaktsioonist) pole veel täidetud; pärast seda perioodi puutuvad ensüüm ja substraat suuremas koguses kokku ning moodustub ES addukt. Seejärel toimib ensüüm substraadile ja toode vabaneb. Seejärel võib öelda, et c "on esialgne ajavahemik, mille jooksul ei saa ES -addukti kontsentratsiooni määratleda; pärast seda perioodi eeldatakse, et püsiseisund on kindlaks määratud, see tähendab, et addukti saamiseni viivate protsesside kiirus on võrdne nende protsesside kiirusega, mis viivad addukti hävitamiseni.
Michaelis-Menteni konstant (KM) on tasakaalukonstant (viidatud esimesele ülalkirjeldatud tasakaalule); hea lähendusega võib öelda (sest arvestada tuleks ka K3 -ga), et KM -i esindab suhe kineetiliste konstandite K2 ja K1 vahel (viidatud addukti ES hävimisele ja moodustumisele esimeses kirjeldatud tasakaalus) .
Michaelis-Menteni konstandi kaudu on meil "märge ensüümi ja substraadi vahelise afiinsuse kohta: kui KM on väike c" on "kõrge afiinsus ensüümi ja substraadi vahel, siis on ES addukt stabiilne.
Ensüümid on reguleeritud (või moduleeritud).
Varem räägiti peamiselt negatiivsest moduleerimisest, st ensüümi katalüütiliste võimete pärssimisest, kuid võib esineda ka positiivset moduleerimist, see tähendab, et on liike, mis on võimelised ensüümi katalüütilisi võimeid suurendama.
Inhibeerimisi on 4 tüüpi (saadud mudeli ligikaudsetest tulemustest, et viia katseandmed kokku matemaatiliste võrranditega):
- konkurentsivõimeline pärssimine
- mittekonkureeriv pärssimine
- konkurentsivõimetu pärssimine
- konkurentsivõimeline pärssimine
Me räägime konkurentsivõimelisest pärssimisest, kui molekul (inhibiitor) on võimeline substraadiga konkureerima. Struktuurilise sarnasuse huvides võib inhibiitor substraadi asemel reageerida; siit ka terminoloogia "konkureeriv pärssimine". Ensüümi seondumise tõenäosus inhibiitori või substraadiga sõltub mõlema kontsentratsioonist ja nende afiinsusest ensüümiga; reaktsioonikiirus sõltub seega nendest teguritest.
Et saada sama reaktsioonikiirus kui ilma inhibiitorita, on vajalik suurem substraadi kontsentratsioon.
Eksperimentaalselt on näidatud, et inhibiitori juuresolekul suureneb Michaelis-Menteni konstant.
Mis puutub selle asemel "mittekonkureerivasse pärssimisse, siis vastastikmõju molekuli, mis peaks toimima modulaatorina (positiivne või negatiivne inhibiitor) ja" ensüümi vahel, kohas, mis erineb interaktsiooni kohast ensüümi ja substraadi vahel; seetõttu räägime allosteerilisest moduleerimisest (kreeka keelest allosteros → muu sait).
Kui inhibiitor seondub ensüümiga, võib see esile kutsuda ensüümi struktuuri muutuse ja järelikult vähendada substraadi ensüümiga seondumise efektiivsust.
Seda tüüpi protsessides jääb Michaelis-Menteni konstant konstantseks, kuna see väärtus sõltub ensüümi ja substraadi tasakaalust ning isegi inhibiitori juuresolekul need tasakaalud ei muutu.
Ebakompetentse pärssimise nähtus on haruldane; tüüpiline konkurentsivõimetu inhibiitor on aine, mis seondub pöörduvalt ES -i adduktiga, põhjustades ESI -d:

Substraadi üleliigne pärssimine võib mõnikord olla konkurentsivõimetu, kuna see juhtub siis, kui teine substraadi molekul seondub ES -kompleksiga, põhjustades ESS -kompleksi.
Teisest küljest võib konkurentsivõimeline inhibiitor seonduda ainult substraadi ensüümiaduktiga nagu eelmisel juhul: substraadi seondumine vaba ensüümiga kutsub esile konformatsioonilise modifikatsiooni, mis muudab saidi inhibiitorile ligipääsetavaks.
Michaelis Menteni konstant väheneb, kui inhibiitori kontsentratsioon suureneb: ilmselt suureneb seetõttu ensüümi afiinsus substraadi suhtes.
Seriini proteaas
Need on ensüümide perekond, kuhu kuuluvad kümotrüpsiin ja trüpsiin.
Kimotrüpsiin on proteolüütiline ja hüdrolüütiline ensüüm, mis lõikab hüdrofoobsetest ja aromaatsetest aminohapetest paremale.
Kimotrüpsiini kodeeriva geeni produkt ei ole aktiivne (see aktiveeritakse käsuga); kümotrüpsiini mitteaktiivset vormi esindab 245 aminohappest koosnev polüpeptiidahel. Kümotrüpsiin on kerakujuline viie disulfiidsilla ja muude väiksemate vastasmõjude tõttu (elektrostaatiline, Van der Waalsi jõud, vesiniksidemed jne).
Kümotrüpsiini toodavad kõhunäärme kümoosrakud, kus see sisaldub spetsiaalsetes membraanides ja väljutatakse kõhunäärme kanali kaudu soolestikku toidu seedimise ajal: kümotrüpsiin on tegelikult seedeensüüm. Dieediga allaneelatud valgud ja toitained lagundatakse väiksemateks ahelateks, imenduvad ja muundatakse energiaks (nt amülaasid ja proteaasid lagundavad toitaineid veresoonte kaudu rakkudesse jõudvateks glükoosideks ja aminohapeteks) nad jõuavad portaalveeni ja sealt edasi maksa, kus neid täiendavalt ravitakse).
Ensüüme toodetakse mitteaktiivses vormis ja need aktiveeritakse alles siis, kui nad jõuavad "kohale, kus nad peavad töötama"; kui nende tegevus on lõpetatud, deaktiveeritakse need. Pärast desaktiveerimist ei saa ensüümi uuesti aktiveerida: "edasiseks katalüütiliseks toimimiseks" tuleb see asendada teise ensüümimolekuliga. Kui kimitrüpsiini toodetaks aktiivses vormis juba kõhunäärmes, siis see ründaks viimast: pankreatiit on patoloogia, mis on tingitud seedetrakti ensüümidest, mis on juba aktiveeritud kõhunäärmes (ja mitte vajalikes kohtades); mõned neist, kui neid ei ravita õigeaegselt, viia surma.
Kümotrüpsiinis ja kõigis seriinproteaasides on katalüütiline toime tingitud alkoholi aniooni (-CH2O-) olemasolust seriini külgahelas.
Seriini proteaasid võtavad selle nime just seetõttu, et nende katalüütiline toime on tingitud seriinist.
Kui kogu ensüüm on oma toimingu teinud, tuleb see enne substraadile taaskasutamist veega taastada; seriini "vabanemine" vee poolt on protsessi kõige aeglasem etapp ja see on see faas mis määrab katalüüsi kiiruse.
Katalüütiline toime toimub kahes etapis:
- katalüütiliste omadustega aniooni (anioonalkoholaat) moodustumine ja sellele järgnev nukleofiilne rünnak karbonüülsüsinikule (C = O) koos peptiidsideme lõhustumise ja estri moodustamisega;
- veerünnak koos katalüsaatori taastamisega (suudab uuesti katalüütilist toimet avaldada).
Erinevad seriinproteaasi perekonda kuuluvad ensüümid võivad koosneda erinevatest aminohapetest, kuid nende kõigi puhul on katalüütilist saiti esindatud seriini külgahela alkohoolne anioon.
Seriinproteaaside alamperekond on hüübimises osalevate ensüümide alamperekond (mis seisneb valgu muundamises nende mitteaktiivsest vormist "teiseks aktiivseks vormiks"). Need ensüümid tagavad, et hüübimine on võimalikult tõhus ja piiratud ruum ja aeg (hüübimine peab toimuma kiiresti ja see peab toimuma ainult vigastatud ala läheduses). Hüübimisega seotud ensüümid aktiveeritakse kaskaadis (ühe ensüümi aktiveerimisel saadakse miljardeid ensüüme: iga aktiveeritud ensüüm , aktiveerib omakorda paljusid teisi ensüüme).
Tromboos on patoloogia, mis on tingitud hüübimisensüümide talitlushäiretest: selle põhjuseks on hüübimisel kasutatavate ensüümide aktiveerimine ilma vajaduseta (kuna vigastusi pole).
Teiste ensüümide jaoks on olemas moduleerivad (reguleerivad) ensüümid ja inhibeerivad ensüümid: viimastega suheldes reguleerivad või pärsivad nad nende aktiivsust; isegi ensüümi produkt võib olla ensüümi inhibiitor.On ka ensüüme, mis toimivad rohkem, seda suurem on substraat.
Lüsosüüm
Luigi Pasteur avastas Petri tassil aevastades, et limas on ensüüm, mis on võimeline baktereid tapma: lüsosüüm; kreeka keelest: liso = mis suurus; zimo = ensüüm.
Lüsosüüm on võimeline lagundama bakterite rakuseina. Bakterid ja üldiselt üherakulised organismid vajavad mehaaniliselt vastupidavaid struktuure, mis piiravad nende kuju; bakterite sees on väga kõrge osmootne rõhk, nii et need tõmbavad vett ligi. Plasmamembraan plahvataks, kui poleks rakuseina, mis oleks vastu vee sisenemisele ja piiraks bakteri mahtu.
Rakusein koosneb polüsahhariidahelast, milles vahelduvad N-atsetüülglükoosamiini (NAG) molekulid ja N-atsetüülmuraamhappe (NAM) molekulid; side NAG ja NAM vahel puruneb hüdrolüüsi teel.NAM karboksüülrühm rakuseinas on seotud peptiidsidemega aminohappega.
Erinevate ahelate vahel moodustuvad sillad, mis koosnevad pseudo-peptiidsidemetest: hargnemine on tingitud lüsiinimolekulist; struktuur tervikuna on väga hargnenud ja see annab sellele kõrge stabiilsuse.
Lüsosüüm on antibiootikum (tapab baktereid): see toimib, tekitades bakteri seina pragu; kui see struktuur (mis on mehaaniliselt vastupidav) puruneb, tõmbab bakter vett, kuni see lõhkeb. Lüsosüüm suudab murda β-1,4 glükosiidsideme NAM ja NAG vahel.
Lüsosüümi katalüütilist saiti kujutab soon, mis kulgeb piki ensüümi, millesse polüsahhariidahel on sisestatud: soonesse on paigutatud kuus ahela glükosiidtsüklit.
Soone kolm positsiooni c "on õhuklapp: sellesse asendisse saab paigutada ainult ühe NAG -i, sest NAM, mis on kõrgemate mõõtmetega, ei pääse sisse. Tegelik katalüütiline koht on positsioonide 4 ja 5 vahel: kuna NAG positsioonil kolm, lõikamine toimub NAM ja NAG vahel (ja mitte vastupidi); lõikamine on seega spetsiifiline.
Lüsosüümi toimimiseks on optimaalne pH viis. Ensüümi katalüütilises kohas, st nelja ja viienda positsiooni vahel, on asparagiinhappe ja glutamiinhappe külgahelad.
Homoloogia aste: mõõdab sugulust (st sarnasust) valgu struktuuride vahel.
Lüsosüümi ja laktoosisüntaasi vahel on tugev seos.
Laktoosi süntetaas sünteesib laktoosi (mis on peamine piimasuhkur): laktoos on galaktosüülglükosiid, milles c "on β-1,4 glükosiidside galaktoosi ja glükoosi vahel.
Seetõttu katalüüsib laktoosi süntetaas vastupidist reaktsiooni lüsosüümi katalüüsitavale reaktsioonile (mis lõhustab hoopis β-1,4 glükosiidsideme)
Laktoosi süntetaas on dimeer, see tähendab, et see koosneb kahest valguahelast, millest ühel on katalüütilised omadused ja mis on võrreldav lüsosüümiga ning teine on reguleeriv allüksus.
Raseduse ajal sünteesivad glükoproteiinid piimanäärme rakud galatosüül-transferaasi toimel (selle "järjestuse homoloogia on 40% lüsosüümiga"): see ensüüm on võimeline üle kandma galaktosüülrühma suure energiaga struktuurist glükoproteiini struktuur. Raseduse ajal indutseeritakse galaktoksüültransferaasi kodeeriva geeni ekspressioon (esineb ka teiste geenide ekspressiooni, mis annavad ka teisi tooteid): rinna suurus suureneb, kuna see aktiveerub piimanääre (varem mitteaktiivne), mis peab tootma piima. Sünnituse ajal toodetakse α-laktalbumiini, mis on reguleeriv valk: see on võimeline reguleerima galaktosüültransferaasi katalüütilist võimekust (substraadi eristamise teel). Α-laktalalbumiiniga modifitseeritud galaktosüültransferaas on võimeline kandma galaktosüüli glükoosimolekulile, moodustades β-1,4 glükosiidsideme ja andes laktoosi (laktoosisüntaasi).
Seega valmistab galaktoosi transferaas piimanäärme ette enne sünnitust ja toodab piima pärast sünnitust.
Glükoproteiinide tootmiseks seondub galaktosüültransferaas galaktosüüli ja NAG -ga; sünnituse ajal seostub laktaalne albumiin galaktosüültransferaasiga, mistõttu viimane tunneb ära glükoosi ja ei anna enam laktoosi.




















.jpg)
-a-cosa-serve.jpg)