Toimeained: tafluprost
SAFLUTAN 15 mikrogrammi / ml silmatilgad, lahus
Miks kasutatakse Saflutani? Milleks see mõeldud on?
Mis tüüpi ravim see on ja kuidas see toimib?
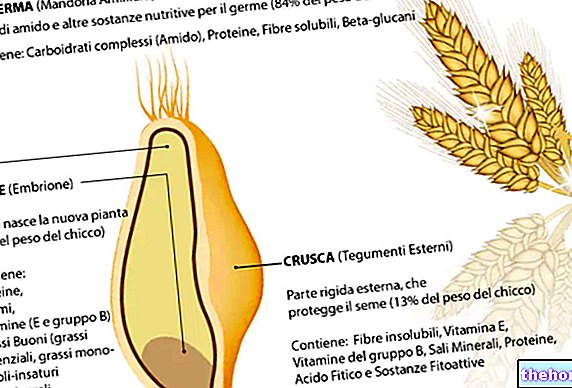
SAFLUTAN silmatilgad sisaldavad tafluprosti, mis kuulub ravimite rühma, mida nimetatakse prostaglandiini analoogideks.SAFLUTAN vähendab silma siserõhku. Seda kasutatakse siis, kui rõhk silma sees on liiga kõrge.
Milleks seda ravimit kasutatakse?
SAFLUTANi kasutatakse glaukoomi tüübi, mida nimetatakse avatud nurga glaukoomiks, raviks, samuti täiskasvanute silmasisese hüpertensiooni raviks. Mõlemad seisundid on seotud silmasisese rõhu suurenemisega ja võivad lõpuks kahjustada nägemist.
Vastunäidustused Kui Saflutani ei tohi kasutada
Ärge kasutage SAFLUTANi, kui olete tafluprosti või selle ravimi mis tahes koostisosade (loetletud lõigus 6) suhtes allergiline.
Ettevaatusabinõud kasutamisel Mida on vaja teada enne Saflutani võtmist
Enne SAFLUTANi kasutamist pidage nõu oma arsti, apteekri või meditsiiniõega
Pidage meeles, et SAFLUTANil võivad olla järgmised toimed, millest mõned võivad olla püsivad:
- SAFLUTAN võib suurendada ripsmete pikkust, paksust, värvi ja / või arvu ning põhjustada silmalaugudel ebatavalist karvakasvu.
- SAFLUTAN võib põhjustada silmade ümbruse naha tumenemist. Eemaldage nahalt lahuse jäägid. See vähendab naha tumenemise ohtu.
- SAFLUTAN võib muuta iirise värvi (silma värviline osa). Kui SAFLUTANi kasutatakse ühes silmas, võib töödeldud silma värv muutuda püsivalt teise silma värvist.
Öelge oma arstile
- kui teil on probleeme neerudega
- kui teil on probleeme maksaga
- kui teil on astma
- kui teil on mõni muu silmahaigus.
Lapsed ja noorukid
SAFLUTANi ei soovitata kasutada lastel ja alla 18 -aastastel noorukitel ohutuse ja efektiivsuse andmete puudumise tõttu.
Koostoimed Millised ravimid või toidud võivad muuta Saflutani toimet
Teatage oma arstile või apteekrile, kui te kasutate või olete hiljuti kasutanud või kavatsete kasutada mis tahes muid ravimeid.
Kui kasutate teisi ravimeid silma, oodake vähemalt 5 minutit SAFLUTANi ja teise ravimi manustamise vahel.
Hoiatused Oluline on teada, et:
Rasedus, imetamine ja viljakus
Kui võite rasestuda, peate SAFLUTAN -ravi ajal kasutama tõhusat rasestumisvastast meetodit. Ärge kasutage SAFLUTANi, kui olete rase. Kui te toidate last rinnaga, ei tohi SAFLUTANi kasutada.
Küsige nõu oma arstilt.
Autojuhtimine ja masinatega töötamine
SAFLUTAN ei mõjuta autojuhtimise ega masinate käsitsemise võimet. Pärast SAFLUTANi manustamist võib teil tekkida ajutine nägemise hägustumine. Ärge juhtige autot ega kasutage tööriistu ega masinaid enne, kui nägemine on taas selge.
Oluline teave mõningate SAFLUTANi koostisainete kohta
SAFLUTAN sisaldab bensalkooniumkloriidi. Bensalkooniumkloriid võib põhjustada silmade ärritust.
Kontaktläätsed
On teada, et bensalkooniumkloriid muudab pehmete kontaktläätsede värvi. Seetõttu vältige kokkupuudet pehmete kontaktläätsedega.
Eemaldage kontaktläätsed enne paigaldamist ja oodake vähemalt 15 minutit, enne kui need tagasi panete.
Annus, manustamisviis ja aeg Kuidas Saflutani kasutada: Annustamine
Kasutage seda ravimit alati täpselt nii, nagu arst või apteeker on teile rääkinud. Kahtluse korral pidage nõu oma arsti või apteekriga.
Soovitatav annus on 1 tilk SAFLUTANi mõlemasse ravitavasse silma üks kord päevas õhtul. Ärge tilgutage rohkem tilka ja ärge kasutage ravimit sagedamini, kui arst on määranud. See võib muuta SAFLUTANi vähem tõhusaks.
Kasutage SAFLUTANi mõlemas silmas ainult siis, kui arst on seda määranud. Kasutada ainult silmatilgadena. Ära alla neela.
Kasutusjuhend:
Uue pudeli käivitamisel:
Ärge kasutage pudelit, kui korki ja kaela kattev plastkile puudub või on terve. Eemaldage plastkile. Kirjutage pudeli avamise kuupäev välispakendile ettenähtud kohta.
Kui te kasutate SAFLUTANi
- Peske käsi.
- Avage pudel. Olge eriti ettevaatlik, et tilguti pudeli ots ei puudutaks teie silma, silmaümbruse nahka ega sõrmi.
- Kallutage pea taha ja keerake pudel tagurpidi üle silma.
- Tõmbad alumise silmalau alla ja vaatad üles. Vajutage pudelile kerget survet, et tilk silmatilku langeks alumise kaane ja silma vahele
- Sulgege korraks oma silm ja suruge sõrmega silma sisenurka umbes minuti jooksul, see aitab vältida silmatilkade voolamist läbi pisarakanali.
- Eemaldage silmaümbruse nahale jäänud lahuse jäägid.
- Pange kork tagasi ja sulgege pudel tihedalt.
Kui tilk ei sattu silma, korrake toimingut.
Kui arst on teile käskinud tilgutada mõlemasse silma, korrake samme 3 kuni 7 teise silma jaoks.
Kui te kasutate oma silmadele muid ravimeid, oodake SAFLUTANi ja teise ravimi manustamise vahel vähemalt 5 minutit.
Kui te unustate SAFLUTANi kasutada, tilgutage üks tilk niipea, kui see teile meenub, ja naaske seejärel oma tavapäraste annustamisaegade juurde. Ärge kasutage kahekordset annust, kui annus jäi eelmisel korral võtmata.
Ärge lõpetage SAFLUTANi kasutamist ilma arstiga nõu pidamata. Kui te lõpetate SAFLUTANi võtmise, tõuseb silmasisene rõhk uuesti. See võib põhjustada püsivaid silmakahjustusi.
Kui teil on lisaküsimusi selle ravimi kasutamise kohta, pidage nõu oma arsti, apteekri või meditsiiniõega.
Üleannustamine Mida teha, kui olete võtnud liiga palju saflutani
Kui te kasutate SAFLUTANi rohkem kui ette nähtud, ei põhjusta see tõenäoliselt tõsiseid tagajärgi. Kandke järgmine annus tavalisel ajal.
Kui ravim on kogemata alla neelatud, küsige nõu oma arstilt.
Kõrvaltoimed Millised on Saflutani kõrvaltoimed
Nagu kõik ravimid, võib ka see ravim põhjustada kõrvaltoimeid, kuigi kõigil neid ei teki. Enamik kõrvaltoimeid ei ole tõsised.
Väga sageli esinevad kõrvaltoimed
Järgmised toimed võivad esineda rohkem kui 1 inimesel 10 -st:
Mõju silmadele:
- silma punetus.
Sageli esinevad kõrvaltoimed
Järgmised toimed võivad esineda kuni 1 inimesel 10 -st:
Mõju närvisüsteemile:
- peavalu
Mõju silmadele:
- sügelev silm
- silmade ärritus
- valu silmas
- ripsmete pikkuse, paksuse ja arvu muutused
- kuiv silm
- võõrkeha tunne silmas
- ripsmete värvimuutus
- silmalaugude punetus
- väikesed põletikulised alad silma pinnal
- tundlikkus valguse suhtes
- suurenenud pisaravool
- ähmane nägemine
- silma võime eristada detaile
- iirise värvimuutus (võib olla püsiv)
Aeg -ajalt esinevad kõrvaltoimed
Järgmised toimed võivad esineda kuni 1 inimesel 100 -st:
Mõju silmadele:
- silmade ümbruse naha värvimuutus
- silmalaugude turse
- väsinud silmad
- silma pindmiste membraanide turse
- silma eritis
- silmalaugude põletik
- põletiku tunnused silma sees
- ebamugavustunne silmas
- silma pinnamembraanide pigmentatsioon
- folliikulid silma pinnamembraanides
- allergiline põletik
- ebanormaalne tunne silmas
Mõju nahale ja nahaaluskoele:
- juuste ebatavaline kasv silmalaugudel.
Teadmata: esinemissagedust ei saa hinnata olemasolevate andmete alusel
Mõju silmadele:
- iirise / uvea põletik (silma keskmine kiht)
- silmad, mis tunduvad vajunud
Mõju hingamissüsteemile:
- astma süvenemine, õhupuudus
Väga harvadel juhtudel on mõnedel patsientidel, kellel on silma eesmise osa (sarvkesta) selge kihi tõsine kahjustus, tekkinud sarvkestale hägused laigud ravi ajal kaltsiumi kogunemise tõttu.
Kõrvaltoimetest teatamine
Kui teil tekib ükskõik milline kõrvaltoime, pidage nõu oma arsti, apteekri või meditsiiniõega. Kõrvaltoime võib olla ka selline, mida selles infolehes ei ole nimetatud. Kõrvaltoimetest võite ka ise teavitada riikliku teavitussüsteemi kaudu aadressil www.agenziafarmaco.gov. It / it / vastutav. Kõrvaltoimetest teatades saate aidata saada lisateavet selle ravimi ohutuse kohta.
Aegumine ja säilitamine
Hoidke seda ravimit laste eest varjatud ja kättesaamatus kohas.
Ärge kasutage seda ravimit pärast kõlblikkusaega, mis on märgitud pudelil ja karbil pärast „EXP“. Kõlblikkusaeg viitab kuu viimasele päevale.
Hoida temperatuuril kuni 25 ° C.
Hoida originaalpakendis.
Nakkuste vältimiseks visake pudel ära 28 päeva pärast esmakordset avamist ja kasutage uut.
Ärge visake ravimeid kanalisatsiooni ega olmejäätmete hulka. Küsige oma apteekrilt, kuidas visata ära ravimeid, mida te enam ei kasuta. See aitab kaitsta keskkonda.
Tähtaeg "> Muu teave
Mida SAFLUTAN sisaldab
- Toimeaine on tafluprost. 1 ml lahust sisaldab 15 mikrogrammi tafluprosti. Üks pudel (2,5 ml) silmatilku, lahus, sisaldab 37,5 mikrogrammi tafluprosti.
- Abiained on bensalkooniumkloriid (säilitusaine), glütserool, naatriumdivesinikfosfaatdihüdraat, dinaatriumedetaat, polüsorbaat 80 ja süstevesi. PH reguleerimiseks lisatakse vesinikkloriidhapet ja / või naatriumhüdroksiidi.
Kuidas SAFLUTAN välja näeb ja pakendi sisu
SAFLUTAN on selge ja värvitu vedelik (lahus), mis on pakitud 1 või 3 läbipaistva plastpudeliga, millest igaüks sisaldab 2,5 ml lahust.
Plastpudelid suletakse keeratava korgiga.
Kõik pakendi suurused ei pruugi olla müügil.
Allika pakendi infoleht: AIFA (Itaalia ravimiamet). Sisu avaldati jaanuaris 2016. Esitatud teave ei pruugi olla ajakohane.
Kõige ajakohasemale versioonile juurdepääsu saamiseks on soovitatav külastada AIFA (Itaalia ravimiamet) veebisaiti. Vastutusest loobumine ja kasulik teave.
01.0 RAVIMPREPARAADI NIMETUS -
SAFLUTAN 15 mikrogrammi / ml silmatilgad, lahus
02.0 KVALITATIIVNE JA KVANTITATIIVNE KOOSTIS -
Üks ml silmatilku lahuses sisaldab 15 mikrogrammi tafluprosti.
Üks pudel (2,5 ml) silmatilku, lahus, sisaldab 37,5 mikrogrammi tafluprosti.
Abiaine: 0,1 mg bensalkooniumkloriidi 1 ml silmatilkade lahuses.
Abiainete täielik loetelu vt lõik 6.1.
03.0 RAVIMVORM -
Silmatilgad, lahus (silmatilgad).
Selge ja värvitu lahus.
04.0 KLIINILINE TEAVE -
04.1 Näidustused -
Kõrgenenud silmasisese rõhu vähendamine avatud nurga glaukoomi ja silma hüpertensiooni korral.
Monoteraapiana patsientidel
• kes on esmavaliku ravile ebapiisavalt reageerinud
• kes ei talu või kellele esmavaliku ravi on vastunäidustatud
Täiendava ravina beetablokaatoritele.
SAFLUTAN on näidustatud ≥ 18 -aastastele täiskasvanutele.
04.2 Annustamine ja manustamisviis
Annustamine
Soovitatav annus on üks tilk SAFLUTANi kahjustatud silma (te) konjunktiivikotti üks kord päevas, õhtul.
Annus ei tohi ületada ühte ööpäevast manustamist, kuna sagedasem manustamine võib vähendada silmasisese rõhu hüpotensiivset toimet.
Kasutamine eakatel:
Eakatel patsientidel ei ole annuse kohandamine vajalik.
Lapsed:
Tafluprosti ohutus ja efektiivsus alla 18 -aastastel lastel ei ole veel tõestatud. Andmed puuduvad.
Kasutamine neeru- / maksakahjustuse korral
Tafluprosti ei ole neeru- / maksakahjustusega patsientidel uuritud, seetõttu tuleb seda ravimit nendel patsientidel kasutada ettevaatusega.
Manustamisviis
Lahuse võimaliku saastumise vältimiseks ei tohi patsiendid puudutada pudeli aplikaatoriga oma silmalauge, ümbritsevaid alasid ega muud pinda.
Silmalaugude naha tumenemise ohu vähendamiseks peavad patsiendid pühkima nahalt lahuse jäägid. Nagu kõigi teiste silmatilkade puhul, on pärast manustamist soovitatav ninakõrva sulgemine või silmalau õrn sulgemine, mis võib vähendada silmaravimite süsteemset imendumist.
Kui kasutatakse rohkem kui ühte paikset oftalmoloogilist ravimit, tuleb iga ravimit manustada vähemalt 5 -minutilise vahega.
04.3 Vastunäidustused -
Ülitundlikkus toimeaine tafluprosti või lõigus 6.1 loetletud mis tahes abiainete suhtes.
04.4 Erihoiatused ja ettevaatusabinõud kasutamisel -
Enne ravi alustamist tuleb patsiente teavitada ripsmete pikenemise, silmalaugude naha tumenemise ja iirise pigmentatsiooni suurenemise võimalusest. Mõned neist muutustest võivad olla püsivad ja võivad põhjustada silmade erinevusi ainult ühe silma korral. silma ravitakse.
Vikerkesta pigmentatsiooni muutus toimub aeglaselt ja ei pruugi olla märgatav mitme kuu jooksul.Silmavärvi muutust on täheldatud peamiselt segavärviliste iiristega patsientidel, näiteks sinakaspruun, hallikaspruun, kollakaspruun ja rohekaspruun. Ühepoolse ravi korral on püsiva heterokroomia oht ilmne.
Puuduvad kogemused tafluprosti kasutamise kohta neovaskulaarse, kitsa nurga, kitsa nurga või kaasasündinud glaukoomiga patsientidel. Tafluprosti kasutamise kohta afakiaga patsientidel ja pigmentaalse või pseudoeksfoliatiivse glaukoomi korral on vähe kogemusi.
Tafluprosti kasutamisel tuleb olla ettevaatlik afaakilistel, pseudofaakilistel patsientidel, kellel on läätse tagumise kapsli rebend või eesmised kambri läätsed, või patsientidel, kellel on teadaolevad tsüstilise makulaarse turse või iriidi / uveiidi riskifaktorid.
Raske astmaga patsientide kohta kogemused puuduvad, seetõttu tuleb selliseid patsiente ravida ettevaatusega.
On teatatud, et bensalkooniumkloriid, mida tavaliselt kasutatakse oftalmoloogiliste toodete säilitusainena, põhjustab punktkeratopaatiat ja / või toksilist haavandilist keratopaatiat. Kuna SAFLUTAN sisaldab bensalkooniumkloriidi, tuleb sagedase või pikaajalise kasutamise korral kuiva silmaga või sarvkesta kahjustusega patsientidel hoolikalt jälgida.
SAFLUTAN sisaldab bensalkooniumkloriidi, mis võib põhjustada silmade ärritust. Vältige kokkupuudet pehmete kontaktläätsedega. Eemaldage kontaktläätsed enne paigaldamist ja oodake vähemalt 15 minutit, enne kui need tagasi panete. Bensalkooniumkloriid muudab pehmete kontaktläätsede värvi.
04.5 Koostoimed teiste ravimitega ja muud koostoimed -
Inimestel ei ole oodata koostoimeid, kuna tafluprosti süsteemne kontsentratsioon on pärast silma manustamist äärmiselt madal, seetõttu ei ole tafluprostiga tehtud spetsiifilisi koostoimeuuringuid teiste ravimitega.
Kliinilistes uuringutes kasutati tafluprosti koos timolooliga ilma koostoimeteta.
04.6 Rasedus ja imetamine -
Fertiilses eas naised / rasestumisvastased vahendid
SAFLUTANi ei tohi kasutada fertiilses eas naised, välja arvatud juhul, kui on olemas piisavad rasestumisvastased vahendid (vt lõik 5.3).
Rasedus
Tafluprosti kasutamise kohta rasedatel ei ole piisavalt andmeid.
Tafluprostil võib olla kahjulik farmakoloogiline toime rasedusele ja / või lootele / vastsündinule.
Loomkatsed on näidanud reproduktiivtoksilisust (vt lõik 5.3). Seetõttu ei tohi SAFLUTANi raseduse ajal kasutada, kui see pole absoluutselt vajalik (kui muud ravivõimalused puuduvad).
Toitmisaeg
Ei ole teada, kas tafluprost või selle metaboliidid erituvad rinnapiima. Rottidel läbi viidud uuring näitas tafluprosti ja / või selle metaboliitide eritumist rinnapiima pärast paikset manustamist (vt lõik 5.3).
Seetõttu ei tohi tafluprosti imetamise ajal kasutada.
Viljakus
Isastel ja emastel rottidel ei mõjutanud tafluprosti intravenoosne annus kuni 100 mikrogrammi / kg ööpäevas paaritusvõimet ja viljakust.
04.7 Toime autojuhtimise ja masinate käsitsemise võimele -
Tafluprost ei mõjuta autojuhtimise ega masinate käsitsemise võimet. Nagu iga oftalmoloogilise ravi korral, peab patsient pärast instillatsiooni nägemise mööduvat hägustumist ootama, kuni nägemine selgub, enne autojuhtimist või masinatega töötamist.
04.8 Kõrvaltoimed -
Kliinilistes uuringutes said rohkem kui 1400 patsienti ravi säilitusaine tafluprostiga kas monoteraapiana või 0,5% timolooli lisandina. Kõige sagedamini raviga seotud kõrvalnäht oli silma hüpereemia. Seda esines ligikaudu 13% patsientidest, kes osalesid Euroopas ja USA -s säilitusaine tafluprosti kliinilistes uuringutes. Enamikul juhtudel oli see sündmus kerge ja viis ravi katkestamiseni keskmiselt 0,4% pilootuuringutes osalenud patsientidest. USA-s läbi viidud 3-kuulises III faasi uuringus, milles võrreldi tafluprosti säilitusaineteta preparaati säilitusainetevaba timolooliga, tekkis silma hüpereemia 4,1% -l (13/320) tafluprosti saanud patsientidest.
Tafluprostiga läbi viidud kliinilistes uuringutes Euroopas ja USA-s täheldati pärast maksimaalselt 24-kuulist jälgimist järgmisi raviga seotud kõrvaltoimeid:
Igas sagedusklassis on kõrvaltoimed teatatud esinemissageduse kahanevas järjekorras.
Närvisüsteemi häired
Sage (≥1 / 100, peavalu
Silma häired
Väga sage (≥1 / 10): konjunktiiv / silma hüpereemia
Sage (≥ 1/100, silmade sügelus, silmade ärritus, silmavalu, ripsmete muutused (pikkuse, paksuse ja arvu suurenemine), silmade kuivus, võõrkeha tunne silmas, ripsmete värvimuutus, silmalaugude erüteem, pindmine keratiit (CPS) , valgusfoobia, suurenenud pisaravool, hägune nägemine, vähenenud nägemisteravus ja suurenenud vikerkesta pigmentatsioon.
Aeg -ajalt (≥ 1/1 000, palpebide turse, astenoopia, sidekesta turse, silma eritis, blefariit, rakkude esinemine eeskambris, ebamugavustunne silmas, venitus väljaspool eesmist kambrit, sidekesta pigmentatsioon, sidekesta folliikulid, allergiline konjunktiviit ja ebanormaalsed aistingud silma.
Teadmata (esinemissagedust ei saa hinnata olemasolevate andmete alusel): iriit / uveiit, silmalaugude süvend.
Väga harva on teatatud sarvkesta lupjumise juhtudest seoses fosfaati sisaldavate silmatilkade kasutamisega mõnedel märkimisväärselt kahjustatud sarvkestaga patsientidel.
Hingamisteede patoloogiad
Teadmata (esinemissagedust ei saa hinnata olemasolevate andmete alusel): astma ägenemine, düspnoe
Naha ja nahaaluskoe kahjustused
Aeg -ajalt (≥1 / 1000, silmalaugude hüpertrichoos
Arvatavatest kõrvaltoimetest teatamine
Pärast ravimi müügiloa väljastamist tekkinud arvatavatest kõrvaltoimetest teatamine on oluline, kuna see võimaldab pidevalt jälgida ravimi kasu ja riski suhet. Tervishoiutöötajatel palutakse teavitada kõigist võimalikest kõrvaltoimetest riikliku teavitussüsteemi kaudu. "Aadress www. agenziafarmaco.gov.it/it/responsabili.
04.9 Üleannustamine -
Üleannustamine pärast silma manustamist on ebatõenäoline.
Üleannustamise korral peab ravi olema sümptomaatiline.
05.0 FARMAKOLOOGILISED OMADUSED
05.1 "Farmakodünaamilised omadused -
Farmakoterapeutiline rühm: glaukoomivastased ravimid ja müootilised preparaadid, prostaglandiinide analoogid
ATC -kood: S01EE05
Toimemehhanism
Tafluprost on prostaglandiin F2α fluoritud analoog. Tafluprostihape, tafluprosti bioloogiliselt aktiivne metaboliit, on väga tugev ja selektiivne inimese prostanoidi FP retseptori agonist. Tafluprostihappe afiinsus FP retseptori suhtes on 12 korda suurem kui latanoprosti puhul. Farmakodünaamilised uuringud ahvidega näitavad, et tafluprost vähendab silmasisest rõhku, suurendades vesivedeliku uveoskleraalset väljavoolu.
Farmakodünaamilised toimed
Katsed normotensiivsetel ahvidel ja okulaarse hüpertensiooniga ahvidel näitasid, et tafluprost on tõhus ühend silmasisese rõhu vähendamiseks. Uuringus, milles hinnati tafluprosti metaboliitide toimet silmasisese rõhu alandamisele, vähendas ainult tafluprostihape silmasisest rõhku oluliselt.
Küülikutel, keda raviti 4 nädalat tafluprosti 0,0015% oftalmoloogilise lahusega üks kord ööpäevas, suurenes nägemisnärvi pea verevool oluliselt (15%) võrreldes algväärtusega, mõõdetuna laigulise täppvoolu abil 14. ja 28. päeval.
Kliiniline efektiivsus
Silmasisese rõhu alanemine algab 2 ... 4 tundi pärast esimest manustamist ja maksimaalne toime saavutatakse ligikaudu 12 tundi pärast tilgutamist. Toime kestus püsib vähemalt 24 tundi. Pilootuuringud tafluprosti preparaadiga, mis sisaldab säilitusainet bensalkooniumkloriidi, on näidanud, et tafluprost on iseenesest efektiivne ja avaldab täiendavat toimet, kui seda manustatakse timolooli täiendava ravina: 6-kuuline uuring näitas, et tafluprost vähendas märkimisväärselt silmasisest rõhku 6 ... 8 mmHg erinevatel kellaaegadel, võrreldes latanoprostiga saadud 7-9 mmHg-ga. Teises 6-kuulises kliinilises uuringus vähendas tafluprost silmasisest rõhku 5 kuni 7 mmHg võrreldes timolooliga saadud 4-6 mmHg-ga. Tafluprosti silmasisest rõhku alandav toime püsis ka nende uuringute pikendamisel kuni 12 kuuni. 6 kuud kestnud uuringus täheldati tafluprosti alandavat toimet silmasisestele rõhku võrreldi selle lahusti rõhuga, kui seda kasutati lisaks timoloolile. Täiendav silmasisese rõhu alandav toime võrreldes algväärtustega (mõõdetud pärast 4-nädalast timolooli manustamist) oli timolool-tafluprosti rühmas 5–6 mmHg ja timolool-kandeaine rühmas 3–4 mmHg. Tafluprosti säilitus- ja säilitusaineteta preparaadid näitasid sarnast toimet, mis alandas silmasisest rõhku üle 5 mmHg väikeses ristuva uuringu käigus, mis kestis 4 nädalat. Peale selle, USA-s läbi viidud 3-kuulises uuringus, milles võrreldi tafluprosti säilitusaineteta preparaati säilitusainetevaba timolooliga, oli tafluprosti toime silmasisese rõhu alandamisel erinevate hindamiste ajal 6,2 kuni 7,4 mmHg. timolool oli vahemikus 5,3 kuni 7,5 mmHg.
05.2 "Farmakokineetilised omadused -
Imendumine
Pärast ühe tilga tafluprosti 0,0015% silmatilkade manustamist silma üks kord ööpäevas 8 päeva jooksul oli tafluprostihappe plasmakontsentratsioon madal ja sarnased profiilid 1. ja 8. päeval. Plasmakontsentratsioonid saavutasid maksimumi 10 minutit pärast manustamist ja vähenesid madalamast avastamislävest (10 pg / ml) alla ühe tunni pärast manustamist. Keskmised Cmax väärtused (24,4 ja 31,4 pg / ml) ja AUC0-viimane (405,9 ja 581,1 pg * min / ml) olid päevadel sarnased 1 ja 8, mis näitab, et silma manustamise esimese nädala jooksul saavutati püsiv ravimi kontsentratsioon. Statistiliselt olulisi erinevusi ei leitud. Süsteemses biosaadavuses säilitusainetega ja ilma.
Küülikutega läbi viidud uuringus oli tafluprosti imendumine vesivedelikku võrreldav pärast ühekordset silma tilgutamist tafluprosti 0,0015% oftalmoloogilise lahusega koos säilitusainega või ilma.
Levitamine
Ahvidel ei täheldatud radioaktiivselt märgistatud tafluprosti spetsiifilist jaotumist iridotsiliaarses kehas või koroidses piirkonnas, sealhulgas võrkkesta pigmendi epiteelis; see viitab madalale afiinsusele melaniini pigmendi suhtes. Kogu organismi autoradiograafia uuringus rottidel oli kõrgeim radioaktiivsust täheldati sarvkestas, millele järgnesid silmalaugud, sklera ja iiris.Väljaspool silma jaotati radioaktiivsus pisaraparaadi, suulae, söögitoru ja trakti vahel.seedetrakt, neerud, maks, sapipõis ja kusepõis.
Happelise tafluprosti seondumine inimese seerumi albumiiniga in vitro oli 99% happelise tafluprosti korral 500 ng / ml.
Biotransformatsioon
Tafluprosti peamine metaboolne rada inimestel, mida on testitud in vitrokoosneb hüdrolüüsist farmakoloogiliselt aktiivseks metaboliidiks, tafluprostihappeks, mis metaboliseerub edasi glükuroniseerimise või beetaoksüdatsiooni teel. mitteaktiivsed, võivad need olla glükuroniseeritud või hüdroksüülitud. Tsütokroom P450 (CYP) ensüümsüsteem ei osale tafluprostihappe metabolismis. Uuringu põhjal küüliku sarvkesta koes ja puhastatud ensüümidega on peamine esteraas, mis vastutab estri hüdrolüüsi eest tafluprostiks hape on karboksüülesteraas. Butüülkoliinesteraas, kuid mitte atsetüülkoliinesteraas, võib samuti kaasa aidata hüdrolüüsile.
Elimineerimine
Pärast ³H-tafluprosti (0,005% oftalmoloogiline lahus; 5 ml / silma) manustamist üks kord ööpäevas 21 päeva jooksul mõlemal silmal rottidel leiti ligikaudu 87% kogu radioaktiivsest annusest väljaheidetest. Kogu uriiniga eritus ligikaudu 27 -38% ja ligikaudu 44 ... 58% annusest eritus väljaheitega.
05.3 Prekliinilised ohutusandmed -
Farmakoloogilise ohutuse, korduvdoosilise süsteemse toksilisuse, genotoksilisuse ja kartsinogeensuse mittekliinilised uuringud ei ole näidanud kahjulikku toimet inimesele. Nagu teistegi PGF2 agonistide puhul, põhjustas tafluprosti korduv annus paikselt manustatuna ahvidele pöördumatut mõju pigmentatsioonile iirise ja palpebraalse lõhe laiuse pöörduv suurenemine.
"Suurenenud emaka kontraktiilsus in vitro Inimese emakapreparaatides ei ole tafluprosti uterotoonilist aktiivsust uuritud.
Reproduktiivtoksilisuse uuringud viidi läbi rottidel ja küülikutel pärast intravenoosset manustamist. Rottidel ei täheldatud kahjulikku toimet viljakusele ega varasele embrüonaalsele arengule, kui süsteemne ekspositsioon ületas maksimaalse kliinilise ekspositsiooni Cmax -i alusel 12 000 korda või AUC -st enam kui 2200 korda.
Tavapärastes embrüo-loote arengu uuringutes põhjustas tafluprost loote kehakaalu languse ja implanteerimisjärgse kaotuse suurenemise. Tafluprost suurendas rottidel luustiku kõrvalekallete esinemissagedust ning küüliku kolju-, aju- ja seljaaju väärarengute esinemissagedust. Küülikute uuringus olid tafluprosti ja selle metaboliitide plasmakontsentratsioonid allpool kvantifitseerimise taset.
Pre- ja postnataalse arengu uuringus rottidel täheldati järglastel suurenenud vastsündinute suremust, kehakaalu vähenemist ja kõrvalesta hilinemist, kui tafluprosti annused ületasid kliinilist annust 20 korda.
Rottidel radioaktiivselt märgistatud tafluprostiga läbi viidud katsed näitasid, et ligikaudu 0,1% silma paikselt manustatud annusest imendus piima. Kuna aktiivse metaboliidi (tafluprostihape) poolväärtusaeg plasmas on väga lühike (inimestel 30 minuti pärast tuvastamatu), oli suurem osa radioaktiivsusest tõenäoliselt tingitud metaboliitidest, millel on vähene farmakoloogiline aktiivsus. Ravimi ja looduslike prostaglandiinide metabolismi põhjal on oodata väga madalat suukaudset biosaadavust.
06.0 FARMATSEUTILINE TEAVE -
06.1 Abiained -
Bensalkooniumkloriid
Glütserool
Naatriumdivesinikfosfaatdihüdraat
Dinaatriumedetaat
Polüsorbaat 80
Vesinikkloriidhape ja / või naatriumhüdroksiid (pH reguleerimiseks)
Süstevesi
06.2 Sobimatus "-
Ei ole asjakohane
06.3 Kehtivusaeg "-
3 aastat.
Pärast pudeli esmakordset avamist: 28 päeva.
06.4 Säilitamise eritingimused -
Hoida temperatuuril kuni 25 ° C.
Hoida originaalpakendis.
06.5 Vahetu pakendi iseloom ja pakendi sisu -
Läbipaistev polüpropüleenpudel polüpropüleenist tilguti otsaga ja suure tihedusega polüetüleenist korgiga. Iga pudeli täitekogus on 2,5 ml.
Saadaval on järgmised pakendi suurused: karbid, mis sisaldavad 1 või 3 2,5 ml pudelit.
Kõik pakendi suurused ei pruugi olla müügil.
06.6 Kasutamis- ja käsitsemisjuhised -
Kasutamata ravim ja sellest tekkinud jäätmed tuleb hävitada vastavalt kohalikele eeskirjadele.
07.0 MÜÜGILOA HOIDJA -
MSD Italia S.r.l.
Via Vitorchiano, 151 - 00189 Rooma
08.0 MÜÜGILOA NUMBER -
15 mikrogrammi / ml silmatilku, lahus
1 pudel 2,5 ml AIC n. 038926010
15 mikrogrammi / ml silmatilku, lahus
3 pudelit 2,5 ml AIC n. 038926022
09.0 MÜÜGILOA VÕI UUENDAMISE KUUPÄEV -
Müügiloa esmase väljastamise kuupäev: mai 2010
Viimane uuendamise kuupäev: veebruar 2014
10.0 TEKSTI LÄBIVAATAMISE KUUPÄEV -
November 2014